(15分)镁铝水滑石[Mg2Al(OH)6Cl·xH2O]在高温下完全分解,其分解方程式为:
2[Mg2Al(OH)6Cl·xH2O] 4MgO+Al2O3+2HCl↑+(5+2x)H2O↑
4MgO+Al2O3+2HCl↑+(5+2x)H2O↑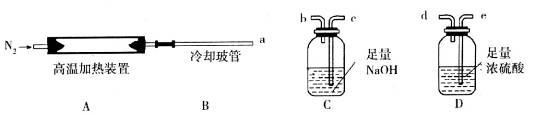
某化学小组现用下图装置进行实验确定其化学式(固定装置略去)。
(1)若只通过测定装置C、D的增重来确定x,则装置的连接顺序为_______________(按气流方向,用接口字母表示)。装置连接后,首先要进行的操作是______________。
(2)加热前先通N2排尽装置中的空气,称取C、D的初始质量后,仍需持续通入N2的作用是
①____________________________②_________________________________。
(3)完全分解后测得C增重3.65 g、D增重9.90 g,则x=_________________。若将通N2改为通干燥的空气,测定的x值将_________(填“偏高”或“偏低”)。
(4)该小组利用镁铝水滑石分解后剩余的固体来提取纯净氧化铝(冶炼铝的原料)。
请补充该小组设计的实验操作步骤
【实验中可选用的试剂:盐酸、氢氧化钠溶液、氨水、二氧化碳气体、蒸馏水】
①取分解后固体于烧杯中,加入足量的_____________,玻璃棒搅拌充分反应,过滤。
②______________________________________________,过滤,洗涤。
③加热
(5)下列实验能比较镁和铝的金属性强弱的是______________。
a.测定镁和铝的导电性强弱
b.测定等物质的量浓度的Al2(SO4)3和MgSO4溶液的pH
c.分别向0.1mol·L-1AlCl3和0.1 mol·L-1MgCl2溶液中逐滴加过量NaOH溶液
d.测定等物质的量的镁和铝与足量盐酸反应生成的H2的多少








 粤公网安备 44130202000953号
粤公网安备 44130202000953号