Fe是人体不可缺少的微量元素,摄入含铁化合物可补充铁。硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定某补血剂中铁元素的含量。实验步骤如下: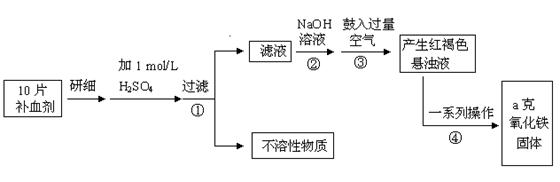
请回答下列问题:
(1)步骤②中加入足量NaOH发生的主要反应的离子方程式为 ,
步骤③中反应的化学方程式为 。
(2)步骤④中一系列处理的操作步骤: 、洗涤、 、冷却、称量。
(3)若实验中需用98%的浓硫酸(密度为1.84g/mL)配制1 mol/L的稀硫酸480 mL。配制时用到的玻璃仪器除量筒、烧杯、胶头滴管、玻璃棒外还有 ,需用量筒量取该浓硫酸 mL。
(4)若实验无损耗,则每片补血剂含铁元素的质量 g(用含a的代数式表示)。








 粤公网安备 44130202000953号
粤公网安备 44130202000953号