(本题共12分)CO的应用和治理是当今社会的热点问题。
29、CO能导致镍系催化剂中毒,工业上常用SO2除去原料气中少量CO,生成物为固体S和CO2。
写出该反应的化学方程式为 。
30、上述反应中,每减少2.24L气体(标准状况下),转移电子数为 。
CO工业上可用于高炉炼铁,发生如下反应: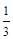 Fe2O3(s) + CO(g)
Fe2O3(s) + CO(g)
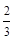 Fe(s) + CO2(g),
Fe(s) + CO2(g),
已知该反应在不同温度下的平衡常数如下表:
| 温度/℃ |
1000 |
1150 |
1300 |
| 平衡常数 |
4.0 |
3.7 |
3.5 |
31、下列说法不正确的是 (选填序号)
a.该反应是一个放热反应
b.该反应的平衡常数表达式是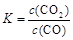
c.其他条件不变,向平衡体系充入CO2气体,K值减小
d.当K值等于1时,反应达到平衡
32、欲提高CO的平衡转化率,促进Fe2O3的转化,可采取的措施是 (选填序号)
a.及时吸收或移出CO2 b.增大反应体系的压强
c.用更高效的催化剂 d.粉碎矿石,增大接触面积
高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇:CO(g) + 2H2(g) CH3OH(g) + Q
CH3OH(g) + Q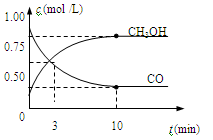
33、从上图可以看出,反应开始到平衡,反应速率v(H2) 。
。
34、甲醇氧化可生成甲酸,能使0.1mol/L的甲酸溶液的电离度与pH值都增大的是 (选填序号)。 a.加水稀释 b.加入少量甲酸钠固体
a.加水稀释 b.加入少量甲酸钠固体
c.通氯化氢 d.加入少量苛性钠固体








 粤公网安备 44130202000953号
粤公网安备 44130202000953号