可以利用氧化锌粗品(含有Fe2O3、FeO、CuO)为原料制备纯净的氧化锌,其化学工艺流程如下: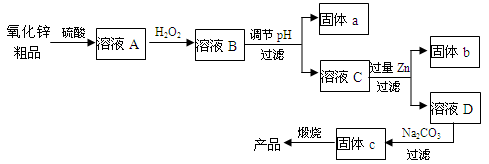
按要求回答下列问题:
(1)加双氧水主要作用是氧化溶液中的Fe2+,该反应的离子方程式为___________。
(2)调节pH主要是使溶液中的Fe3+生成沉淀而被除去,溶液pH对除Fe效率影响如图所示。则除Fe3+时应控制溶液的pH为 (填序号)。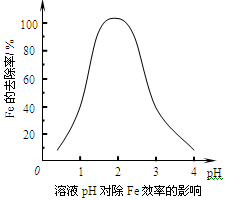
a.3.5~4.0 b.2.5~3.5
c.1.5~2.5 d.0.5~1.5
(3)固体b为_________(填化学式),固体c为碱式碳酸锌,锻烧固体c的化学方程式为__________。
(4)工业上也可以将氧化锌粗品采用碱溶的方法,将氧化锌转化为Na2[Zn(OH)4]溶液,然后电解该溶液制取锌,以石墨为电极电解时,阴极的电极反应式为___________,当生成1mol锌时,阳极上生成气体在标准状况下的体积为__________L。“纸质电池”的纸片内充入的是水和氧化锌组成的电解液,纸的一边镀锌另一边镀二氧化锰,电池总反应为Zn+2MnO2+H2O=ZnO+2MnO(OH),该电池的负极反应式为_________。








 粤公网安备 44130202000953号
粤公网安备 44130202000953号