某同学分析Zn与稀H2SO4的反应。
(1)该反应的离子方程式是 。
(2)制H2时,用稀硫酸而不用浓硫酸,原因是_________。
(3)已知:Zn(s)+1/2O2(g)=ZnO(s) △H=-332kJ/mol
ZnO(s) + H2SO4(aq) = ZnSO4(aq) + H2O(l) △H=-112kJ/mol
H2(g) +1/2 O2(g) = H2O(l) △H=-286kJ/mol
则Zn与稀H2SO4反应生成1mol H2时的反应热△H= kJ/mol。
(4)该同学用如下装置进行实验,分析影响反应速率的因素。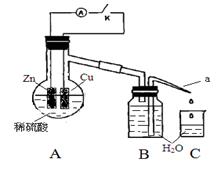
实验时,从断开K开始,每间隔1分钟,交替断开或闭合K,并连续计数每1 分钟内从a管流出的水滴数,得到的水滴数如下表所示:
| 1分钟水滴数(断开K) |
34 |
59 |
86 |
117 |
… |
102 |
| 1分钟水滴数(闭合K) |
58 |
81 |
112 |
139 |
… |
78 |
分析反应过程中的水滴数,请回答:
①由水滴数58>34、81>59,说明在反应初期,闭合K时比断开K时的反应速率______(填“快”或“慢”),主要原因是_________。
②由水滴数102>78,说明在反应后期,断开K时的反应速率快于闭合K时的反应速率,主要原因是_______。
③从能量转换形式不同的角度,分析水滴数86>81、117>112的主要原因是_______。








 粤公网安备 44130202000953号
粤公网安备 44130202000953号