把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间(单位:秒)的关系可用如图曲线来表示,回答下列问题: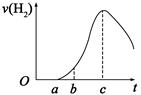
(1)曲线由O →a段不产生氢气的原因(请用有关反应的化学方程式表示)是 。
(2)曲线a→c段,产生氢气的速率增加较快,而曲线由c以后,产生氢气的速率逐渐下降,解释上述现象的原因是 。
(3)在b到c这段时间内,收集到氢气VL(标准状况),则这段时间内用硫酸表示的平均速率为 (假设反应前后溶液体积不变)。
(4)对于足量镁条和100ml 2mol/L硫酸生成氢气的反应,下列措施能减缓反应速率,但又不影响生成氢气的总量的是 。
① 加NaOH固体;
② 加适量BaCl2溶液;
③ 加KNO3溶液;
④ 加适量H2O;
⑤ 将镁条换成镁粉;
⑥ 加小苏打溶液;
⑦ 加少量CuSO4溶液;
⑧ 加适量Na2SO4溶液;
⑨ 将2 mol/L硫酸换成160mL 2.5mol/L的盐酸 ;
(5)若使用催化剂,会不会使氢气的产量增加? (填“会”或“不会”)。








 粤公网安备 44130202000953号
粤公网安备 44130202000953号