工业生产硝酸铵的流程图如下图。请回答:
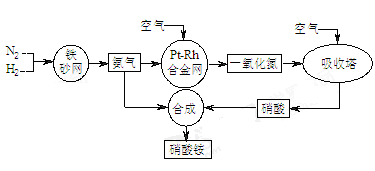
(1)已知 :N2(g)+3H2(g)  2NH3(g) ΔH=-92.4 kJ·mol-1。
2NH3(g) ΔH=-92.4 kJ·mol-1。
①在500℃、2.02×107Pa和铁催化条件下向一密闭容器中充入1molN2和3molH2,充分反应后,放出的热量_____(填“<”、“>”或“=”)92.4kJ,理由是 。
②为提高氨的产量,获得更大的效益,实际生产中宜采取的措施有 。
A 降低温度 B 最适合催化剂活性的适当高温 C 增大压强
D 降低压强 E 循环利用和不断补充氮气 F 及时移出氨
(2)已知铂铑合金网未预热也会发热。写出氨催化氧化的化学方程式: ,该反应的化学平衡常数表达式K= ,当温度升高时,K值 (填“增大”、“减小”或“不变”)。
(3)在一定温度和压强的密闭容器中,将平均相对分子质量为8.5的H2和N2混合,当该反应达到平衡时,测出平衡混合气的平均相对分子质量为10,请计算此时H2的转化率(写出计算过程)。








 粤公网安备 44130202000953号
粤公网安备 44130202000953号