为探究物质溶解过程中的能量变化,某同学设计图Ⅰ所示装置。在盛有水的烧杯中放入一装有饱和硝酸钾溶液的试管,向水中加入足量物质X,搅拌。结合图Ⅱ硝酸钾溶解度曲线,对硝酸钾溶液变化的推断,合理的是( )
①X为NaCl固体,试管中无晶体析出,硝酸钾溶液仍是饱和溶液
②X为NaOH固体,试管中无晶体析出,硝酸钾溶液仍是饱和溶液
③X为NH4NO3晶体,试管中有晶体析出,硝酸钾溶液仍是饱和溶液
④X为浓H2SO4,试管中无晶体析出,硝酸钾溶液为不饱和溶液
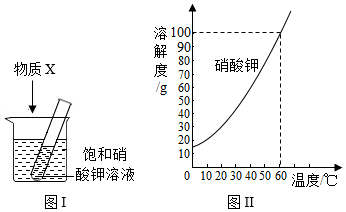
A.①②③B.①③④C.①②④D.②③④
如图为甲和乙两种固体物质的溶解度曲线。回答下列问题:
(1)当温度为 时,甲、乙两种物质的饱和溶液中溶质的质量分数相等。
(2)图中a点对应的甲溶液是 (填"饱和"或"不饱和")溶液。
(3)当温度为t 3℃时,要将质量分数为20%的甲溶液100g变成饱和溶液,需要加入 g甲固体(不含结晶水)。

如图是A、B、C三种物质的溶解度曲线,请认真分析并回答:
(1)t3℃时,A、B、C三种物质的溶解度由小到大的顺序为 。
(2)t2℃时,A、B、C三种物质的饱和溶液降温到t1℃时变为不饱和溶液的是 。
(3)当A中含有少量的B,可采用 (填“降温”或“蒸发”)结晶的方法提纯A物质。
(4)t3℃时,若用A、B两物质各50g配成饱和溶液,则所需加水的质量A B(填“>”,“<”,“=”号)

如图是A、B、C三种固体物质的溶解度曲线,请回答下列问题:
(1)P点表示的意义: 。
(2))t2℃时,A、B、C三种固体物质的溶解度大小顺序是: 。
(3)t2℃时,将60gA物质放入100g水中,充分溶解后,所得溶液是 (填“饱和溶液”或“不饱和溶液”),所得溶液的质量是 g。

甲、乙、丙三种物质在中形成的饱和溶液溶质的质量分数随温度变化如图所示,请回答下列问题:
(1)25℃时,甲物质的溶解度为 (答案保留一位小数)
(2)从乙溶液中获得乙晶体的方法是 (填“蒸发结晶”或“降温结晶”)
(3)将50℃甲的溶液降温至25℃,溶液为 (填“饱和溶液”或“不饱和溶液”)
(4)气体的溶解度随温度的变化规律与 (填“甲”、“乙”或“丙”)相似。

下列关于溶液的说法正确的是( )
A.水是最常用的溶剂
B.饱和溶液一定比不饱和溶液浓度大
C.澄清、透明的液体一定是溶液
D.饱和溶液一定不能再继续溶解溶质
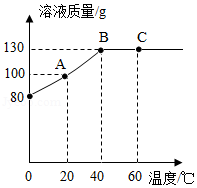
将80gM物质加入50g水中,充分溶解,测得溶液的质量随温度的变化曲线如图所示,按要求填空。
(1)A点时,该溶液的溶质质量分数为 。
(2)A、B、C三点所对应的溶液,属于不饱和溶液的是 (填字母)。
(3)在40℃时,M物质的溶解度为 g,若保持溶剂的质量不变,从C点对应的溶液获得M的晶体,可以采用的方法是 。
张老师在讲授溶液时,用固体M做了如下实验,图一中甲、乙、丙、丁是充分搅拌后静置的现象,请回答相关问题(忽略水的挥发):
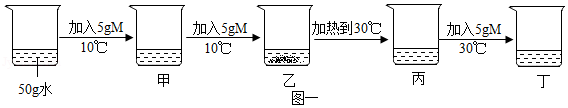
(1)上述烧杯中,溶液质量最大的是 (填序号)。
(2)上述实验可以判断物质M的溶解度曲线是图二对应的 (填序号)。
(3)甲、乙、丙烧杯中的溶液一定呈饱和状态的是 (填序号)。
(4)根据图二,若要使丁烧杯中的溶液恰好达到饱和状态,还需要加入 g的M固体。
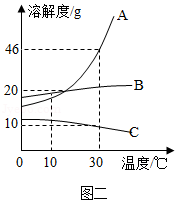
如图所示,在分别盛有100g水的烧杯中放入KNO3充分溶解,则说法正确的是( )
温度(℃) |
t1 |
t2 |
KNO3的溶解度(g/100g水) |
60 |
90 |
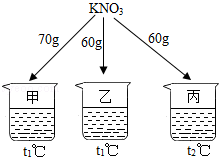
A.甲、乙混合后为t1℃的不饱和溶液
B.乙升温至t2℃,溶液质量增加
C.乙、丙溶液中溶质质量相等
D.丙降温至t1℃,有晶体析出
如图是对某固体物质的溶液在一定温度下,进行恒温蒸发操作的实验记录,请回答:

(1)乙中的溶液为 (填“饱和”或“不饱和”)溶液。
(2)该固体物质在当时温度下的溶解度为 。
(3)甲、乙、丙、丁中溶液溶质质量分数的大小关系是 。
(4)给丁中的溶液升高温度时,固体逐渐消失,说明该物质的溶解度随温度升高而 (填“增大”或“减小”)。
下表是KNO3在不同温度时的溶解度,回答问题。
温度/℃ |
30 |
40 |
50 |
60 |
70 |
80 |
90 |
溶解度/g |
45.8 |
63.9 |
85.5 |
110 |
138 |
169 |
202 |
(1)影响固体物质溶解度大小的因素有 (填一种)。
(2)30℃时KNO3溶液的溶质质量分数的最大值是 (只列出表达式)。
(3)90℃时,将一定质量的KNO3溶液按图示进行操作:

90℃时的KNO3溶液是 (填“饱和”或“不饱和”)溶液。图中n的数值为 。
如表是NaCl和KNO 3在不同温度时的溶解度,回答问题
| 温度/℃ |
10 |
20 |
30 |
40 |
50 |
60 |
|
| 溶解度/g |
NaCl |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
| KNO 3 |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
110.0 |
|
(1)两种物质中,溶解度受温度影响变化较大的是 。
(2)60℃时,按图示操作:

A中溶液是 (填"饱和"或"不饱和")溶液,C中溶液的总质量是 g。
(3)50℃时,将两种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到50℃,剩余溶液的质量:NaCl溶液 (填"大于""等于"或"小于")KNO 3溶液。
根据下表回答问题:
温度/℃ |
10 |
20 |
30 |
40 |
50 |
60 |
|
溶解度 /g |
NaCl |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
4Cl |
33.5 |
37.2 |
41.4 |
45.8 |
50.4 |
55.2 |
|
(1)海水中含有大量的氯化钠,海水晒盐的原理是 ,氨碱法制纯碱先向饱和食盐水中通入氨气,通入氨气的作用是 3溶液中加入 以回收氨,使之循环使用。
(2)氯化钠和氯化铵具有相同溶解度的温度范围在 ℃之间。
4Cl溶液,经过如下操作后,得到固体。
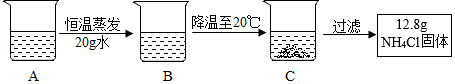
I.C中溶液的质量是 4Cl的 (选填“饱和”或“不饱和”)溶液,该溶液中溶质的质量分数为 (结果精确到0.1%)。
II.对以上过程的分析,正确的是 (选填编号)。
①A到B的过程中,溶质质量没有改变
②B中溶质与溶剂的质量比为55.2:100
4Cl固体的温度在40℃至50℃之间。
20℃时,将等质量的甲、乙两种固体分别加入盛有100g水的烧杯中,充分搅拌后现象如图1所示,甲、乙两物质的溶解度曲线如图2所示。请回答下列问题:

(1)图l中一定为饱和溶液的是 溶液(填“甲”或“乙”)
(2)图2中P点表示的意义 。
(3)图2中表示乙物质溶解度曲线的是 (填“M”或“N”)
控制变量法是科学探究中常用的方法之一。
(1)在探究固体物质的溶解度时,需要考虑的因素有:①溶质的种类;②溶剂的种类;③溶质最多被溶解的质量;④溶剂的质量;⑤温度。
如测定“某物质在不同温度下的溶解度”,研究的是 (填序号)受温度的影响,这就需要控制其他因素保持不变。
(2)右表是利用控制变量法测得的氯化钠、硝酸钾在不同温度时的溶解度,请根据表格内容及实验现象回答下列问题。
温度(℃) |
20 |
40 |
50 |
|
溶解度/g |
NaCl |
36.0 |
36.6 |
37.0 |
KNO3 |
31.6 |
63.9 |
85.5 |
|
①从上表可知,两种物质的溶解度受温度变化影响较大的是 ;
②20℃时,将等质量的NaCl、KNO3分别放入盛有100g水的两个烧杯中,充分溶解后如图1所示,升温到50℃时如图2所示。试判断:50℃时甲烧杯中的溶液一定是 (填“饱和溶液”、“不饱和溶液”或“不能确定”)。

试题篮
()