如图所示,是小科建构的铜及其化合物之间相互转化的关系图。
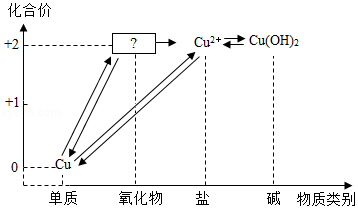
(1)写出图中“?”处物质的化学式 。
(2)要一步实现图中“Cu→Cu2+”的转化,可将铜加入适量的某种盐溶液中,则该溶液的溶质是 。
(3)根据图中的转化关系,利用硝酸铜溶液制备纯净的硫酸铜晶体。请设计一个实验方案,要求写出主要操
作步骤及所需要的试剂 。
铁的化合物有广泛用途,如碳酸亚铁(FeCO3)可作补血剂。某硫酸厂产生的炉渣中除了有Fe2O3、FeO,还有一定量的SiO2.兴趣小组利用炉渣尝试制备FeCO3,其流程如图: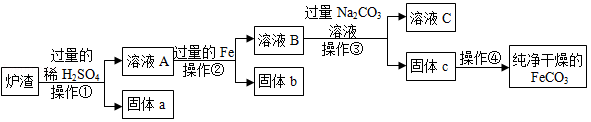
【已知:Fe+Fe2(SO4)3═3FeSO4;SiO2不溶于水,也不与稀硫酸反应】
(1)操作①的名称是 。
(2)溶液A中的溶质除H2SO4外,还存在 。
(3)上述流程中生成固体c的化学方程式 。
一水硫酸四氨合铜的化学式为[Cu(NH3)4]SO4•H2O,是一种高效、安全的杀菌剂。它在乙醇﹣﹣水混合溶剂中的溶解度随乙醇体积分数的变化曲线如图甲所示。小明在实验室以氧化铜为主要原料合成该物质,他设计的合成路线如图乙所示:

(1)溶液A中一定存在的溶质为 。
(2)溶液B中含硫酸四氨合铜,“一系列操作”是指向溶液B中加入适量 、过滤、洗涤、干燥等。
如图所示转化关系中的反应均为初中化学常见的反应。下列选项中甲、乙、丙、丁四种物质间能通过一步反应实现图示转化关系的是( )
| 选项 |
甲 |
乙 |
丙 |
丁 |
| A |
CuO |
CuSO 4 |
FeSO 4 |
FeCl 2 |
| B |
CO 2 |
Na 2CO 3 |
H 2O |
O 2 |
| C |
O 2 |
MgO |
H 2O 2 |
H 2O |
| D |
HCl |
BaCl 2 |
BaSO 4 |
H 2SO 4 |

| A. |
A |
B. |
B |
C. |
C |
D. |
D |
在抗击"新冠肺炎病毒"期间,消毒剂在公共场所进行卫生防疫时发挥着重要作用。二氧化氯(ClO 2)是一种高效、广谱、安全的杀菌消毒剂。以粗盐水(含可溶性杂质MgSO 4、CaCl 2)为原料,制取ClO 2的工艺流程如图:

(1)试剂A为 。
(2)加入过量Na 2CO 3溶液的作用是 。
(3)步骤④中发生反应的化学方程式为 。
(4)步骤⑤涉及的物质中含氯元素化合价最高的物质是 。
(5)如图流程中可循环利用的物质有 。
孔雀石的主要成分是CuCO3•Cu(OH)2及少量不溶性杂质(杂质不与酸反应),某同学按下列实验步骤制取了少量氧化铜。

(1)白色沉淀的化学式为 。
(2)写出步骤③中发生反应的化学方程式 ; 。
(3)蓝色沉淀受热分解生成另一种氧化物的化学式是 。
(4)若向溶液A中逐滴加入NaOH溶液,其过程中溶质种数会发生变化,最多时可达 种。
从某废旧电子产品中可以提炼贵重金属,并得到硫酸铜溶液。其工艺流程如图所示:
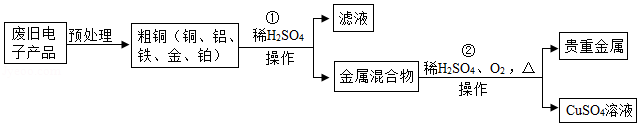
(1)图中“操作”的名称是 。
(2)写出所得贵重金属中任意一种成分的化学式 。
(3)写出①中发生的化学反应方程式 (任写一种);该反应的基本类型为 。
(4)写出②中发生的化学反应方程式 。
镁及其合金是一种用途很广泛的金属材料。大量的镁是从海水蒸发结晶得到粗盐后的苦卤水中提取的。根据下列工业制镁的主要生产步骤回答问题:
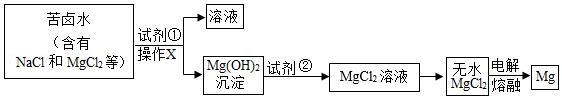
(1)操作X的名称是 ;
(2)试剂②可选用 ;
(3)MgCl2在熔融状态下,通电后会产生金属镁和氯气(Cl2),该反应的化学方程式为 。
工业上利用氟碳铈矿(主要成分为CeFCO3)提取CeCl3的一种工艺流程如图:

(1)流程中Ce(BF4)3转化成KBF4的基本反应类型是 。
(2)在足量氧气中高温焙烧CeFCO3,化学方程式为 。
(3)流程涉及的化合物中,铈元素的化合价为 价。
(4)酸浸过程中,CeO2与盐酸反应有刺激性气味的气体单质生成,且化学方程式中CeO2与盐酸的化学计量数之比为1:4,则化学方程式为 。
2019年诺贝尔化学奖授予对锂离子电池研究作出贡献的三位科学家。如图是从钴酸锂废极片[主要成分为钴酸锂(LiCoO2)]中回收得到Co2O3和Li2CO3的一种工艺流程。
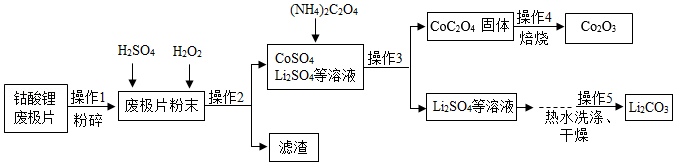
(1)操作1中,粉碎废极片的目的是 ;
(2)实验室中完成操作2时,需用到的玻璃仪器是 (填一种即可);
(3)操作4中,在高温条件下,CoC2O4在空气中反应生成Co2O3和二氧化碳,化学方程式为 ;
(4)操作5中,Li2CO3晶体用热水洗涤比用冷水洗涤损耗更少,说明Li2CO3的溶解度随温度升高而 。
以FeSO4•7H2O为原料制备铁红(Fe2O3)的一种方法如图:

已知“沉淀”时的主要反应为:2FeSO4+H2O2+2H2O═2FeO(OH)↓+2H2SO4
(1)FeO(OH)中铁元素的化合价为 。FeO(OH)可表示为mFe2O3•nFe(OH)3, 。
(2)“沉淀”时需控制溶液的pH与反应的温度。
①“沉淀”时调节溶液的初始pH约为4,过程中应始终保持溶液的pH为3.0~4.5,需不断加入物质Z调节溶液的pH,Z应具备的性质有 (填字母)。
A.能与酸反应
B.能与碱反应
C.不与FeO(OH)反应
②“沉淀”时反应温度不宜过高,其原因是 。
(3)“过滤”后需对固体进行洗涤与干燥。洗涤时被除去的沾于固体表面的阴离子为 (填离子符号)。
(4)“煅烧”时反应的化学方程式为 。
(5)如图为其他条件相同时不同煅烧温度对产品中Fe2O3质量分数的影响。煅烧温度较低时,产品中Fe2O3质量分数较低,其原因是 。当煅烧温度达800℃时,继续升高温度,产品中Fe2O3质量分数降低,且铁元素质量分数升高,所得产品发黑,其可能原因是 。

(6)用该方法制备Fe2O3,计算理论上13.9t FeSO4•7H2O(相对分子质量为278)可制得Fe2O3的质量(写出计算过程)。
已知:NaOH溶液能与MgSO4溶液反应生成Na2SO4和难溶于水的Mg(OH)2.镁大多是从海水中提取。某小组从预先处理后的海水中提取镁的主要步骤如图:

(1)沉淀时,NaOH应过量的目的是 。
(2)过滤时,使用玻璃棒的作用是 。
(3)溶解时,稀盐酸与Mg(OH)2发生反应的化学方程式为 ,该反应的反应类型为 。
A、B、C三种物质之间的一步转化关系如图所示(部分反应物、生成物未标出)。其中,A是石灰石或大理石的主要成分;B是金属氧化物,可作干燥剂;C是碱。下列说法错误的是( )

A.大理石和物质C均可作建筑材料
B.物质B有吸水性,易跟水起化合反应
C.物质A可用来配制农药波尔多液和改良酸性土壤
D.C溶液较长时间放在空气中表面会有一层白膜(若水没有减少),则溶液的溶质质量分数变小
四氧化三铁是一种常用的磁性材料,由工业废料铁泥(含Fe、Fe2O3、FeO和杂质,杂质不参与反应)制取Fe3O4的一种流程如图:
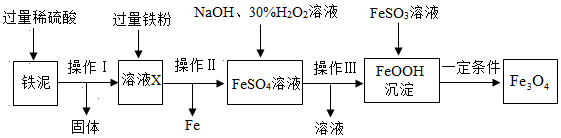
(1)操作Ⅱ的名称是 。
(2)Fe2O3与稀硫酸反应的化学方程式为 ,为使铁泥与稀硫酸充分反应,可采取的措施是 (答出一点即可)。
(3)向溶液X中加入过量铁粉的作用是 。
(4)FeOOH与FeSO3溶液在一定条件下反应生成Fe3O4和 (填化学式)。
试题篮
()