某工厂生产硼砂产生的固体废料,主要含有MgCO3、CaCO3、SiO2、Al2O3和Fe2O3等,其中MgCO3质量分数为63%.回收镁的工艺流程如图
(1)“酸浸”时MgCO3发生反应的化学方程式为 。
(2)“调pH”前滤液Ⅰ的pH 7(填“>”或“<”)。
(3)滤液Ⅲ中可回收的主要物质 (填化学式)。
(4)已知固体废料质量为m,理论上可生产Mg(OH)2的质量为 。
(5)某BaCO3中混有SiO2杂质,简述提纯该BaCO3的实验操作: 。
中国科学院张青莲院士对铟、铱、锗等的相对原子质量测定作出了杰出贡献。锗是重要的半导体材料,由锗精矿(含GeO2、GeS2、As2O3等)制备金属锗的步骤如下:
①焙烧,GeS2转化为GeO2,然后用盐酸溶解得到GeCl4.②用Cl2将杂质转化为不易挥发的H3AsO4.③加热混合溶液使GeCl4气化,再冷凝为液态,经过一系列转化得到GeO2.④用H2将GeO2还原为Ge,同时H2转化为H2O。
(1)步骤①盐酸溶解GeO2的化学方程式为 。
(2)完成步骤②除杂反应的化学方程式:AsCl3+4H2O+Cl2═H3AsO4+5 。
(3)步骤③分离GeCl4的方法是 (填标号)。
A.过滤
B.蒸馏
C.升华
D.蒸发
(4)步骤④消耗H2和生成Ge的质量之比为 。
如图,给出了三种物质可能存在的转化关系,根据所学的物质性质及化学变化规律,判断下列选项正确的是( )
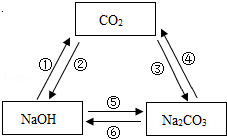
A.不能一步实现转化的有①②
B.实现③转化,可通至氯化钠溶液
C.实现⑤转化,可加入碳酸钙粉末
D.实现⑥转化,可加入氢氧化钾溶液
从盐湖中提取的某种矿物主要含有KCl,还有少量MgSO4、CaCl2及不溶性杂质SiO2.从该矿物中提取KCl的流程如图:
回答下列问题:
(1)滤渣I的主要成分是 。
(2)Y溶液中溶质的化学式为 。
(3)向滤液Ⅱ中加入过量盐酸的目的是 。
(4)蒸发溶液得到KCl固体的过程中,要用玻璃棒不断搅拌,目的是 。
为了从含有FeSO4、CuSO4的工业废水中回收Cu和硫酸亚铁晶体,某学习小组设计并完成了以下实验。
下列说法正确的是( )
A.固体X中只含有Cu
B.试剂B是稀硫酸
C.溶液Z中的溶质为FeSO4和CuSO4
D.操作Ⅰ用到的玻璃仪器只有烧杯和玻璃棒
内江拥有中国西南地区最大的再生资源基地,可回收处理大量废旧塑料电器及玻璃等,某品牌电器的废旧电路板中含有Fe、Cu、Ag、Ni(镍,银白色金属) 等金属,如下图是某车间回收部分金属的工艺流程。已知,2Cu+O2+2H2SO4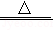 2CuSO4+2H2O。
2CuSO4+2H2O。
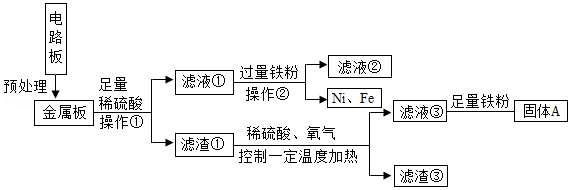
回答下列问题。
(1)操作①中,使用的玻璃仪器除烧杯、玻璃棒外,还需 ;
(2)滤渣③中含有的金属是 ;
(3)根据以上工艺流程图,可以得出Ni、Fe的金属活动性强弱顺序是Ni Fe(填“>”或“<”)。
(4)滤液③中加入足量铁粉的主要目的是 ,固体A除主要含有铜外,还含有一定量的铁,为了进一步提纯铜,可以向固体A中加入适量的稀硫酸,发生反应的化学方程式为 ;
(5)相比于直接焚烧废旧电路板回收金属,该工艺流程的主要优点是 。
氯化钙(CaCl2)可用作干燥剂、混凝土防冻剂等。实验室用工业大理石(含有少量Al2O3、Fe2O3、SiO2等杂质)制备氯化钙的主要流程如下:
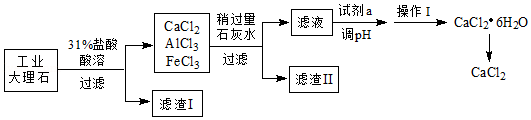
请回答下列问题:
(1)配制31%的稀盐酸730g,需要36.5%的浓盐酸 g。
(2)酸溶时碳酸钙参与反应的化学方程式为 。
(3)滤渣I的成分为 ,滤渣II中含有Al(OH)3和 。
(4)过滤使用到的玻璃仪器有 。操作I采用的方法是:蒸发浓缩、 、 、过滤。
(5)加入试剂a的目的是中和稍过量的石灰水,该反应的化学方程式为 。
某矿石主要成分是MgO,含少量的Fe2O3、CuO和SiO2杂质。用该矿石制备Mg(OH)2的工艺流程简图如图:
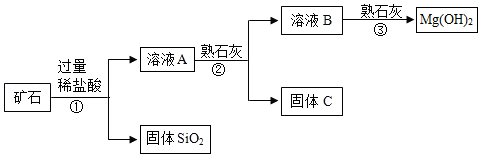
回答下列问题:
(1)步骤①和步骤②均用到的操作是 。
(2)溶液A中所含的阳离子有Fe3+、Cu2+、Mg2+和 (填离子符号)。
(3)已知部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表:
对应离子 |
Fe3+ |
Cu2+ |
Mg2+ |
开始沉淀时的pH |
1.9 |
4.2 |
9.1 |
完全沉淀时的pH |
3.2 |
6.7 |
11.1 |
步骤②加入熟石灰,调节溶液的pH范围为 ,固体C中所含成分的化学式为 。
(4)步骤③制得Mg(OH)2的化学方程式为 。
下列物质之间的转化,只通过一步反应不能实现的是( )
A.Fe2O3→FeCl2B.KMnO4→MnO2
C.CO2→COD.CuSO4→Cu(OH)2
辉铜矿的主要成分为硫化亚铜(Cu2S),工业上用辉铜矿冶铜的一种工艺流程图如下:
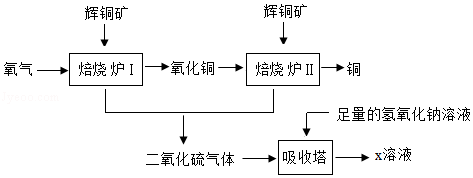
请你回答下列有关问题:
(1)硫化亚铜中铜元素的化合价为 。
(2)焙烧炉Ⅱ中发生反应的化学方程式为 。
(3)二氧化硫与二氧化碳具有相似的化学性质,则x溶液中盐的化学式是 。
如图是实验室模拟工业上用大理石(含少量Fe 2O 3和SiO 2)为原料提纯碳酸钙的实验流程,请回答下列问题:
已知:①SiO 2不溶于水也不溶于酸
②氨水呈碱性,与盐酸反应的化学方程式为:NH 3•H 2O+HCl=NH 4Cl+H 2O
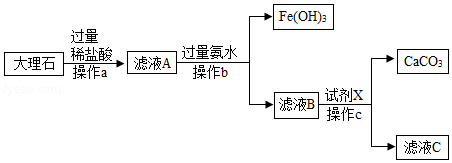
(1)稀盐酸不能用稀硫酸代替,原因是 。
(2)操作a中需要用到的玻璃仪器有烧杯、玻璃棒和 。
(3)写出滤液A中加氨水生成Fe(OH) 3的化学方程式 。
(4)滤液B中加入试剂X,恰好完全反应,若滤液C中只含有两种溶质,则试剂X的化学式为 。
某金属冶炼厂的管道烟泥中含有少量铜、锌、硫等单质。现欲回收铜和锌,并对硫进行环保处理,主要步骤如图所示:

已知:加热的条件下,Zn、Cu都可以与氧气反应生成相应的金属氧化物。
(1)烟泥最初处理需要除油污,用洗涤剂除油污的过程中发生了 现象。步骤①产生的废气B中,一定含有的有害气体是 (填化学式)。环保处理最好釆用的试剂是 (填字母序号)。
A、浓硫酸 B、食盐水 C、石灰乳
(2)写出步骤④中得到铜的化学方程式 ,它属于基本反应类型中的 反应。
(3)步骤③和④中主要操作的名称是 。
(4)我国古代就制得了一种外观似金子的锌和铜的合金,也就是黄铜,它的硬度比纯铜 (填“高”或者“低”)。
(5)取少量的溶液C,往其中加入一定质量的镁粉,充分反应后过滤,得到滤渣和滤液。往滤渣中加入稀盐酸有气泡产生,则滤液中一定没有 (填字母序号)。
A、硫酸镁 B、硫酸锌 C、硫酸铜 D、硫酸铜和硫酸锌
稀土元素被誉为“工业的维生素”,是不可再生资源,应用广泛。
①稀土元素与铝、钛等金属熔合,形成特种合金,其性能会有较大提高,强度更好,抗腐蚀性能更强。坦克、飞机、核潜艇等的制造都用到了特种合金。
②稀土元素在自然界中以化合物的形式存在。二氧化铈(CeO2)是稀土氧化物中用途极广的一种材料,因为具有较为独特的萤石晶体结构,使得其具有特殊的性能。主要用于玻璃、原子能、电子管等工业。
③中国的稀土储量最多时占世界的71.1%,目前占比在23%以下。中国并非世界上唯一拥有稀土的国家,却在过去几十年承担了世界稀土供应的角色,结果付出了破坏自身天然环境与消耗自身资源的代价。近几年,我国出台了一系列政策,采取了出口控制等措施,保护我国现有的稀土资源。
阅读以上材料,回答以下问题:
(Ⅰ)稀土元素铼与“太空金属”钛制成的钛铼合金,可用来制造核潜艇。请写出钛铼合金的优良性能(任写一点) 。
(Ⅱ)关于稀土资源,下列说法正确的是 (填序号)
A.稀土的开采与环境问题无关
B.稀土在材料工业方面发挥着重要作用,它是万能的
C.稀土元素化学性质稳定,在自然界中以单质形式存在
D.稀土不可再生,珍贵,保护稀土资源,是我们义不容辞的责任
(Ⅲ)某品牌平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2等物质)。以此粉末为原料进行资源回收,其工艺流程如图:
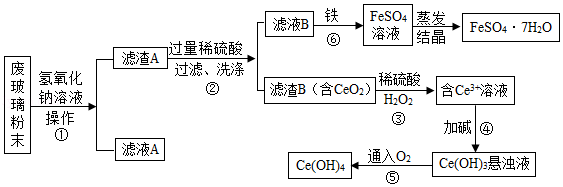
已知:2NaOH+SiO2=Na2SiO3+H2O,Na2SiO3溶于水。
(1)第①步操作的名称是 ;
(2)第②步加入过量稀硫酸的目的是 ;
(3)洗涤滤渣B的目的是为了除去 (填离子符号),提高产品的纯度;
(4)若第④步加的碱为NaOH,写出该反应的化学方程式 。
某班同学在实验室完成实验探究后得到废液A,其中含有稀硫酸、硫酸亚铁和硫酸铜。老师将同学们分成甲乙两组,继续进行如下实验,请完成下列相关问题:
[甲组任务]将废液转化成硫酸亚铁晶体。实验流程如图
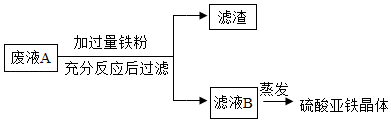
(1)滤液B中的溶质来自于哪几个部分?
(2)写出上述流程中的一个化学反应方程式: 。
[乙组任务]利用废液来探究金属铝的化学性质。实验流程如图: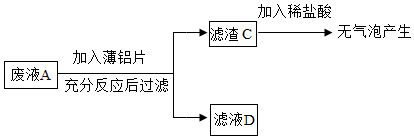
(3)滤渣C中一定没有 。
(4)滤液D中一定含有的溶质是 (填化学式,下同),可能含有的溶质是 。
试题篮
()