某兴趣小组同学利用氧化还原反应:
2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如下原电池,盐桥中装有饱和溶液.下列说法正确的是
| A.a电极上发生的反应为:MnO4-+8H++5e-═Mn2++4H2O |
| B.外电路电子的流向是从a到b |
| C.电池工作时,盐桥中的SO42-移向甲烧杯 |
| D.b电极上发生还原反应 |
如图所示,电流表G发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液。则A、B、C为
A. A是Zn,B是Cu,C是稀H2SO4
B. A是Cu,B是Zn,C是稀H2SO4
C. A是Fe,B是Ag,C是稀AgNO3溶液
D. A是Ag,B是Fe,C 是稀 AgNO3溶液
下列化学反应在理论上可设计成原电池是
| A.2Al(s) + 2NaOH(aq) +2H2O(l) ="=" 2NaAlO2(aq) + 3H2(g) △H<0 |
| B.HNO3(aq) + KOH(aq) ="=" KNO3(aq) + H2O(l) △H<0 |
| C.Ba(OH)2·8H2O(s) + 2NH4Cl(s) ="=" BaCl2(aq)+ 2NH3·H2O(aq)+ 8H2O(l) △H﹥0 |
| D.Na2O(s)+ H2O(l) ="=" 2NaOH(aq) △H<0 |
随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要原因是( )
| A.利用电池外壳的金属材料 |
| B.防止电池中汞、镉和铅等重金属离子对土壤和水源的污染 |
| C.防止电池中渗漏的电解质溶液腐蚀其他物品 |
| D.回收其中的石墨电极 |
如图所示的装置中,M为活动性顺序位于氢之前的金属,N为石墨棒,关于此装置的下列叙述中,不正确的是( )

| A.N上有气体放出 |
| B.M为负极,N为正极 |
| C.是化学能转变为电能的装置 |
| D.导线中有电流通过,电流方向是由M到N |
将纯锌片和纯铜片按图示插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )

| A.两烧杯中铜片表面均无气泡产生 |
| B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的pH均增大 |
| D.产生气泡的速率甲比乙慢 |
某实验小组依据反应 设计如图1原电池,探究pH对AsO4 氧化性的影响。测得电压与pH的关系如图2。下列有关叙述不正确的是( )
设计如图1原电池,探究pH对AsO4 氧化性的影响。测得电压与pH的关系如图2。下列有关叙述不正确的是( )
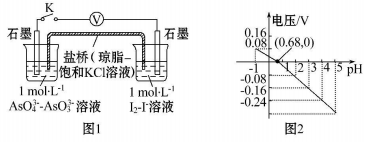
| A.调节pH可以改变反应的方向 |
| B.pH=0.68时,反应处于平衡状态 |
| C.pH=5时, 负极电极反应式为2I--2e -= I2 |
| D.pH>0.68时,氧化性I2>AsO43- |
下图所示的装置中,若通入直流电5 min时,铜电极质量增加2.16 g,试回答:
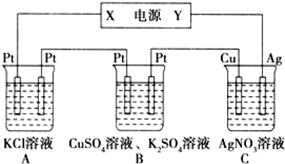
(1)电源电极X的名称为 。
(2)pH变化:A ,B ,C 。(填“增大”“减小”或“不变”)
(3)通电5 min后,B中共收集224 mL气体(标准状况),溶液体积为200 mL,则通电前CuSO4溶液的质的量浓度为 (设电解前后溶液体积无变化)。
(4)若A中KCl溶液的体积也是200 mL,电解后,溶液中OH-的物质的量浓度为 (设电解前后溶液体积无变化)。
依据原电池原理,回答下列问题:
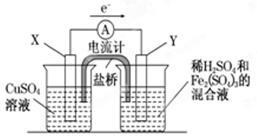
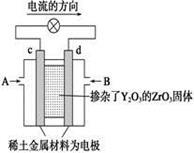
图(1) 图(2)
(1)图(1)是依据氧化还原反应:Cu(s)+2Fe3+(aq)=Cu2+(aq)+2Fe2+(aq)设计的原电池装置。
①电极X的材料为是 ;电极Y的材料为是 。
②Y电极发生的电极反应式为: 。
(2)图(2)是使用固体电解质的燃料电池,装置中,以稀土金属材料作惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导阳极生成的O2-离子(O2+4e―→2O2-)。
① c电极的名称为 ②d电极上的电极反应式为 。
下图两个装置中,液体体积均为200mL,开始工作前电解质溶液的浓度均为0.5 mol·L -1,工作一段时间后,测得有0.02 mol电子通过,若忽略溶液体积的变化,下列叙述正确的是
| A.产生气体体积 ①=② |
| B.①中阴极质量增加,②中正极质量减小 |
| C.电极反应式:①中阳极:4OH- - 4e- = 2H2O+O2 ↑ ②中负极:2H + +2e-=H2 ↑ |
| D.溶液的pH变化:①减小,②增大 |
钢铁在潮湿的空气中会被腐蚀,发生的原电池反应:2Fe+2H2O+O2 =2Fe2++4OH-。以下说法正确的是
| A.负极发生的反应为:Fe-2e-=Fe2+ |
| B.正极发生的反应为:2H2O+O2+2e-=4OH- |
| C.原电池是将电能转变为化学能的装置 |
| D.钢柱在水下部分比在空气与水交界处更容易腐蚀 |
某合作学习小组的同学利用下列氧化还原反应设计 原电池:2KMnO4 + 10FeSO4 + 8H2SO4=2MnSO4 + 5Fe2(SO4)3+K2SO4+8H2O,盐桥中装有饱和K2SO4溶液。下列叙述中正确的是
| A.乙烧杯中发生还原反应 |
| B.甲烧杯中溶液的pH逐渐减小 |
| C.电池工作时,盐桥中的SO42-移向甲烧杯 |
| D.外电路的电流方向是从a到b |
Ⅰ.A、B、C、D、E、F、G均为短周期元素,原子序数依次递增。A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的元素.请用化学用语回答:
(1)推断B元素在元素周期表中的位置_______________________。
(2)A与D形成的18电子的化合物与FD2化合生成一种强酸,其化学方程式为_____________。
(3)用电子式表示化合物E2F的形成过程_______________________。
(4)下图为某新型发电装置示意图,其负极电极反应为_______________________。

(5)在101kPa、25℃下,16g液态C2A4在D2中完全燃烧生成气体C2,放出312kJ热量,则C2A4和D2反应的热化学方程式为_______________________。
Ⅱ.A、B、C、X均为常见的纯净物,它们之间有如下转化关系(副产品已略去)。
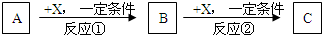
试回答:
(1)若X是强氧化性单质,则A不可能是___________。
a.S b.N2 c.Na d.Mg e.Al
(2)若X是金属单质,向C的水溶液中滴入AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则B的 化 学式为___________。
(3)若A、B、C为含某金属元素的无机化合物,X为强电解质,A溶液与C溶液反应生成B,则B的化学式为___________。
试题篮
()