已知:
①不对称烯烃与不对称加成物在不同的条件下有不同的加成方式,如: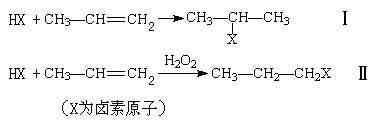
②烃基上的卤素原子在一定条件下能发生取代反应,如: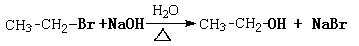
也能发生消去反应,如: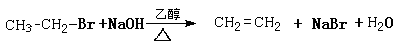
对溴苯乙烯(Br CH=CH2)与丙烯的共聚物是一种高分子阻燃剂,具有低毒、热稳定性好等优点。
CH=CH2)与丙烯的共聚物是一种高分子阻燃剂,具有低毒、热稳定性好等优点。
完成下列填空:
(1)写出该共聚物的结构简式
(2)实验室由乙苯制取对溴苯乙烯,需先经两步反应制得中间体Br CHBrCH3。
CHBrCH3。
写出该两步反应所需的试剂及条件。
(3)将Br CHBrCH3与足量氢氧化钠溶液共热得到A,得到A时,苯环上没有化学键的断裂和生成。
CHBrCH3与足量氢氧化钠溶液共热得到A,得到A时,苯环上没有化学键的断裂和生成。
写出生成A的化学方程式 。
由上述反应可推知 。
由A生成对溴苯乙烯的反应方程式为 。
(4)丙烯催化二聚得到2,3-二甲基-1-丁烯,B与2,3-二甲基-1-丁烯互为同分异构体,且所有碳原子处于同一平面。写出B的结构简式。 ,1molB完全燃烧时耗氧___________mol
完成下列获得B的化学方程式(条件错误不得分):
①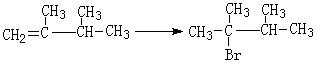
________________________________________________
②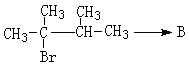
_________________________________________________
在如图所示的一些常见单质,化合物等物质之间的转化关系中(有些反应过程中的水,部分产物和反应条件未全部列出),已知反应①是氯碱工业的最基础的反应,A、B、F、H、J的焰色反应均为黄色,热的F溶液可以去除物品表面的油污,I为地壳中含量最多的金属元素的单质,L是典型的两性氧化物,在常温常压下C、D、G均为气体,D呈黄绿色,G是形成温室效应的主要气体.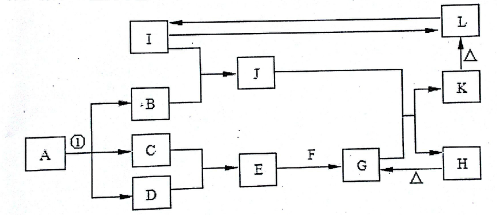
(1)反应①进行的条件为 .
(2)化合物F的化学式为 .
(3)I与氧化铁反应的化学方程式为 .
(4)J的水溶液与G反应生成K和H的离子方程式为 .
已知A、B、C、D四种强电解质溶液,分别含有下列阴阳离子中的各一种,且互不重复:Ba2+、H+、Na+、NH4+、CO32﹣、NO3﹣、SO42﹣、OH﹣.已知:①A和B反应生成的气体能被D吸收,而A和D反应生成的气体能被B吸收;②向A或D中滴入C,均有白色沉淀产生.另有晶体E的摩尔质量为474g/mol,可用于自来水的净水剂.试判断:
(1)晶体E的名称为 ,用离子方程式和必要的文字说明E可用作净水剂的原理 .
(2)写出A、B、C的化学式:A ,B ,C .
(3)写出A与D反应的离子方程式 .
(4)将200mL0.5mol/L的B溶液加入到150mL0.2mol/L的E溶液中,最终生成的白色沉淀质量为 g.
下列框图所示的转化关系中,甲为生活中常见的金属单质,乙、丙、丁为气体单质,D为家庭中常用物质(部分反应物和生成物及溶剂水已略去).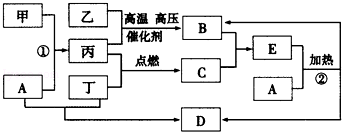
请回答:
(1)E的化学式为 ;甲的原子结构示意图为 ;
(2)反应①的离子方程式为 ;反应②的化学方程式为 ;
(3)实验室制取并收集B的操作中,用 法收集B,验证B已收集满的方法是 (限答一种).
(4)实验室制备丁的方程式为 ,工业上输送丁的管道出现气体泄漏,如何查漏(用方程式表示) .
甲、乙、丙、丁四种物质转化关系如图.已知甲是一种导致钢铁生锈及许多还原性物质变质的单质,化合物乙、丙、丁均含有第三周期一种相同元素R.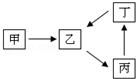
(1)钢铁因甲而生锈时的正极反应式为 .
(2)若乙是难溶于水的酸性氧化物.则
①R的原子结构示意图 .
②乙的一种重要用途是 .
(3)若丙是离子化合物,且阴离子含金属元素R.
①工业上由乙制取R的单质伴随的能量主要转化形式是: 能转化为 能.
②R的单质与MnO2反应的化学方程式为 .
③染料工业排放的废水中含有大量有毒的NO2¯,可以在碱性条件下加入R的单质除去(加热处理后的废水,会产生能使湿润的红色石蕊试纸变蓝的气体).除去NO2¯(有丙的阴离子生成)的离子方程式为 .
有机化合物A~H的转换关系如下所示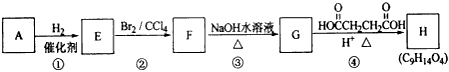
请回答下列问题
(1)链烃A有支链且只有一个官能团,其相对分子质量在65~75之间,1molA完全燃烧消耗7mol氧气,则A的结构简式是__________________,名称是__________________;
(2)在特定催化剂作用下,A与等物质的量的H2反应生成E。由E转化为F的化学方程式是_______________________________;
(3)G与金属钠反应能放出气体,由F转化为G的化学方程式是__________________;
(4)①的反应类型是__________________;③的反应类型是__________________;
(5)链烃B是E的同分异构体,存在着顺反异构,其催化氢化产物为直链烷烃,写出B的结构简式_______________;
(6)C是A的一种同分异构体,它的一氯代物只有一种(不考虑立体异构,则C的结构简式__________________。
电化学在化学工业有着广泛的应用,
(1)工业冶炼铝的化学方程式是 ;
(2)工业级氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换法膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。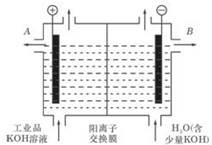
①该电解槽的阳极反应式是 ;
②除去杂质后的氢氧化钾溶液从液体出口 (填写“A”或“B”)导出。
(3)爱迪生蓄电池的反应式为:Fe+NiO2+2H2O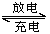 Fe(OH)2+Ni(OH)2;高铁酸酸钠(Na2FeO4)
Fe(OH)2+Ni(OH)2;高铁酸酸钠(Na2FeO4)
是一种新型净水剂.用下面装置可以制取少量高铁酸钠。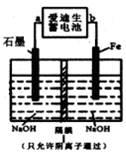
①此装置中爱迪生蓄电池的负极是________(填“a”或“b”),该电池工作一段时间后必须充电,充电时生成NiO2的反应类型是 。
②写出在用电解法制取高铁酸钠时,阳极的电极反应式 。
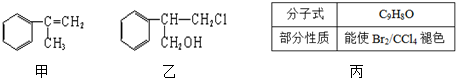
(1)乙中含有的官能团的名称为__________。
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):
其中反应Ⅰ的反应类型是__________,反应Ⅱ的条件是__________。
(3)由甲出发合成丙的路线之一如下: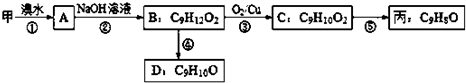
①下列物质不能与B反应的是(选填序号)__________
a.金属钠 b.FeCl3 c.碳酸钠溶液 d.HBr
②丙的结构简式为__________,
③写出反应③的化学方程式为__________。
④写出D符合下列条件的所有同分异构体的结构简式__________。
a.苯环上的一氯代物有两种 b.遇FeCl3溶液发生显色反应 c.能与Br2/CCl4溶液反应
节能减排是中国转型发展的必经之路,工业生产中联合生产是实现节能减排的重要措施,下图是几种工业生产的联合生产工艺: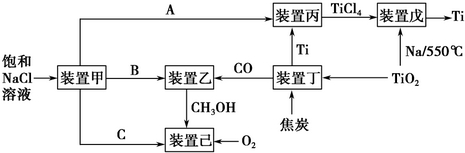
请回答下列问题:
(1)装置甲为电解池(惰性电极),根据图示转化关系可知:A为__________(填化学式),阴极反应式为__________。
(2)装置丙的反应物为Ti,而装置戊的生成物为Ti,这两个装置在该联合生产中并不矛盾,原因是__________装置戊进行反应时需要的环境为__________(填字母序号).
A.HCl气体氛围中 B.空气氛围中 C.氩气氛围中 D.水中
(3)装置乙中发生的是工业合成甲醇的反应:CO(g)+2H2(g)=CH3OH(g)△H<0.
①该反应在不同温度下的化学平衡常数(K)如下表:
| 温度/℃ |
250 |
350 |
| K |
2.041 |
x |
符合表中的平衡常数x的数值是__________(填字母序号).
A.0 B.0.012 C.32.081 D.100
②若装置乙为容积固定的密闭容器,不同时间段各物质的浓度如下表:
| c(CO)/mol•L-1 |
c(H2)/mol•L-1 |
c(CH3OH)/mol•L-1 |
|
| 0min |
0.8mol•L-1 |
1.6mol•L-1 |
0 |
| 2min |
0.6mol•L-1 |
y |
0.2mol•L-1 |
| 4min |
0.3mol•L-1 |
0.6mol•L-1 |
0.5mol•L-1 |
| 6min |
0.3mol•L-1 |
0.6mol•L-1 |
0.5mol•L-1 |
反应从2min到4min之间,H2的平均反应速率为__________,反应达到平衡时CO的转化率为__________,反应在第2min时改变了反应条件,改变的条件可能是__________(填字母序号).
A.使用催化剂 B.降低温度 C.增加H2的浓度
有一包白色粉末状混合物,可能含有K2CO3、CuSO4、AlCl3、NaOH中的某几种,现进行如下实验:
① 将混合物溶于水,得到无色透明溶液。
② 取少量上述溶液两份:
第一份中加入稀硝酸,开始出现白色沉淀,有气泡产生,继续加入稀硝酸,沉淀全部溶解,再加入AgNO3溶液,又出现白色沉淀;
第二份进行焰色反应,直接观察,火焰呈黄色。
根据上述实验现象回答:
(1)原混合物中肯定有 。
(2)第一份中,继续加入稀硝酸,沉淀全部溶解的离子方程式为 。
(3)第一份中,再加入AgNO3溶液,又出现白色沉淀的离子方程式为 。
(4)第二份进行焰色反应,为什么观察不到K+的焰色反应 。
化合物A(C12H16O2)经碱性水解、酸化后得到B和C(C8H8O2)。C的核磁共振氢谱表明含有苯环,且苯环上有2种氢原子。B经过下列反应后得到G(C8H12O4),核磁共振氢谱显示只有一个峰。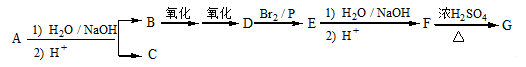
已知:
请回答下列问题:
(1)A的结构简式: 。
(2)写出F→G反应的化学方程式: ,该反应属于 (填反应类型)。
(3)写出满足下列条件的C的所有同分异构体的结构简式(至少写出3种): 。
①是苯的对位二取代化合物; ②能与FeCl3溶液发生显色反应;
③不考虑烯醇(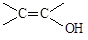 )结构。
)结构。
有机物H是一种药物的有效成分,其合成路线如下:
根据以上信息回答下列问题:
(1)A的结构简式为________,F含有的官能团是________(填名称)。
(2)反应①的条件是________,反应②的类型是________。
(3)合成的产物H具有的性质为________ (填序号)。
| A.在水中溶解度大于苯酚 |
| B.既有酸性又有碱性 |
| C.能发生缩聚反应 |
| D.能与溴水发生加成反应 |
(4)写出B在浓碱、高压条件下水解的化学方程式________。
(5)写出符合下列条件的D的一种同分异构体________。
①苯环上只有一个侧链②能和NaOH发生中和反应③分子中无甲基
(6)已知:① 发生取代时,在羧基间位取代;②
发生取代时,在羧基间位取代;② 易发生氧化反应。以A为原料合成化合物
易发生氧化反应。以A为原料合成化合物 的设计合成路线为(其他试剂任选):(合成路线流程图示例:
的设计合成路线为(其他试剂任选):(合成路线流程图示例:  )
)
辣椒素是辣椒的活性成分,可在口腔中产生灼烧感,能够起到降血压和胆固醇的功效,进而在很大程度上预防心脏病,也能缓解肌肉关节疼痛。辣椒素酯类化合物的结构可以表示为: (R为烃基)
(R为烃基)
其中一种辣椒素酯类化合物J的合成路线如下:
已知:
①A、B和E为同系物,其中B的相对分子质量为44,A和B核磁共振氢谱显示都有两组峰;
②化合物J的分子式为C15H22O4;
③
回答下列问题:
(1)G所含官能团的名称为 。
(2)由A和B生成C的化学方程式为 。
(3)由C生成D的反应类型为 ,D的化学名称为 。
(4)由H生成I的化学方程式为 。
(5)J的结构简式为 。
(6)G的同分异构体中,苯环上的一氯代物只有一种的共有 种(不含立体异构),核磁共振氢谱显示2组峰的是 (写结构简式)。
对羟基甲苯甲酸丁酯(俗称尼泊金丁酯)可用作防腐剂,对酵母和霉菌有很强的抑制作用,工业上常用对羟基苯甲酸与丁醇在浓硫酸催化下进行酯化反应而制得。以下是某课题组开发的廉价、易得的化工原料出发制备对羟基苯甲酸丁酯的合成路线
已知以下信息:
①通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基;
②D可与银氨溶液反应生成银镜; ③F的核磁共振氢谱表明其有两种不同化学环境的氢,且峰面积比为1:1。回答下列问题:
(1)E中所含官能团的名称为 ;
(2)D的结构简式为 ;F的分子式为 ;
(3)由B生成C的化学方程式为 ,该反应类型为 ; (4)在一定条件下,由G聚合得到的高分子化合物的结构简式为 。
(4)在一定条件下,由G聚合得到的高分子化合物的结构简式为 。
(5)写出符合下列条件的化合物G的所有同分异构体的结构简式 。
①苯环上一溴代产物只有两种;②遇FeCl3溶液显紫色;③能发生银镜反应。
①~⑨是几种有机物的名称或化学式:
①2,2,3-三甲基丁烷、②3-甲基-1-氯戊烷、③甲苯、④ 、⑤ClCH=CHCl、
、⑤ClCH=CHCl、

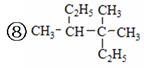 ⑨1,3,5-庚三烯
⑨1,3,5-庚三烯
据此回答下列问题:
(1)用系统命名法命名有机物⑧:_____________
(2)上述有机物中,互为同分异构体的是____________(用编号表示),存在顺反异构的是_______(用编号表示)。
(3)③苯环上的二氯代物有__________种,以该有机物为原料制备TNT炸药的化学方程式为_______
(4)已知在有机物分子中,若某个碳原子上连接4个不同的原子或基团,则这种碳原子称为“手性碳原子”,
如 中带*的C原子。若同一个碳原子上连着2个碳碳双键(如C==C==C)时,分子极不稳定,不存在。⑨1,3,5-庚三烯的众多链烃同分异构体中:
中带*的C原子。若同一个碳原子上连着2个碳碳双键(如C==C==C)时,分子极不稳定,不存在。⑨1,3,5-庚三烯的众多链烃同分异构体中:
含有“手性碳原子”,且与足量H2发生加成反应后仍具有“手性碳原子”的____________种。
含有“手性碳原子”,但与足量H2发生加成反应后,不具有“手性碳原子”的结构简式是___________________。
试题篮
()