氢气的生产、存储是氢能应用的核心。目前较成熟的生产、存储路线之一为:利用CH 3OH和H 2O在某Cu/Zn﹣Al催化剂存在下生产H 2,H 2与Mg在一定条件下制得储氢物质X。
回答问题:
(1)Al在周期表中的位置 。基态Zn的价层电子排布式 。
(2)水分子中氧原子的杂化轨道类型 。
(3)键能是衡量共价键稳定性的参数之一。 CH 3OH键参数中有 种键能数据。CH 3OH可以与水以任意比例互溶的原因是 。
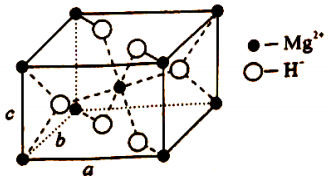
(4)X的晶胞结构如图所示(晶胞参数:α=β=γ=90°,a=b=450.25pm),密度为1.4g•cm ﹣ 3,H ﹣的配位数为 ,X的储氢质量分数是 ,c= pm (列出计算式即可)。
X、Y、Z均为短周期主族元素,它们原子的最外层电子数之和为10,X与Z同族,Y最外层电子数等于X次外层电子数,且Y原子半径大于Z。下列叙述正确的是( )
A. 熔点:X的氧化物比Y的氧化物高 B. 热稳定性:X的氢化物大于Z的氢化物
C. X与Z可形成离子化合物ZX D. Y的单质与Z的单质均能溶于浓硫酸
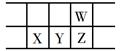
今年是门捷列夫发现元素周期律150周年。下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法错误的是( )
| A. |
原子半径:W<X |
B. |
常温常压下,Y单质为固态 |
| C. |
气态氢化物热稳定性:Z<W |
D. |
X的最高价氧化物的水化物是强碱 |
W、X、Y和Z为原子序数一次增大的四种短周期元素。W与X可生成一种红棕色有刺激性气味的气体;Y的周期数是族序数的3倍;Z原子最外层的电子数与W的电子总数相同,下列叙述正确的是()
| A. |
X与其他三种元素均可形成两种或两种以上的二元化合物 |
B. |
Y与其他三种元素分别形成的化合物中只含有离子键 |
| C. |
四种元素的简单离子具有相同的电子层结构 |
D. |
W的氧化物对应的水化物均为强酸 |
主族元素W、X、Y、Z的原子序数依次增加,且均不大于20,W、X、Z最外层电子数之和为10;W与Y同族;W与Z形成的化合物可与浓硫酸反应,其生成物可腐蚀玻璃。下列说法正确的是( )
| A. |
常温常压下X的单质为气态 |
B. |
Z的氢化物为离子化合物 |
| C. |
Y和Z形成的化合物的水溶液呈碱性 |
D. |
W与Y具有相同的最高化合价 |
短周期主族元素W、X、Y、Z的原子序数依次增大,W的简单氢化物可用作制冷剂,Y的原子半径是所有短周期主族元素中最大的.由X、Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气体产生.下列说法不正确的是( )
| A. |
X的简单氢化物的热稳定性比W强 |
B. |
Y的简单离子与X的具有相同的电子层结构 |
| C. |
Y与Z形成的化合物的水溶液可使蓝色石蕊试纸变红 |
D. |
Z与X属于同一主族,与Y属于同一周期 |
四种短周期主族元素W,X,Y,Z的原子序数依次增大,W,X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与Y同族,Z与X形成的离子化合物的水溶液呈中性.下列说法正确的是( )
| A. |
简单离子半径: |
B. |
W与X形成的化合物溶于水后溶液呈碱性 |
| C. |
气态氢化物的热稳定性: |
D. |
最高价氧化物的水化物的酸性: |
科学家合成出了一种新化合物(如图所示),其中
为同一短周期元素,Z核外最外层电子数是X核外电子数的一半。下列叙述正确的是

A. 的水溶液呈碱性
B.元素非金属性的顺序为 Z
C.Y的最高价氧化物的水化物是中强酸
D.该新化合物中Y不满足8电子稳定结构
我国嫦娥五号探测器带回1.731kg的月球土壤,经分析发现其构成与地球土壤类似。土壤中含有的短周期元素W、X、Y、Z,原子序数依次增大,最外层电子数之和为15。X、Y、Z为同周期相邻元素,且均不与W同族。下列结论正确的是( )
| A. |
原子半径大小顺序为 |
| B. |
化合物XW中的化学键为离子键 |
| C. |
Y单质的导电性能弱于Z单质的 |
| D. |
Z的氧化物的水化物的酸性强于碳酸 |
试题篮
()