在HCl、Cl2、O2、NH3、NO2、CO2、H2、SO2等中,
(1)不能用浓硫酸干燥的气体有_____________________________;
(2)酸雨主要有________________________气体造成的;
(3)比空气轻的气体有___________________________;
(4)用水作溶剂,可进行喷泉实验的气体有_________________;
(5)能用碱石灰干燥的气体有__________________________________;
(6)能使品红溶液褪色的气体有________________________________;
(7)可导致光化学烟雾的气体有________________________________。
(7分) 喷泉是一种常见的自然现象,产生原因是存在压强差。
试根据下图,回答下列问题: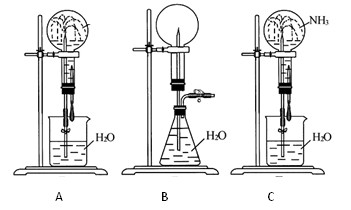
(1)在图A的烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体。下列组合中不可能形成喷泉的是( )。
A.HCl和H2O B.SO2和饱和NaHSO3溶液
C.Cl2和饱和NaCl溶液 D.CO2和NaOH溶液
(2)在图B的锥形瓶中,分别加入足量的下列物质,可能产生喷泉的是( )
A.Cu与稀盐酸 B.NaHCO3与NaOH溶液
C.CaCO3与稀硫酸 D.NaHCO3与浓盐酸
(3)如果提供如图C的装置,引发喷泉的方法和原理是
。
向如下图所示的装置中缓慢地通入气体X,若关闭活塞K,则品红溶液无变化而澄清石灰水变浑浊;若打开活塞K,则品红溶液褪色。X和Y可能是
| |
A |
B |
C |
D |
| X |
SO2 |
NO2 |
HCl |
Cl2 |
| Y |
饱和NaHCO3溶液 |
水 |
Na2SO3溶液 |
Na2SO3溶液 |
下列有关Cl、N、S等非金属元素化合物的说法正确的是:( )
| A.漂白粉的成分为次氯酸钙 |
| B.实验室可用浓硫酸干燥HI气体 |
| C.实验室可用NaOH溶液处理NO2和HCl废气 |
| D.Cl2与SO2以等物质的量比同时通入品红溶液,能增强其漂白性。 |
下列相关实验不能达到预期目的的是( )
| |
相关实验 |
预期目的 |
| ① |
将SO2通入溴水,溴水褪色后加热观察能否恢复原色 |
验证SO2漂白的可逆性 |
| ② |
将氯水加入淀粉KI溶液中 |
验证Cl的非金属性比I强 |
| ③ |
在相同温度下,将表面积相同的铝条和镁条投入等体积同浓度的盐酸中,观察产生气泡的速率。 |
比较同周期金属元素的金属性强弱。 |
| ④ |
将盐酸加入到Na2CO3溶液中,并将产生的气体通入Na2SiO3溶液中,观察实验现象。 |
比较Cl、C、Si的非金属性强弱。 |
A.仅① B.①④ C.②③ D.③④
CO、NO与SO2等物质是大气污染物。
(1)SO2不仅本身污染大气,而且它在大气中经尘粒催化能与水、氧气作用形成危害更大的酸雨,反应的化学方程式是:① ② 。
(2)CO、NO是汽车尾气的主要成分之一。冶理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,写出一氧化碳与一氧化氮反应的化学方程式: 。
根据硝酸和硫酸所具有的性质,选择适当的字母按要求填空。
| A.吸水性 | B.脱水性 | C.强氧化性 | D.强氧化性和酸性 |
(1)浓硫酸常用作干燥剂,说明浓硫酸具有 ;
(2)用玻璃棒蘸浓硫酸滴在纸上,发现变黑,说明浓硫酸具有 ;
(3)浓硫酸和浓硝酸都可以与铜反应,反应中浓硫酸和浓硝酸显示出 ;
北京奥运会所颁发的“金镶玉”奖牌,将青海软玉创造性地运用于奥运奖牌之上,蕴含着“以玉比德”的理念,中国特色浓厚,艺术风格典雅。青海软玉主要成分是由“透闪石”和“阳起石”组成的纤维状微晶结合体,“透闪石”的化学成分为Ca2Mg5Si8O22(OH)2。下列有关说法不正确的是:
| A.“透闪石”的化学式写成氧化物的形式为:2CaO·5MgO·8SiO2·H2O |
| B.“透闪石”中Mg元素的质量分数是Ca元素质量分数的2倍 |
| C.“透闪石”的化学式写成硅酸盐的形式为:2CaSiO3·5MgSiO3·H2SiO3 |
| D.“透闪石”不耐热,也不耐酸腐蚀 |
下列有关Cl、N、S、Si等非金属化合物的说法不正确的是( )
| A.硅胶、浓硫酸、碱石灰、无水氯化钙都是实验室常用的干燥剂,它们都可以用来干燥NH3、Cl2、SO2、H2等气体 |
| B.将氯气和石灰乳混合可制漂白粉,其有效成分是氯化钙 |
| C.硅是一种良好的半导体材料,可用作做光电池和计算机芯片 |
| D.液氨可用作制冷剂 |
(6分)把含硫酸铵和硝酸铵的混合液a L分成两等份。一份加入bmol NaOH并加热,恰好把NH3全部赶出,另一份需消耗cmol BaCl2沉淀反应恰好完全,试计算:
原混合溶液中含有的NH4+为 mol;
原溶液中NO3- 的浓度为 mol/L
合成氨厂所需H2可由焦炭与水反应制得,其中有一步反应为CO(g)+H2O(g)==CO2(g)+H2(g) △H<0欲提高CO转化率,可采用的方法是( )
①降低温度; ②增大压强; ③使用催化剂;④增大CO浓度; ⑤增大水蒸气浓度
| A.①②③ | B.④⑤ | C.①⑤ | D.⑤ |
试题篮
()