下表是元素周期表中短周期部分,表中所列字母分别代表一种元素,试回答有关问题。
(1)只由A、D、F三种元素组成的可为人体提供能量的营养物质是 (填其中一种物质的名称)
(2)A和D可形成一种最简单化合物,它的分子构型为: 。这种化合物含
键。(填“极性”或“非极性”)
(3)由上表元素中的两个原子形成的阴离子的电子式为 。
(4)NH3·H2O的电离方程式为: ,据此电离方程式推断NH3溶于水后的合理结构是: (填序号)。
(5)下图是A2与F2发生反应生成A2F的途径和三个状态的能量(E)
则:①步骤l是 (填“吸热”或“放热”,下同)过程,步骤2是 过程。
②比较E1、E2、E3的大小 。(由大到小顺序排列)
X、Y、Z三种短周期元素,它们的原子序数之和为16。三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如图所示变化。已知一个B分子中含有的Z元素的原子个数比C分子中少一个。
请回答下列问题:
(1)X元素在周期表中的位置是 ;Y单质的电子式为 。
(2)X的单质与Z的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由空隙中逸出,并在电极表面放电,则正极通入 (填物质名称);负极电极反应式为 。
(3)A与C在一定条件下反应,该反应是消除硝酸工业尾气污染的原理,其化学方程式是
(4)X、Y、Z三种元素可组成一种强酸W与C反应的离子方程式为:
有X、Y、Z三种元素,已知:①X、Y为短周期元素,且X2-、Y-两种离子均具有相同的电子数;②Z与Y可组成化合物ZY3,ZY3溶液遇KSCN溶液显红色。试回答:
(1)X的最高价氧化物对应水化物的化学式是
(2)将ZY3溶液滴入沸水可得到红褐色胶体,反应的离子方程式是 ,光束通过该液体时形成光亮的“通路”,该现象叫____________。
(3)Na2X的电子式为
(4)X的低价氧化物与含1.5molY的一种含氧酸(该酸的某盐常用于实验室制备氧气)的溶液在一定条件下反应,可生成一种强酸和一种氧化物,若有1.5×6.02×1023个电子转移时,该反应的化学方程式是
现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A与D同主族,C与E同主族,D、E、F同周期,A、B的最外层电子数之和与C的最外层电子数相等,A能分别与B、C形成电子数相等的分子,且A与C形成的化合物常温下为液态,A能分别与E、F形成电子总数相等的气体分子.请回答下列问题(题中字母只代表元素代号,与实际元素符号无关):
(1)B、F可形成三角锥形分子,其电子式为 (2分)
(2)B、C、E的气态氢化物沸点由高到低的顺序为: (2分)
(3)C、E形成的化合物通入F的单质的水溶液中,可形成两种强电解质,则该反应的离子方程式为: 。
(4)A、B、C可形成常见的化合物H,足量的H的稀溶液与a g Fe完全反应,被还原的H的物质的量为: 。
下表为元素周期表的一部分。表中所列的字母分别代表某一元素。
(1)元素F的名称是_____________;
(2)B、C、D、E四种元素的氢化物中最稳定的是____________(写化学式);
(3)写出B的最高价氧化物的电子式 ________;
(4)1molA与D的氢化物完全反应产生的气体在标准状况下的体积为 。
(21分)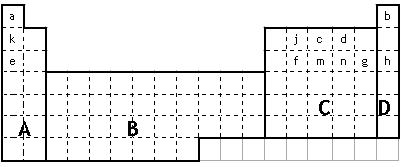
(1)在上面元素周期表中全部是金属元素的区域为 。


(a)A (b)B (c)C (d)D
(2)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或浓硝酸中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。
②甲、乙两元素相比较,金属性较强的是 (填名称),可以验证该结论的实
验是 。
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
③写出甲的氧化物及氧化物对应水化物分别与强碱反应的离子方程式
、 。


(3)表中所列小写字母分别代表一种化学元素:
①m、f、j的单质熔点由高到低的顺序___________________________(填元素符号)。
②以上元素形成的金属单质中,熔点最低的是____________________(填元素符号)。
③f、m、n、g所形成的氢化物的稳定性还性由强到弱的顺序为
____________________________________________________________(填化学式);
④甲、乙、c、d、e形成的简单离子的半径由小到大的顺序为
___________________________________________________________。
⑤f元素单质是在生产中用量很大,试写出工业上制备f元素单质的化学方程式
_____________________________________________________________________。
⑥c元素的单质用途_______________________________________________(填一条)。
A、B、C、D、E、F都是短周期元素,原子序数依次增大。
| 元素 |
有关信息 |
| A |
原子最外层电子数和电子层数相等 |
| B |
原子的最外层电子数是内层电子数的2倍 |
| C |
元素主要化合价为-2,原子半径为66pm |
| D |
与A同主族,最高价氧化物对应的水化物易溶于水 |
| E |
原子半径为104pm,所在主族序数与所在周期序数之差为3 |
| F |
单质为有色的气体 |
(1)D2C的电子式 ;
(2)沸点:A2C A2E(填“>”或“<”或“=”);
(3)E的非金属性比F (填“强”或“弱”),并用化学事实加以说明(用化学方程式表示) ;
(4)化合物甲由A、B、C、D四种元素组成,其化学式量为84,是焙制糕点所用发酵粉的主要成分之一。写出甲在水溶液中与盐酸反应的离子方程式 。
X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X、Y、E的元素符号依次为 、_______ 、 ____ ;
(2)XZ2与YZ2分子的立体结构分别是 和 ,
相同条件下两者在水中的溶解度较大的是
(写分子式),理由是 ;
(3)Q的元素符号是 ,它属于第 周期,
它的核外电子排布式为 ,在形成化合物时,它的最高化合价为 .
已知五种元素的原子序数的大小顺序为C>A>B>D>E;A、C同周期,B、C同主族;A与B形成离子化合物,A2B中所有离子的电子数相同,其电子总数为30;D和E形成4核10电子分子。试回答下列问题:
(1)C位于元素周期表中第________周期________族;A的原子结构示意图为___________________。
(2)用电子式表示离子化合物A2B的形成过程___________________________。
(3)写出D元素形成单质的结构式____________,A、B、E形成化合物的电子式________________。
(4)A、B两元素组成化合物A2B2属于_________(“离子”“共价”)化合物,存在的化学键是___________________,写出A2B2与水反应的化学方程式_________________________。
某元素同位素 ,其氯化物XCl2 1.11g溶于水制成溶液后,加入1mol/L的AgNO3溶液20mL恰好完全反应。若这种同位素原子核内有20个中子,则:
,其氯化物XCl2 1.11g溶于水制成溶液后,加入1mol/L的AgNO3溶液20mL恰好完全反应。若这种同位素原子核内有20个中子,则:
(1)Z值和A值;Z= ;A= ;
(2)X元素在周期表中的位置 ;
(3)根据已学知识推测,把X的单质放入水中反应的化学方程式为. 。
A、B、C、D、E五种短周期元素,它们的原子序数依次增大。B元素原子L层上的电子数为K层电子数的2倍;元素D的2价阴离子的核外电子排布与氖原子相同;E与A同主族;A和E 这两种元素与D都能形成X2Y、X2Y2型化合物。请回答:
(1)写出元素的符号:A ;C_______
(2)画出D的离子结构示意图_____________,B在周期表的位置为 。
(3)B的X2Y2型化合物结构式是_______,E的X2Y型化合物电子式为 。
(4)B与D形成最高价化合物的电子式 。
(5)C的氢化物和C的最高价氧化物的水化物反应生成M,M的化学式为 ,M中的化学键类型有__________________。
现有部分短周期元素的性质或原子结构如下表:
| 元素编号 |
元素性质或原子结构 |
| T |
M层上有6个电子 |
| X |
最外层电子数是次外层电子数的2倍 |
| Y |
常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z |
元素最高正价是+7价 |
(1)元素T为 元素(填元素名称)。元素X的一种同位素可测定文物年代,这种同位素的符号是 。
(2)元素Y与氢元素形成一种离子YH4+,写出该微粒的电子式
(用元素符号表示)。
(3)元素Z与元素T相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是 ,理由是 
下表为元素周期表的一部分,请参照①~⑩在表中的位置,用化学用语回答下列问题:
(1)元素③形成的单质的电子式为 ;元素②形成的最高价氧化物的结构式为 。
(2)⑥、⑦两元素的最高价氧化物的水化物之间反应的离子方程式为 。
(3)②、③、④、⑤元素形成的氢化物中,热稳定性最强的是 (填化学式),沸点最高的是 (填化学式)。
(4)⑧、⑨元素的最高价氧化物的水化物酸性强弱比较 > (填化学式)。
(5)用电子式表示⑥、⑧两元素结合成化合物的形成过程 。
(6)元素⑩在周期表中的位置 ;该元素的单质主要用途 (填一种)。
A、B、C、D四种元素在周期表中分别处于元素X的四周,已知X元素最高价氧化物的化学式为X2O5,且五种元素中有一种元素的原子半径是它们所处的同族中最小的。试确定:
| |
B |
|
| A |
X |
C |
| |
D |
|
(1)各元素的符号:
A C
(2)确定C、D、X最高价氧化物对应水化物的化学式,并排列酸性由强到弱的顺序 ____________ 。
(3)确定A、B、X气态氢化物的化学式,并排列稳定性由强到弱的顺序 _______ 。
试题篮
()