A、B、C、D、E五种元素均是短周期的主族元素,原子序数依次增大。B、E原子的最外层电子数均为其电子层数的两倍,D、E元素原子的最外层电子数相等。X、Y、Z、W均由上述元素的两种元素组成,甲、乙均由上述元素的三种元素组成。元素B形成的单质M与甲、乙均能反应(相对分子质量甲<乙)。转化关系如图(反应条件略去)。请回答下列问题:
(1)X、Y、Z、W属于同一类物质,这类化合物可称为 ;X、Y、W都能与Z反应,则Z为 (写化学式)。
(2)写出M与甲的浓溶液、M与乙的浓溶液加热时反应的化学方程式:
① ;② 。
(3)化合物BE2与化合物Y结构相似,则BE2的电子式为 。
(4)上述六种化合物中 是空气质量日报必须分析测定的物质,他们的危害是 。(写一种及对应危害即可)
(5)将X、W与D按1:1:n通入Z中,充分反应后无气体剩余或生成,写出反应的化学方程式 。
下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:

(1)④、⑤、⑥的原子半径由大到小的顺序为_________________________。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是_________________________。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。
(4)由表中两种元素的原子按1:1组成的常见液态化合物的溶液易被催化分解,可使用的催化剂为(填序号)_________________。
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
X溶液与Y溶液反应的离子方程式为_______________________________,
N→⑥的单质的化学方程式为______________________________________。
短周期元素A、B、C、D中,0.5mol A元素的离子得到6.02×1023个电子被还原为中性原子,0.4g A的氧化物恰好与100ml 0.2mol/L的盐酸完全反应,A原子核内质子数目与中子数目相等,B元素原子核外M层电子数目比K层多1个,C―比A元素的离子多1个电子层,D元素的原子核外L层比K层多2个电子。
(1)A、B、C、D四种元素的名称分别是 、 、 、 。
(2)画出C―和D原子的结构 示意图 ,
示意图 ,
(3)向B、C两种元素形成的化合物的水溶液里逐滴滴入苛性钠溶液,现象为__________,写出有关离子方程式_____________;________________。
下表是元素周期表的前三周期:
| |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 一 |
A |
|
|
|
|
|
|
|
| 二 |
B |
|
|
C |
D |
E |
F |
|
| 三 |
G |
|
H |
|
|
|
I |
J |
回答下列问题:
⑴写出下列元素的元素的符号:
F______________、J_____________。
⑵G元素与E元素形成的化合物的化学式是____________、____________,它们都是_________________(填“离子”或“共价”)化合物。
⑶表格中十种元素的最高氧化物对应的水化物中,酸性最强的是_____________,属于两性氢氧化物的是_______________(用化合物的化学式表示)。
⑷只含有A、C两种元素的化合物称为_____________,这些化合物中:
①相对分子质量最小的是________________,该化合物的分子空间构型是_______________;
②分子中含有双键,但原子数最少的是______________,它与HCl反应的化学方程式为______________________________;
⑸将H单质与C的一种单质(导体)按如下图装置连接,该装置称为_____________。其中C极为______________,(填正负极)并写出该电极反应式为:____________________。请在下图中标出电子流动方向。
(11分) 元素周期表反映了元素性质的周期性变化规律。请根据短周期元素在周期表中的位置、结构和相关性质,回答下列问题:
(7) 第VIA族元素形成的气态氢化物中沸点最高的是____________(用分子式表示),原因是____________________,该分子的空间构型为______________。
(8) 第二周期元素中,除Be、B、Ne三种元素外,其他元素的氢化物沸点如表1所示,其中E的化学式为 ;第三周期元素单质的熔点(℃)变化如图a所示,其中h的元素符号为 。 (表1)
| 氢化物 |
A |
B |
HF |
D |
E |
| 沸点/℃ |
1317 |
100 |
19.5 |
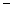 33.35 33.35 |
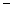 164 164 |
(9) 第二、第三周期的某些元素能形成单质甲和化合物乙,它们具有图b所示的结构单元,甲和乙的晶体类型相同,甲的某种同素异形体与乙在高温时能发生置换反应生成h的单质和CO。若该反应生成的h的单质含有1 mol共价键,则参加反应的乙的质量为_______________g。
(10)碳元素的某种单质具有平面层状结构,该单质的名称为__________;同一层中的原子构成许多的正六边形,单质与熔融的钾相互作用,形成某种青铜色的物质(其中的元素钾用“●”表示),原子分布如图c所示,该物质的化学式为 。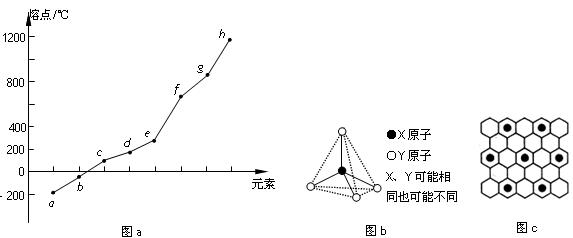
(9分) A、B、C、D是中学化学中常见的四种短周期元素。已知①A具有多种同素异形体,A元素原子最外层电子数是次外层电子数的2倍。②B元素最高正价为 + 5。③C元素有多种化合价,且常温下C元素的单质与某种一元碱溶液反应,可得到两种含C元素的化合物。④B、C两种元素质子数之和是A元素质子数的4倍。⑤D是地壳中含量第二的元素,它的单质是一种良好的半导体材料。
(1) 写出A元素的名称_________和C离子的结构示意图____________。
(2) 工业上利用A的单质来制备单质D,请写出相应的方程式:
________________________________________________________________________。
(3) 由B、C两种元素组成的化合物X,常温下为易挥发的淡黄色液体,X分子为三角锥形分子,且分子里B、C两种原子最外层均达到8个电子的稳定结构。X遇水蒸气可形成一种见的漂白性物质和一种能使石蕊试纸变蓝的气体。则X的分子式 。X分子中B、C原子间的化学键的类型为___________(填“极性键”或“非极性键”)。X与水反应的化学方程式________________________。
a、b、c、d、e、f、g为七种由短周期元素构成的粒子,它们都有10个电子,其结构特点如下:
其中b的离子半径大于e的离子半径;d是由极性键构成的四原子分子;试写出:
(1)、写出下列粒子的电子式:
①c__________;②d__________;③e__________;④a__________。
(2)、b与e相应元素的最高价氧化物对应水化物的碱性强弱比较为:__________>__________(用化学式表示)。
(3)、用电子式表示b元素与氧形成的化合物b2O的形成过程:________________。
A、B、C、D、E、F是原子序数依次增大的同周期元素,已知A、C、F的原子最外层电子数之和为11,且这三种元素的最高价氧化物对应的水化物之间两两皆能反应,均生成盐和水;D元素原子的次外层电子数比最外层电子数多4,E元素原子的最外层与最内层电子数的差是3。试回答下列问题:
(1)写出下列元素符号:A ,C ,D ,E 。
(2)用电子式表示B和F形成化合物的过程: 。
(3)写出A、C、F三种元素最高价氧化物对应的水化物相互反应的化学方程式:
、 、 。
(7分)短周期元素A、B、C、D原子序数依次增大。已知A与D同主族,B与C同周期,A元素原子核外只有1个电子,B元素原子的最外层电子数是次外层电子数2倍,C元素原子的电子总数是电子层数的4倍,回答下列问题:
(1)B元素在周期表中的位置是________________;B元素能形成金刚石、石墨、C60等多种单质,这几种单质互称为_________________。
(2)C元素与A 元素形成的化合物A2C常温下可D元素的单质发生剧烈反应,该反应的离子方程式为:_____________ _。
(3)B元素最高价氧化物X与D元素最高价氧化物对应水化物Y发生反应可生成两种盐
(酸式盐和正盐),写出由X和Y两种化合物反应生成正盐的化学方程式:_____________ ____ ________。
1932年,美国化学大师Linus Pauling提出电负性(用希腊字母χ表示)的概念,用来确定化合物中原子某种能力的相对大小。Linus Pauling假定F的电负性为4,并通过热化学方法建立了其他元素的电负性。Linus Pauling建立的主族元素的电负性如下:
| H:2.1 |
|
|
|
|
|
|
| Li:1.0 |
Be:1.5 |
B:2.0 |
C:2.5 |
N:3.0 |
O:3.5 |
F:4.0 |
| Na:0.9 |
Mg:1.2 |
Al:1.5 |
Si:1.8 |
P:2.1 |
S:2.5 |
Cl:3.0 |
| K:0.8 |
Ca:1.0 |
Ga:1.6 |
Ge:1.8 |
As:2.0 |
Se:2.4 |
Br:2.8 |
| Rb:0.8 |
Sr:1.0 |
In:1.7 |
Sn:1.8 |
Sb:1.9 |
Te:χ |
I:2.5 |
| Cs:0.7 |
Ba:0.9 |
Tl:1.8 |
Pb:1.9 |
Bi:1.9 |
Po:2.0 |
At:2.2 |
| Fr:0.7 |
Ra:0.9 |
|
|
|
|
|
回答下列问题:
⑴纵观各周期主族元素电负性变化,谈谈你对元素性质呈现周期性变化的理解: ;
⑵预测Te元素χ的值 ;
⑶你认为Linus Pauling提出电负性的概念是确定化合物中原子哪种能力的相对大小? ;
⑷大量事实表明,当两种元素的电负性差值小于1.7时,这两种元素通常形成共价化合物。用电子式表示AlBr3的形成过程 。
有A、B、C、D、E五种短周期元素,已知A、B、C三种元素的原子序数越来越大,在周期表中A、B同族,B、C为同周期相邻元素,这三种元素的原子核外电子数之和是41,D元素的质子数介于A、B之间,它在空气中燃烧生成淡黄色固体,E元素的原子核内中子数比质子数多1个,0.9 g E单质与足量稀盐酸反应生成0.1 g氢气,并转化为E3+,试回答:
(1)写出元素符号A 、B 、C 、D的离子结构示意图 、E在周期表中的位置是 ;C单质的电子式为
(2)用电子式表示B与D形成的化合物的过程:
(3)D在空气中燃烧的化学方程式
(4)写出D、E的最高价氧化物对应水化物间反应的离子方程式:
原子序数依次增大的A、B、C、D四种短周期元素。元素A的原子半径在短周期中最小,元素C的单质在空气中含量最多,D所在周期的各元素单质沸点变化如图I(原子序数按递增顺序连续排列)。B、C、D三种元素均能与A形成等电子的三种分子,且化合物中各原子的个数比为:
| 化合物 |
甲 |
乙 |
丙 |
| 原子个数比 |
B∶A=1∶3 |
C∶A=1∶2 |
D∶A=1∶2 |
(1)元素D在元素周期中的位置 。
(2)B、C形成的一种化合物X是一种原子晶体,晶体中B、C原子均达到稳定结构,则X的化学式为 ;X的熔点 金刚石(填“大于”、“等于”或“小于”)。
(3)写出图I中沸点最高的单质与NaOH溶液反应的离子方程式 。
计算下列分子或离子中的价电子对数,并根据已学填写下表
| 物质 |
价电子 对数 |
成键电 子对数 |
孤电子 对数 |
中心原子杂 化轨道类型 |
杂化轨道/电子 对空间构型 |
轨道 夹角 |
分子空 间构型 |
键角 |
| CO2 |
|
|
|
|
|
|
|
|
| BF3 |
|
|
|
|
|
|
|
|
| CH4 |
|
|
|
|
|
|
|
|
| H2O |
|
|
|
|
|
|
|
|
| NH3 |
|
|
|
|
|
|
|
|
| PCl3 |
|
|
|
|
|
|
|
|
有A、B、C、D、E五种短周期元素,且相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的氢氧化物是两性氢氧化物,E的阳离子与A的阴离子核外电子层结构相同。
请回答下列问题:
(1)B元素在周期表中的位置为 ;
(2)A与氢元素能形成原子物质的量之比为1:1的化合物,其电子式为 ;
(3)向D与E形成的化合物的水溶液中滴入NaOH溶液直至过量,观察到的现象是 ,最后阶段反应的离子方程式为 ;
(4)B、C、D、E的最高价氧化物的水化物的酸性从强到弱的顺序为(物质用化学式表示) 。
试题篮
()