下列对有关事实的解释正确的是( )
事实 |
解释 |
|
A |
某些金属盐灼烧呈现不同焰色 |
电子从低能轨道跃迁至高能轨道时吸收光波长不同 |
B |
CH4与NH3分子的空间构型不同 |
二者中心原子杂化轨道类型不同 |
C |
HF的热稳定性比HCl强 |
H﹣F比H﹣Cl的键能大 |
D |
SiO2的熔点比干冰高 |
SiO2分子间的范德华力大 |
A.AB.BC.CD.D
下表中对应关系正确的是
| A |
CH3CH3+Cl2 CH3CH2Cl+HCl CH3CH2Cl+HClCH2=CH2+HCl→CH3CH2Cl |
均为取代反应 |
| B |
由油脂得到甘油 由淀粉得到葡萄糖 |
均发生了水解反应 |
| C |
Cl2+2Br‾=2Cl‾+Br2 Zn+Cu2+=Zn2++Cu |
均为单质被还原的置换反应 |
| D |
2Na2O2+2H2O=4NaOH+O2↑ Cl2+H2O=HCl+HClO |
均为水作还原剂的氧化还原反应 |
硫及其化合物有许多用途,相关物质的物理常数如下表所示:
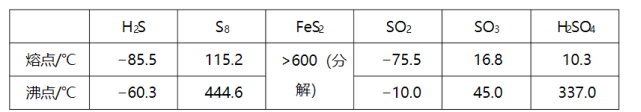
回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为________,基态S原子电子占据最高能级的电子云轮廓图为________ 形。
(2)根据价层电子对互斥理论, , , 的气态分子中,中心原子价层电子对数不同于其他分子的是________。
(3)图(a)为 的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为________。
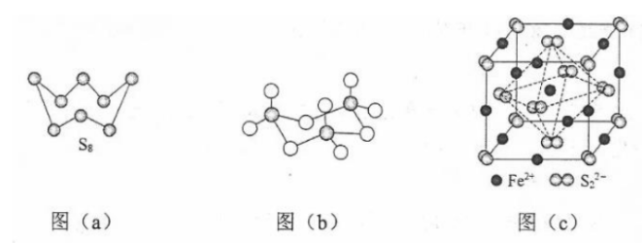
(4)气态三氧化硫以单分子形式存在,其分子的立体构型为________形,其中共价键的类型有________种;固体三氧化硫中存在如图(b)所示的三氯分子。该分子中S原子的杂化轨道类型为________。
(5) 晶体的晶胞如图(c)所示,晶胞边长为 , 相对式量为M、阿伏伽德罗常数的值为 , 其晶体密度的计算表达式为________ ;晶胞中 位于 所形成的正八面体的体心,该正八面体的边长为________ nm
下列有机反应属于加聚反应的是
A.CH4+Cl2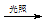 CH3Cl+HCl CH3Cl+HCl |
B.nCH2=CH2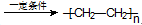 |
C.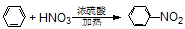 + H2O + H2O |
D.2CH3CH2OH +2Na→2CH3CH2ONa+H2↑ |
下列有机反应属于加成反应的是
A.CH4+Cl2 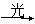 CH3Cl+HCl CH3Cl+HCl |
B.CH3CH2OH+CH3COOH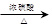 CH3COOCH2CH3+H2O CH3COOCH2CH3+H2O |
C.H2C=CH2 + HCl H2C-CH2Cl H2C-CH2Cl |
D.2CH3CH2OH + O2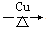 2CH3CHO + 2H2O 2CH3CHO + 2H2O |
下列反应中,属于加成反应的是
A.CH3CH2OH+CH3COOH CH3COOCH2CH3+ H2O CH3COOCH2CH3+ H2O |
B.2CH3CHO + O2 2CH3COOH 2CH3COOH |
C.CH3—CH=CH2 + Br2  CH3—CHBr-CH2Br CH3—CHBr-CH2Br |
D. +Br2 +Br2  + HBr + HBr |
过渡金属元素铬 是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
(1)对于基态 原子,下列叙述正确的是 (填标号)。
A.轨道处于半充满时体系总能量低,核外电子排布应为
B. 电子能量较高,总是在比 电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
(2)三价铬离子能形成多种配位化合物。 中提供电子对形成配位键的原子是 ,中心离子的配位数为 。
(3) 中配体分子 、 以及分子 的空间结构和相应的键角如图所示。
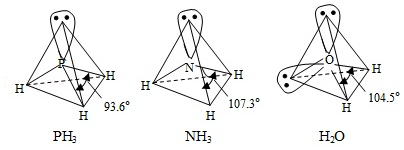
中 的杂化类型是 。 的沸点比 的 ,原因是 。 的键角小于 的,分析原因 。
(4)在金属材料中添加 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。 具有体心四方结构,如图所示。处于顶角位置的是 原子。设 和 原子半径分别为 和 ,则金属原子空间占有率为 %(列出计算表达式)。

下图是一些常见有机物的转化关系,关于反应①~⑦的说法不正确的是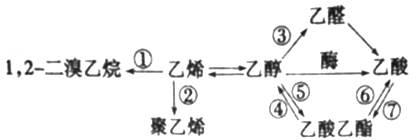
| A.反应①是加成反应 | B.只有反应②是加聚反应 |
| C.只有反应⑦是取代反应 | D.反应④⑤⑥是取代反应 |
下列各化合物中,能发生酯化、加成、消去三种反应的是
| A.CH3—CH==CH—CHO |
B.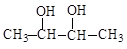 |
| C.HOCH2—CH2—CH==CH—CHO |
D.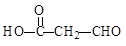 |
[化学--选修3:物质结构与性质]
研究发现,在 低压合成甲醇反应 中, 氧化物负载的 氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1) 基态原子核外电子排布式为________。元素 与O中,第一电离能较大的是________,基态原子核外未成对电子数较多的是________。
(2) 和 分子中 原子的杂化形式分别为________和________。
(3)在 低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为________,原因是________。
(4)硝酸锰是制备上述反应催化剂的原料, 中的化学键除了 键外,还存在________。
(5) 具有 型结构(如图),其中阴离子采用面心立方最密堆积方式, 射线衍射实验测得 的晶胞参数为 ,则 为________ 。 也属于 型结构,晶胞参数为 ,则 为________ 。

锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Zn原子核外电子排布式为________。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能 ________ (填"大于"或"小于")。原因是________。
(3) 具有较高的熔点(872 ℃),其化学键类型是________; 不溶于有机溶剂而 、 、 能够溶于乙醇、乙醚等有机溶剂,原因是________。
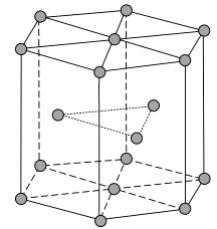
(4)《中华本草》等中医典籍中,记载了炉甘石( )入药,可用于治疗皮肤炎症或表面创伤。 中,阴离子空间构型为________,C原子的杂化形式为________。 (5)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为________。六棱柱底边边长为 acm,高为 ccm,阿伏加德罗常数的值为 , Zn的密度为________ (列出计算式)。
砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等.回答下列问题:
(1)写出基态As原子的核外电子排布式________.
(2)根据元素周期律,原子半径Ga________As,第一电离能Ga________As.(填"大于"或"小于")
(3) 分子的立体构型为________,其中As的杂化轨道类型为________.
(4) 的熔点高于1000℃, 的熔点为77.9℃,其原因是________.
(5)GaAs的熔点为1238℃,密度为 , 其晶胞结构如图所示.
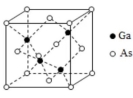
该晶体的类型为________,Ga与As以________键键合.Ga和As的摩尔质量分别为 和 , 原子半径分别为 和 ,阿伏伽德罗常数值为 ,则GaAs晶胞中原子的体积占晶胞体积的百分率为________.
氨硼烷(NH 3BH 3)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
(1)H、B、N中,原子半径最大的是 。根据对角线规则,B的一些化学性质与元素 的相似。
(2)NH 3BH 3分子中,N﹣B化学键称为 键,其电子对由 提供。氨硼烷在催化剂作用下水解释放氢气:
3NH 3BH 3+6H 2O═3NH 4 ++B 3O 6 3 ﹣+9H 2
B 3O 6 3 ﹣的结构为 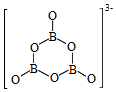 .在该反应中,B原子的杂化轨道类型由 变为 。
.在该反应中,B原子的杂化轨道类型由 变为 。
(3)NH 3BH 3分子中,与N原子相连的H呈正电性(H δ +),与B原子相连的H呈负电性(H δ﹣),电负性大小顺序是 。与NH 3BH 3原子总数相等的等电子体是 (写分子式),其熔点比NH 3BH 3 (填"高"或"低"),原因是在NH 3BH 3分子之间,存在 作用,也称"双氢键"。
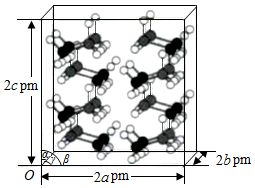
(4)研究发现,氨硼烷在低温高压条件下为正交晶系结构,晶胞参数分别为apm、bpm、cpm,α=β=γ=90°.氨硼烷的2×2×2超晶胞结构如图所示。氨硼烷晶体的密度ρ= g•cm ﹣ 3(列出计算式,设N A为阿伏加德罗常数的值)。
解热、镇痛药物布洛芬的两种合成路线如下:
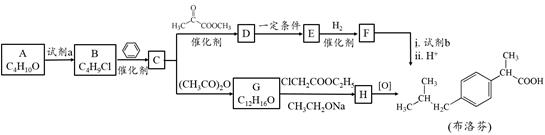
已知: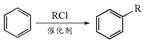 (R为烃基)
(R为烃基)
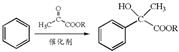 (R为烃基)
(R为烃基)
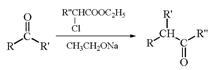 (R、R’、R’’为烃基或氢原子)
(R、R’、R’’为烃基或氢原子)
(1)A为醇,其核磁共振氢谱有四个吸收峰。A的结构简式是 。
(2)A与试剂a反应生成B的反应类型是 。
(3)由B生成C的化学方程式是 。
(4)D与E的相对分子质量相差18,由D生成E的化学反应方程式是 。
(5)G的结构简式是 ,H的含氧官能团的名称是 。
(6)布洛芬有多种同分异构体,写出满足下列条件的任意两种同分异构体的结构简式 。
a. 羧基与苯环直接相连 b. 苯环上有三个取代基,且苯环上的一氯代物有两种
试题篮
()