离子可在琼脂中移动,某简易电池如图所示,放电时,下列说法错误的是
| A.锌极上电极反应式为:Zn-2e-=Zn2+ |
| B.MnO2得电子被还原 |
| C.NH4+离子通过琼脂向锌极移动 |
| D.外线路中电流的方向从碳棒到锌片 |
高铁电池是一种新型可充电电池,该电池能长时间保持稳定的放电电压。高铁电池的总反应为: 下列判断正确的是
下列判断正确的是
| A.充电时阳极反应为:2FeO42-+8H2O-6e-=2Fe(OH)3+10OH- |
| B.充电时阴极附近溶液的pH变大 |
| C.放电时,负极材料为Zn |
| D.放电时,每转移0.2 mol电子,正极的质量减少6.5 g |
零排放燃料电池曾被美国《时代》杂志列为21世纪改变人类生活的十大新科技之首。其中最具代表意义的质子交换膜燃料电池的工作原理如图所示,其中电极a、b均为多孔活性铂电极。下列说法中不正确的是
| A.a极为该电池的负极 |
| B.该电池的正极反应式为O2 + 4H+ + 4e- =2H2O |
| C.该电池的能量转化主要形式是化学能转化为电能 |
| D.H+(质子)由正极移动至负极 |
对外加电流的保护中,下列叙述正确的是
| A.被保护的金属与电源的正极相连 |
| B.被保护的金属与电源的负极相连 |
| C.在被保护的金属表面上发生氧化反应 |
| D.被保护的金属表面上不发生氧化反应,也不发生还原反应 |
常见的铅蓄电池的电极材料为PbO2和Pb,电解液为30%的稀硫酸溶液,电池放电的总反应为:PbO2 + Pb + 2H2SO4  2PbSO4 + 2H2O,则下列说法正确的是
2PbSO4 + 2H2O,则下列说法正确的是
| A.PbO2为电池的负极 | B.放电时电子由正极流向负极 |
| C.放电时正极发生氧化反应 | D.放电时电解液的pH值逐渐增大 |
(8分)电池有干电池、蓄电池、燃料电池等。
(1)手电筒使 用的是普通锌-锰电池,请写出该电池工作时发生的
用的是普通锌-锰电池,请写出该电池工作时发生的
a.正极反应_____________________________________________________
b.电池总反应___________________________________________________ (2)汽车上使用的是Pb-PbO2-H2SO4构成的可反复使用的蓄电池,请写出该电池工作时
(2)汽车上使用的是Pb-PbO2-H2SO4构成的可反复使用的蓄电池,请写出该电池工作时
a.正极反应_________________________________________
b.电池总反应_________________________________________________
某储能电池的原理如图所示,溶液中c(H+) =" 2.0" mol·L-1,阴离子为SO42-,a、b均为惰性电极,充电过程中左槽溶液颜色由蓝色变为黄色。下列叙述正确的是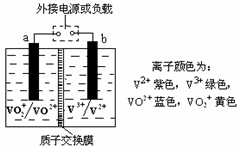
| A.当右槽溶液颜色由绿色变为紫色时,电池中能量转化形式为化学能转化为电能 |
| B.充电过程中,a极的反应式为VO2+-e-+ H2O = VO2++ 2H+ |
| C.储能电池a、b两极间的电解质溶液中通过电子的定向移动形成闭合回路 |
| D.放电时,当转移的电子数为6.02 × 1023时,共有1.0 mol H+从右槽迁移进入左槽 |
科学家预言,燃料电池将是21世纪获得电能的重要途径。近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子和水分子通过。其工作原理的示意图如下:下列说法错误的是
| A.a是负极,b是正极 |
| B.b极的电反应是:O2+4H++4e-=2H2O |
| C.甲醇在a极上得电子,发生还原反应 |
D.当电路上通过2mol电子消耗的CH3OH为 mol mol |
下图是生活中常用的锌锰干电池的示意图,下列有关说法中不正确的是
| A.电池内部含有电解质 | B.锌是负极,碳棒是正极 |
| C.电池用完后可埋入土壤 | D.锌锰干电池属一次电池 |
(8分)某同学用铅蓄电池作电源,用石墨做电极电解500 mL某浓度的CuSO4溶液,观察到A电极表面有红色固体物质生成,当溶液中原有溶质完全电解后,停止通电,取出A电极,洗涤、干燥、称量,电极增重1.6 g。已知铅蓄电池的工作原理为:
Pb+PbO2+2H2SO4 2PbSO4+2H2O
2PbSO4+2H2O
请按要求回答下列问题:
(1)电解CuSO4溶液的化学方程式 ,
(2)当反应过程中转移的电子为0.02mol时,铅蓄电池内消耗硫酸的物质的量为 mol。
(3)电解前CuSO4溶液的物质的量浓度为 。
(4)若电解前后溶液的体积不变,电解后溶液的pH=
(5)写出铅蓄电池负极的电极反应式:
一种新型燃料电池,它是用惰性金属作电极插入KOH溶液中,然后向两极上分别通入甲烷和氧气,发生的电极反应为:X极:CH4 + 10OH--8e-= CO32-+ 7 H2O Y极:2O2 + 4 H2O + 8e-=" 8" OH-;关于此燃料电池的说法不正确的是( )
| A.X极发生氧化反应,Y极发生还原反应 |
| B.工作一段时间后,KOH的物质的量减少 |
| C.该电池工作时通甲烷一极附近溶液的pH 升高 |
| D.在标准状况下通入5.6 L O2完全反应,则有1 mol电子发生转移 |
2009年8月15日,陕西省凤翔县政府新闻发布会宣布,东岭冶炼公司是导致凤翔县长青镇部分儿童血铅超标的主要原因。血铅超标,可致免疫力低下、学习困难、智商水平下降等症状。下列关于铅的说法正确的是 ( )
| A.铅位于周期表中的第7周期、ⅣA |
| B.二氧化碳?二氧化铅均有很强的氧化性 |
| C.与铅同主族的单质均能导电 |
| D.在铅蓄电池中,负极电极方程式为:Pb + SO42--2e- =PbSO4 |
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为:3Zn +2K2FeO4 +8H2O 3Zn(OH)2 +2Fe(OH)3 + 4KOH,下列叙述不正确的是( )
3Zn(OH)2 +2Fe(OH)3 + 4KOH,下列叙述不正确的是( )
| A.放电时负极反应为:Zn – 2e- + 2OH- = Zn(OH)2 |
| B.充电时阴极反应为:Fe(OH)3 - 3e- + 5OH- = FeO42- + 4H2O |
| C.放电时每转移3mol电子,正极有1mol K2FeO4被氧化 |
D.放电时正极附近溶液的碱性增强 |
下图是日常生活中常见电动自行车主要部件之铅蓄电池结构示意图,有关说法不正确的是
| A.铅蓄电池属于二次电池 | B.实际使用过程中可以无限次充放电 |
| C.使用过程中负极发生氧化反应 | D.铅蓄电池体积大有污染还不是最理想的电池 |
试题篮
()