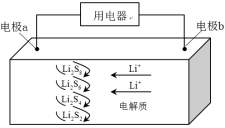
全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极a常用掺有石墨烯的 材料,电池反应为: 。下列说法错误的是( )
| A. |
电池工作时,正极可发生反应: |
| B. |
电池工作时,外电路中流过 电子,负极材料减重 |
| C. |
石墨烯的作用主要是提高电极a的导电性 |
| D. |
电池充电时间越长,电池中 的量越多 |
近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也随之迅速增长。因此,将氯化氢转化为氯气的技术成为科学研究的热点。回答下列问题:
(1)Deacon发明的直接氧化法为: 。下图为刚性容器中,进料浓度比 c(HCl) ∶ 分别等于1∶1、4∶1、7∶1时HCl平衡转化率随温度变化的关系:
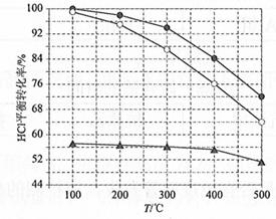
可知反应平衡常数 K(300℃)________ K(400℃)(填"大于"或"小于")。设HCl初始浓度为 , 根据进料浓度比 c(HCl)∶ c(O 2)=1∶1的数据计算 K(400℃)=________(列出计算式)。按化学计量比进料可以保持反应物高转化率,同时降低产物分离的能耗。进料浓度比 c(HCl)∶ 过低、过高的不利影响分别是________。
(2)Deacon直接氧化法可按下列催化过程进行:
Δ
Δ
Δ
则 的 Δ H=________ 。
(3)在一定温度的条件下,进一步提高HCl的转化率的方法是________。(写出2种)
(4)在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺方案,主要包括电化学过程和化学过程,如下图所示:
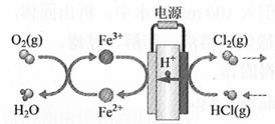
负极区发生的反应有________(写反应方程式)。电路中转移1 mol电子,需消耗氧气________L(标准状况)
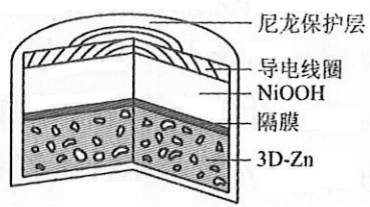
为提升电池循环效率和稳定性,科学家近期利用三维多孔海绵状Zn(3D−Zn)可以高效沉积ZnO的特点,设计了采用强碱性电解质的3D−Zn-NiOOH二次电池,结构如下图所示。电池反应为
。下列说法错误的是( )
| A. |
三维多孔海绵状Zn具有较高的表面积,所沉积的ZnO分散度高 |
| B. |
充电时阳极反应为 |
| C. |
放电时负极反应为 |
| D. |
放电过程中 通过隔膜从负极区移向正极区 |
一种可充电锂-空气电池如图所示。当电池放电时,
与
在多孔碳材料电极处生成
。下列说法正确的是( )
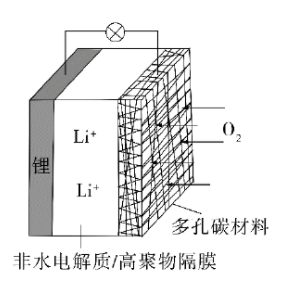
| A. | 放电时,多孔碳材料电极为负极 |
B. | 放电时,外电路电子由多孔碳材料电极流向锂电极 |
| C. | 充电时,电解质溶液中 向多孔碳材料区迁移 |
D. | 充电时,电池总反应为 |
我国科学家研发了一种室温下"可呼吸"的
二次电池,将
溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:
 ,下列说法错误的是()
,下列说法错误的是()
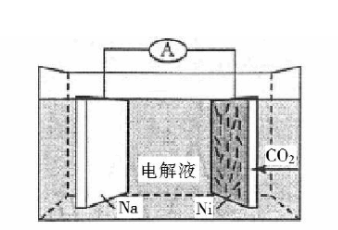
| A. | 放电时, 向负极移动 |
B. | 充电时释放 ,放电时吸收 |
| C. | 放电时,正极反应为: |
D. | 充电时,正极反应为 |
锌﹣空气燃料电池可用作电动车动力电源,电池的电解质溶液为KOH溶液,反应为 。下列说法正确的是( )
| A. |
充电时,电解质溶液中K +向阳极移动 |
| B. |
充电时,电解质溶液中 逐渐减小 |
| C. |
放电时,负极反应为: |
| D. |
放电时,电路中通过2mol电子,消耗氧气22.4L(标准状况) |
利用生物燃料电池原理研究室温下氨的合成,电池工作时
在电极与酶之间传递电子,示意图如下所示。下列说法错误的是( )

A.相比现有工业合成氨,该方法条件温和,同时还可提供电能
B.阴极区,在氢化酶作用下发生反应
C.正极区,固氮酶为催化剂, 发生还原反应生成
D.电池工作时质子通过交换膜由负极区向正极区移动
某燃料电池主要构成要素如图所示,下列说法正确的是( )

A.电池可用于乙醛的制备
B.b电极为正极
C.电池工作时,a电极附近pH降低
D.a电极的反应式为O 2+4e ﹣﹣4H +═2H 2O
圣路易斯大学研制的新型乙醇燃料电池,用能传递质子(H+)的介质作溶剂,反应为C2H5OH+3O2→2CO2+3H2O,如图是该电池的示意图,下列说法正确的是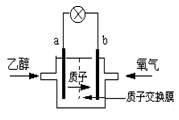
| A.a极为电池的正极 |
| B.电池正极的电极反应为4H++O2+4e-=2H2O |
| C.电池工作时电流由a极沿导线经灯泡再到b极 |
| D.电池工作时,1mol乙醇被氧化时就有6mol电子转移 |
锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:
Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s) 下列说法错误的是
| A.电池工作时,锌失去电子,电解液内部OH-向负极移动 |
| B.电池正极的电极反应式为:2MnO2(s)+H2O(1)+2e-=Mn2O3(s)+2OH-(aq) |
| C.电池工作时,电子由正极通过外电路流向负极 |
| D.外电路中每通过0.2mol电子,锌的质量理论上减小6.5g |
通过NOx传感器可监测NOx的含量,其工作原理示意图如下,下列说法不正确的是
| A.Pt电极是该装置的正极 |
| B.正极的电极反应式:O2 + 4e−+ 2H2O=4OH− |
| C.负极的电极反应式:NO−2e−+O2−=NO2 |
| D.固体电解质中O2−向负极移动 |
铅蓄电池是典型的可充电电池,在现代生活中有着广泛的应用,其充电、放电按下式进行: Pb+PbO2+2H2SO4  2PbSO4+2H2O, 有关该电池的说法正确的
2PbSO4+2H2O, 有关该电池的说法正确的
| A.放电时,电解质溶液的pH不断降低且正负极均有PbSO4生成 |
| B.放电时,每通过1mol电子,蓄电池就要消耗2mol H2SO4 |
| C.充电时,阳极反应:PbSO4 +2e- = Pb + SO42- |
| D.充电时,铅蓄电池的负极与外接电源的负极相连 |
甲醇可作为燃料电池的原料。以CH4和H2O为原料,通过下列反应来制备甲醇。
I:CH4(g) + H2O (g) =CO(g) + 3H2(g) △H =+206.0 kJ/mol
II:CO (g) + 2H2 (g) = CH3OH (g) △H =—129.0 kJ/mol
(1)CH4(g)与H2O(g)反应生成CH3OH (g)和H2(g)的热化学方程式为_______________。
(2)将1.0 mol CH4和2.0 mol H2O(g)通入容积为100 L的反应室,在一定条件下发生反应I,测得在一定的压强下CH4的转化率与温度的关系如图

假设100 ℃时达到平衡所需的时间为15min,则用H2表示该反应的平均反应速率为_______________。
(3)写出甲醇—空气—KOH溶液的燃料电池负极的电极反应式:______________。
(4)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧化成CO2而净化。实验室用下图装置模拟上述过程:

① 写出阳极电极反应式_______________。
② 写出除去甲醇的离子方程式_________________。
下列叙述错误的是( )
| A.氢氧燃料电池是一种将化学能转化为电能的装置 |
| B.铁船舶的外壳上镶嵌锌块,可避免船体遭受腐蚀 |
| C.钢铁腐蚀时负极的电极反应式:Fe-3e-=Fe3+ |
| D.工业上电解饱和食盐水时阴极的电极反应式:2H++2e-=H2↑ |
如图为某种甲醇燃料电池示意图,工作时电子移动方向如图所示,下列判断正确的是( )

| A.X为氧气 |
| B.电极A反应式:CH3OH-6e-+H2O=CO2+6H+ |
| C.B电极附近溶液pH增大 |
| D.电极材料活泼性:A>B |
试题篮
()