锌银电池的负极是Zn,正极是Ag2O,以苛性钠溶液为电解质,电池放电时的总反应为Zn+Ag2O+H2O==Zn(OH)2 + 2Ag,下列判断正确的是( )
| A.放电时,OH-向负极方向移动 |
| B.放电时,正极反应式为Zn+2OH--2e-===ZnO+H2O |
| C.充电时,Zn发生氧化反应 |
| D.充电时, 阴极附近PH 减小 |
用碱性氢氧燃料电池为电源进行电解的实验装置图如图所示,下列说法中正确的是( )

A.燃料电池工作时,正极反应为:O2+2H2O+4e- 4OH- 4OH- |
| B.a极是碳,b极是铜时,b极逐渐溶解,a极上有铜析出 |
| C.CuSO4溶液电解结束后溶液呈中性 |
| D.a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
2010年4月中旬全球核安全峰会在华盛顿举行,发展核电、制裁核武器发展是会议主题,各式各样电池的发展是化学对人类的一项重大贡献,下列有关电池的叙述正确的是
| A.手机上用的锂离子电池属于一次电池 |
| B.锌锰干电池中,锌电极是负极 |
| C.氢氧燃料电池工作时氢气在负极被还原 |
| D.太阳能电池的主要材料为二氧化硅 |
纽扣电池的两极材料分别为锌和氧化银,电解质溶液为KOH溶液.放电时两个电极反应分别为:Z n+2OH﹣→Zn(OH)2+2e﹣Ag2O+H2O+2e﹣→2Ag+2OH﹣下列说法正确的是( )
| A.溶液中OH﹣向正极移动,K+、H+向负极移动 |
| B.锌发生还原方应,氧化银发生还原反应 |
| C.锌是负极,氧化银是正极 |
| D.在电池放电过程中,电解质溶液的酸碱性基本保持不变 |
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)==Zn(OH)2(s)+Mn2O3(s)。下列说法错误的是
| A.电池工作时,锌失去电子 |
| B.电池正极的电极反应式为:2MnO2(s)+H2O(1)+2e—=Mn2O3(s)+2OH-(aq) |
| C.电池工作时,电子由正极通过外电路流向负极 |
| D.外电路中每通过0.2mol电子,锌的质量理论上减小6.5g |
圣路易斯大学研制的新型乙醇燃料电池,用能传递质子(H+)的介质作溶剂,反应为C2H5OH+3O2→2CO2+3H2O,如图是该电池的示意图,下列说法正确的是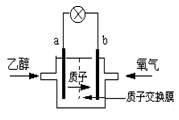
| A.a极为电池的正极 |
| B.电池正极的电极反应为4H++O2+4e-=2H2O |
| C.电池工作时电流由a极沿导线经灯泡再到b极 |
| D.电池工作时,1mol乙醇被氧化时就有6mol电子转移 |
某同学按如下图所示的装置进行实验。A、B为两种中学常见金属,它们的硫酸盐可溶于水,当S闭合时,在交换膜处SO从右向左移动。下列说法错误的是( )

A.电解一段时间后,向Ⅱ装置通入适量的HCl气体可以恢复原来的浓度
B.反应初期,Y电极周围出现白色沉淀
C.B电极质量增加
D.X电极产生气泡,且生成1mol气体的同时,有1molA参与反应
下列措施有利于节能减排、改善环境质量的是
①研制开发新型燃料电池汽车,减少机动车尾气污染
②开发推广太阳能、水能、风能等能源
③使用填埋法处理未经分类的生活垃圾
④推广使用燃煤脱硫技术,防治SO2污染
| A.①②④ | B.①② | C.①②③④ | D.③④ |
氢氧燃料电池是一种能在航天飞机上使用的特殊电池,其反应原理示意图如图。下列有关氢氧燃料电池的说法不正确的是
A.由于A、B两电极没有活动性差别,不能构成原电池
B.A电极是负极,电极上发生氧化反应
C.产物为无污染的水,属于环境友好的绿色电池
D.外电路中电流由B电极通过导线流向A电极
航天器中常使用可充电电池,构造示意图如图(氢化物电极为储氢金属,可看做H2直接参加反应)。白天太阳能帆板发电,将一部分电量储存在镍氢电池里,夜晚镍氢电池供电。下列说法正确的是( )
| A.在使用过程中此电池要不断补充水 |
| B.放电时NiOOH在电极上发生氧化反应 |
| C.充电时阴极区电解质溶液pH升高 |
| D.充电时阴极反应为Ni(OH)2-e-+OH-= NiOOH+H2O |
锂离子电池已经成为应用最广泛的可充电电池。某种锂离子电池的结构示意图如图,其中两极区间的隔膜只允许Li+通过。电池充电时的总反应化学方程式为:
LiCoO2===Li1-xCoO2+xLi。关于该电池的推论错误的是( )。
A.放电时,Li+主要从负极区通过隔膜移向正极区
B.放电时,负极反应xLi-xe-===xLi+
C.充电时,将电能转化为化学能
D.充电时,负极(C)上锂元素被氧化
研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,下列“水”电池在海水中放电时的有关说法正确的是( )
| A.正极反应式:Ag+Cl﹣﹣e﹣=AgCl |
| B.每生成1mol Na2Mn5O10转移2mol电子 |
| C.Na+不断向“水”电池的负极移动 |
| D.AgCl是还原产物 |
下列叙述错误的是( )
| A.氢氧燃料电池是一种将化学能转化为电能的装置 |
| B.铁船舶的外壳上镶嵌锌块,可避免船体遭受腐蚀 |
| C.钢铁腐蚀时负极的电极反应式:Fe-3e-=Fe3+ |
| D.工业上电解饱和食盐水时阴极的电极反应式:2H++2e-=H2↑ |
LiAl/FeS电池是一种正在开发的车载电池,该电池中正极的电极反应式为:
2Li++FeS+2e-→Li2S+Fe ,有关该电池的下列说法中,正确的是( )
| A.负极的电极反应式为Al-3e-―→Al3+ |
| B.该电池的总反应式为2Li+FeS===Li2S+Fe |
| C.LiAl在电池中作为负极材料,该材料中Li的化合价为+1 |
| D.充电时,阴极发生的电极反应式为Li2S+Fe-2e-===2Li++FeS |
近几年科学家发明的一种新型可控电池——锂水电池,工作原理如图所示。下列有关说法正确的是
| A.碳极发生的反应是:2H2O+O2+4e-=4OH- |
| B.有机电解质通过固体电解质可进入水溶液中 |
| C.理论上,外电路中每转移1mol电子,负极消耗的质量为7g |
| D.该电池如可以充电,充电时碳极接外加电源的负极,锂极接外加电池的正极 |
试题篮
()