钠氯化镍蓄电池是一种新型的电动汽车蓄电池,其正极MCl2中的M代表Ni、Fe、Ca、Cr、Mn、Cu等一系列金属,其中NiCl2的效果最好。而负极的活性物质是液态金属钠。正、负极活性物质被一种只允许Na+迁移的β-Al2O3固体电解质陶瓷管分隔,由于正极是固态多孔金属氧化物,所以还需要添加NaAlCl4熔盐在正极处作第二电解质,在正、负极之间传导钠离子。下列有关钠氯化镍蓄电池的说法错误的是
| A.电池放电时的总反应为2Na+NiCl2===Ni+2NaCl |
| B.充电时阳极的电极反应为Na++e-===Na |
| C.放电时正极的电极反应为Ni2++2e-===Ni |
| D.该电池被称为绿色电池,最大原因是从废弃电池中可以方便地回收较纯的镍,其他产物对环境没有影响 |
用铂作电极电解1L含有0.4molCuSO4和0.2molNaCl的水溶液,一段时间后在一个电极上得到了19.2 g Cu,在另一极上析出的气体在标况下的体积是
| A.4.48 L | B.5.6 L | C.6.72 L | D.13.44 L |
被称之为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰。在纸内的离子“流过”水和氧化锌组成的电解液。电池总反应为:
Zn + 2 MnO2 + H2O ="=" ZnO + 2MnO (OH)。下列说法正确的是
| A.该电池的正极为锌 |
| B.该电池反应中二氧化锰起催化剂作用 |
| C.当 0.l mol Zn 完全溶解时,流经电解液的电子个数为 1.204×l023 |
| D.电池正极反应式为: 2MnO2 + 2e -+2H2O ="=2MnO" (OH)+2OH- |
下列关于铜锌原电池(稀硫酸作电解质溶液)的叙述错误的是
| A.电子由正极通过导线流向负极 | B.负极反应式为:Zn-2e-=Zn2+ |
| C.正极产生1molH2电池转移2mol电子 | D.可以用碳棒代替铜片作为正极 |
当电解质溶液为氢氧化钾水溶液的氢氧燃料电池电解饱和碳酸钠溶液一段时间,假设电解时温度不变且用惰性电极,下列说法正确的是( )
| A.当电池负极消耗m g气体时,电解池阳极同时有m g气体生成 |
| B.电池的负极反应式为:O2+2H2O+4e-=4OH- |
| C.电解后c(Na2CO3)不变,且溶液中有晶体析出 |
| D.燃料电池中c(KOH)不变;电解池中溶液pH变大 |
干电池的负极反应是:Zn –2e = Zn 2+,现以干电池作电源电解32.4g 34%的硝酸钾溶液,一段时间后,测得溶液中溶质的质量分数为36%,则干电池中消耗锌的物质的量为
| A.0.3mol | B.0.05mol | C.0.2mol | D.0.1mol |
获得“863”计划支持的环境友好型铝碘电池已研制成功,电解质溶液为AlI3溶液,电池总反应式为2Al+3I2=2AlI3。下列说法不正确的是
| A.该电池负极的电极反应为:Al–3e-=Al3+ |
| B.电池工作时,溶液中铝离子向正极移动 |
| C.消耗相同质量金属时,用锂作负极产生电子的物质的量比用铝时多 |
| D.当导线中有3.612×1024个电子通过时,电池负极质量减少27 g |
有关下图装置中的叙述正确的是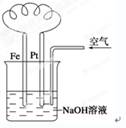
| A.这是电解NaOH溶液的装置 |
| B.溶液中发生了变化:4Fe(OH)2+O2+2H2O===4Fe(OH)3 |
| C.Fe为正极,电极反应为:Fe-2e-+2OH-=Fe(OH)2 |
| D.NaOH溶液的碱性逐渐减弱 |
将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿棕色铁锈环(b),如图所示。导致该现象的主要原因是液滴之下氧气含量比边缘少。下列说法正确的是
| A.液滴中的Cl―由a区向b区迁移 |
B.液滴边缘是正极区,发生的电极反应为:O2+2H2O+4e- 4OH- 4OH- |
| C.液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH―形成Fe(OH)2,进一步氧化、脱水形成铁锈 |
| D.若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为Cu-2e-=Cu2+ |
如右图所示,在一U型管中装入含有紫色石蕊的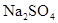 试液,通直流电,一段时间后U型管内会形成一个倒立的三色 “彩虹”,从左到右颜色的次序是( )
试液,通直流电,一段时间后U型管内会形成一个倒立的三色 “彩虹”,从左到右颜色的次序是( )
| A.蓝、紫、红 | B.红、蓝、紫 |
| C.红、紫、蓝 | D.紫、红、蓝 |
为体现“城市让生活更美好”的主题,上海市政府承诺世博园区内交通“零排放”、园区周边交通“低排放”。2010年4月15日新能源车交车仪式在世博园举行,该车装着“绿色心脏”——质子交换膜燃料电池,其工作原理如图所示,下列叙述正确的是( )
| A.通入氧气的电极发生氧化反应 |
| B.通入氢气的电极为正极 |
C.总反应式为O2+2H2 2H2O 2H2O |
| D.正极的电极反应式为O2+4H++4e-===2H2O |
电池是人类生产和生活中的重要能量来源,各式各样电池的发明是化学对人类的一项重大贡献。下列有关电池的叙述正确的是( )
| A.锌锰干电池工作一段时间后碳棒变细 |
| B.氢氧燃料电池可将热能直接转变为电能 |
| C.氢氧燃料电池工作时氢气在负极被氧化 |
| D.太阳能电池的主要材料是高纯度的二氧化硅 |
下列几种化学电池中,不属于可充电电池的是
| A.碱性锌锰电池 | B.手机用锂电池 |
| C.汽车用铅蓄电池 | D.玩具用镍氢电池 |
电池是人类生产和生活中的重要能量来源,各式各样电池的发展是化学对人类的一项重大贡献。下列有关电池的叙述正确的是
| A.锌锰干电池工作一段时间后碳棒变细 |
| B.氢氧燃料电池可将热能直接转变为电能 |
| C.在现实生活中,电化学腐蚀要比化学腐蚀严重的多,危害更大 |
| D.太阳能电池的主要材料是高纯度的二氧化硅 |
试题篮
()