获得“863”计划和中科院“百人计划”支持的环境友好型铝碘电池已研制成功,电解质为AlI3溶液,已知电池的总方程式为2Al+3I2===2AlI3。下列说法不正确的是
| A.该电池负极的电极方程式为Al-3e-===Al3+ |
| B.电池工作时,溶液中铝离子向正极移动 |
| C.消耗相同质量金属时,用锂作负极时,产生电子的物质的量比铝多 |
| D.该电池可能是一种可充电的二次电池 |
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,其负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示。下列说法正确的是
| A.电池放电时Na+从a极区移向b极区 |
| B.每消耗3 mol H2O2,转移的电子为3 mol |
| C.电极a采用MnO2,MnO2既作电极材料又有催化作用 |
D.该电池的负极反应为   |
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:CH3CH2OH–4e- + H2O = CH3COOH + 4H+。下列有关说法正确的是
| A.检测时,电解质溶液中的H+向负极移动 |
| B.若有0.4mol电子转移,则在标准状况下消耗4.48L氧气 |
| C.电池反应的化学方程式为:CH3CH2OH + O2 = CH3COOH + H2O |
| D.正极上发生的反应为:O2 + 4e- + 2H2O = 4OH- |
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。RFC的工作原理如图所示。下列有关说法正确的是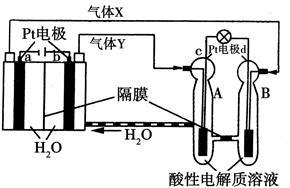
A.当有0.1 mol电子转移时,a电极产生2.24 L H2
B.b电极上发生的电极反应式为4H2O+4e-===2H2↑+4OH-
C.c电极上进行还原反应,B池中的H+可以通过隔膜进入A池
D.d电极上发生的电极反应式为O2+4H++4e-===2H2O
据报道,最近苹果公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。其电池反应为:2CH3OH + 3O2 + 4OH— =2CO32— + 6H2O,则下列说法错误的是
| A.放电时CH3OH参与反应的电极为正极 |
| B.充电时电解质溶液的pH逐渐增大 |
| C.放电时负极的电极反应为:CH3OH-6e-+8OH- = CO32— + 6H2O |
| D.充电时每生成1 mol CH3OH转移6 mol电子 |
下列说法正确的是
| A.氢氧燃料电池的能量转换形式之一为化学能转化为电能 |
| B.铅蓄电池放电时的负极和充电时的阴极均发生氧化反应 |
| C.电解精炼铜过程中,阳极质量的减少与阴极质量的增加一定相等 |
| D.催化剂通过降低化学反应的焓变加快化学反应速率 |
大功率镍氢动力电池及其管理模块,是国家“十五”863计划电动汽车专项中一项重要课题。我国镍氢电池居世界先进水平,解放军潜艇将装备国产大功率镍氢动力电池。常见镍氢电池的某极是储氢合金LaNi5H6(LaNi5H6中各元素化合价均为零),电池反应通常表示为:LaNi5H6+6NiO(OH) LaNi5+6Ni(OH)2,下列有关镍氢电池的说法,不正确的是
LaNi5+6Ni(OH)2,下列有关镍氢电池的说法,不正确的是
| A.电池工作时,储氢合金作负极 |
| B.电池充电时,阳极发生氧化反应 |
| C.电池工作时,负极反应式:LaNi5H6 + 6OH-−6e- ="=" LaNi5 + 6H2O |
| D.电池放电时,电子由正极通过外电路流向负极 |
我国知名企业比亚迪公司开发了具有多项专利的锂钒氧化物二次电池,其成本较低,对环境无污染,能量密度远远高于其他电池,电池总反应为V2O5 + xLi 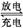 LixV2O5。下列说法合理的是
LixV2O5。下列说法合理的是
| A.电池在放电时,Li+向负极移动 |
| B.锂在放电时作正极,充电时作阳极 |
| C.该电池充电时阳极的反应为LixV2O5 _ xe-=V2O5 + xLi+ |
| D.V2O5只是锂发生反应的载体,不参与电池反应 |
镁及其化合物一般无毒(或低毒)、无污染,且镁电池放电时电压高而平稳,越来越成为人们研制绿色原电池的关注焦点。其中一种镁电池的反应为:xMg+Mo3S4 MgxMo3S4,下列说法正确的是
MgxMo3S4,下列说法正确的是
| A.电池放电时,Mg2+向负极迁移 |
| B.电池放电时,正极反应为Mo3S4+2xe-+xMg2+=MgxMo3S4 |
| C.电池充电时,阴极发生还原反应生成Mo3S4 |
| D.电池充电时,阳极反应为xMg﹣2xe-=xMg2+ |
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O Cd(OH)2 +2Ni(OH)2
Cd(OH)2 +2Ni(OH)2
有关该电池的说法正确的是
| A.充电时阳极反应:Ni(OH)2-e— + OH- ="=" NiOOH + H2O |
| B.充电过程是化学能转化为电能的过程 |
| C.放电时负极附近溶液的碱性不变 |
| D.放电时电解质溶液中的OH- 向正极移动 |
铅蓄电池是最常见的二次电池,其电池总反应可以表示为:
Pb(s)+PbO2(s)+2H2SO4(aq)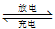 2PbSO4(s)+2H2O(l),下列说法不正确的是
2PbSO4(s)+2H2O(l),下列说法不正确的是
| A.电池的电解液为酸性溶液,正极为PbO2、负极为Pb |
| B.电池放电时,正极反应为PbO2+2 e-+SO42-+4H+=PbSO4+2H2O |
| C.电池充电过程中,阳极附近溶液的pH升高 |
| D.电池充电时,阴极反应为PbSO4+2e-=Pb+SO42- |
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O Cd(OH)2 + 2Ni(OH)2 有关该电池说法正确是
Cd(OH)2 + 2Ni(OH)2 有关该电池说法正确是
| A.充电时阳极反应:Ni(OH)2-e- + OH- ="NiOOH" + H2O |
| B.充电过程是化学能转化为电能的过程 |
| C.放电时负极附近溶液的碱性不变 |
| D.放电时电解质溶液中的OH-向正极移动 |
下列有关电池的说法不正确的是
| A.手机上用的锂离子电池属于二次电池 |
| B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极 |
| C.甲醇燃料电池可把化学能转化为电能 |
| D.锌锰干电池中,锌电极是负极 |
碱性电池具有容量大,放电电流大的特点,因而得到广泛应用。锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应为:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s)。下列说法错误的是
| A.电池工作时,锌失去电子 |
| B.电池正极的电极反应式为2MnO2(s)+H2O(l)+2e- = Mn2O3(s)+2OH-(aq) |
| C.电池工作时,电子由正极通过外电路流向负极 |
| D.外电路中每通过0.2mol电子,锌的质量理论上减少6.5g |
试题篮
()