“天宫一号”的供电系统(RFC)是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池。右图为RFC工作原理示意图,有关说法正确的是
A.当有0.1 mol电子转移时,a电极产生1.12 L H2
B.b极上发生的电极反应是:4H2O+4e-===2H2↑+4OH-
C.d极上发生的电极反应是:O2+4H++4e-===2H2O
D.c极上发生还原反应,B中的H+通过隔膜进入A
正、负极都是碳材料的双碳性电池,电池充、放电过程为2nC+LiA CnA+LiCn,充电时Li+、A-分别吸附在两极上形成LiCn和CnA(如图所示),下列说法正确的是
CnA+LiCn,充电时Li+、A-分别吸附在两极上形成LiCn和CnA(如图所示),下列说法正确的是
| A.a是电池的负极 |
| B.放电时,A-离子向b极移动 |
| C.放电时,负极的电极反应式是nC-e-+A-= CnA |
| D.充电时,电解质中的离子浓度保持不变 |
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:CH3CH2OH-4e-+H2O=CH3COOH+4H+。下列有关说法正确的是( )
| A.检测时,电解质溶液中的H+向负极移动 |
| B.若有0.4 mol电子转移,则在标准状况下消耗4.48L氧气 |
| C.电池反应的化学方程式为:CH3CH2OH+O2=CH3COOH+H2O |
| D.正极上发生的反应为:O2+4e-+2H2O=4OH- |
已知某镍镉(Ni—Cd)电池的电解质溶液为KOH溶液,其放电按下式进行:
Cd+2NiOOH+2H2O=Cd(OH)2+2Ni(OH)2。有关该电池的说法正确的是( )
| A.充电时阳极反应:NiOOH+H2O+e-===Ni(OH)2+OH- |
| B.充电过程是电能转化为化学能的过程 |
| C.放电时负极附近溶液的碱性不变 |
| D.放电时电解质溶液中的OH-向正极移动 |
如图甲池和乙池中的四个电极都是惰性材料,请根据图示判断下列说法正确的是
| A.两个装置之间没有盐桥,故不能形成电流 |
| B.a电极的电极反应式 C2H5OH+16OH--12e-==2CO32-+11H2O |
| C.一段时间后,乙池d电极周围的溶液呈现棕褐色 |
| D.乙池在反应前后溶液的pH不变 |
如图装置(Ⅰ)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池放电时的化学方程式为:2K2S2 +KI3=K2S4 +3KI。装置(Ⅱ)为电解含有0.5mol NaCl的溶液示意图,当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法正确的是
| A.K+从右到左通过离子交换膜 |
| B.电极A上发生的反应为:3I-﹣2e-=I3- |
| C.电极X上发生的反应为:2Cl-﹣2e-=Cl2↑ |
| D.当有0.1 mol K+通过离子交换膜,X电极上产生1.12 L(标准状况)气体 |
利用如图所示原电池可测量空气中Cl2含量,其中电解质是Ag+可以自由移动的固体物质。
下列分析不正确的是( )
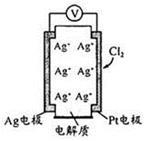
| A.电子经外电路流向Pt电极 |
| B.电池工作时,电解质中Ag+数目减少 |
| C.正极反应:Cl2+2e—+2Ag+ = 2AgCl |
| D.空气中c(Cl2)越大,Ag极消耗速率越快 |
RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池,RFC工作原理见图。下列有关说法正确的是
| A.转移0.1mol电子时,a电极产生标准状况下O2 1.12L |
| B.b电极上发生的电极反应是:2H2O+2e-=H2↑+2OH- |
| C.c电极上进行还原反应,B池中的H+可以通过隔膜进入A池 |
| D.d电极上发生的电极反应是:O2+4H++4e-=2H2O |
微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如下图所示。下列有关说法错误的是
| A.正极反应中有CO2生成 |
| B.微生物促进了反应中电子的转移 |
| C.质子通过交换膜从负极区移向正极区 |
| D.电池总反应为C6H12O6+6O2=6CO2+6H2O |
人工光合作用能够借助太阳能,用CO2和H2O制备化学原料。科学家用氮化镓材料与铜组装如图的人工光合系统,成功地实现了以CO2和H2O合成CH4,下列说法不正确的是
| A.该过程是将太阳能转化为化学能的过程 |
| B.GaN表面发生氧化反应,有O2产生 |
| C.电解液中的H+从质子交换膜右侧向左侧迁移 |
| D.Cu表面的电极反应式CO2+8e-+8H+=CH4+2H2O |
某同学按如下图所示的装置进行实验。A、B为两种中学常见金属,它们的硫酸盐可溶于水,当S闭合时,在交换膜处SO从右向左移动。下列说法错误的是( )

A.电解一段时间后,向Ⅱ装置通入适量的HCl气体可以恢复原来的浓度
B.反应初期,Y电极周围出现白色沉淀
C.B电极质量增加
D.X电极产生气泡,且生成1mol气体的同时,有1molA参与反应
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O Cd(OH)2 + 2Ni(OH)2有关该电池的说法正确的是
Cd(OH)2 + 2Ni(OH)2有关该电池的说法正确的是
| A.充电时阳极反应:Ni(OH)2-e-+ OH- =" NiOOH" + H2O |
| B.充电过程是化学能转化为电能的过程 |
| C.放电时负极附近溶液的碱性不变 |
| D.放电时电解质溶液中的OH-向正极移动 |
人工光合作用能够借助太阳能,用CO2和H2O来制备化学原料。下图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是 
| A.该过程是将太阳能转化为化学能的过程 |
| B.催化剂a表面发生氧化反应,有O2产生 |
| C.催化剂a附近酸性减弱,催化剂b附近酸性增强 |
| D.催化剂b表面的反应是CO2 +2H++2e一=HCOOH |
液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点。一种以肼( N2H4)为燃料的电池装置如图所示。该电池用空气中的氧气作为氧化剂,KOH作为电解质。下列关于该燃料电池的叙述不正确的是
| A.电流从右侧电极经过负载后流向左侧电极 |
| B.负极发生的电极反应式为:N2H4+4OH- - 4e-=N2+ 4H2O |
| C.该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触 |
| D.该燃料电池持续放电时.K+从负极向正极迁移,因而离子交换膜需选用阳离子交换膜 |
试题篮
()