在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液。当溶液中的Ba2+恰好完全沉淀时,溶液pH=11。若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积比是
| A.1∶9 | B.1∶1 | C.1∶2 | D.1∶4 |
常温下,向0.1 mol/L的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验时不同阶段的溶液,下列有关说法中不正确的是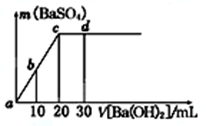
| A.溶液的pH:a<b<c<d |
| B.溶液的导电能力:a>b>d>c |
| C.c、d溶液呈碱性 |
| D.a、b溶液呈酸性 |
用0.1 mol/L NaOH溶液滴定0.1 mol/L盐酸,如达到滴定终点时不慎多加1滴NaOH溶液(1滴溶液体积约为0.05 mL),继续加水至50 mL,所得溶液的pH是
| A.4 | B.7.2 | C.10 | D.11.3 |
常温下,pH=13的强碱溶液和pH=2的强酸溶液混合,所得溶液的pH=11,则强碱溶液和强酸溶液的体积之比为
| A.11:1 | B.9:1 | C.1:11 | D.1:9 |
下列叙述正确的是( )。
| A.任何浓度的溶液都可以用pH来表示其酸性的强弱 |
| B.c(H+)=1×10-7 mol·L-1的溶液一定是中性溶液 |
| C.0.2 mol·L-1 CH3COOH溶液中的c(H+)是0.1 mol·L-1 CH3COOH溶液中的c(H+)的2倍 |
| D.无论是纯水,还是酸性、碱性或中性稀溶液,在常温下,其c(H+)·c(OH-)都是定值。 |
某学生用0.1 mol·L-1的KOH标准溶液滴定未知浓度的盐酸,其操作分解为如下几步:
| A.移取20 mL待测盐酸注入洁净的锥形瓶,并加入2~3滴酚酞 |
| B.用标准溶液润洗滴定管2~3次 |
| C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液 |
| D.取标准KOH溶液注入碱式滴定管至“0”刻度以上1~2 cm |
E.调节液面至“0”或“0”以下某一刻度,记下读数
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写)__________________;
(2)上述B步骤操作的目的是_______________________;
(3)上述A步骤操作之前,先用待测液润洗锥形瓶,则对滴定结果的影响是______________;
(4)判断到达滴定终点的实验现象是______________________;
(5)若滴定时在晃动锥形瓶的过程中不小心将液体洒出,对实验结果的影响是_______;
(6)若称取一定量的KOH固体(含少量NaOH)配制标准溶液并用来滴定上述盐酸,则对滴定结果产生的影响是__________________________________。
常温下有浓度均为0.5 mol/L的四种溶液:
①Na2CO3、②NaHCO3、③HCl、④NH3·H2O
(1)上述溶液中,可发生水解的是______(填序号,下同)。
(2)上述溶液中,既能与氢氧化钠反应,又能和硫酸反应的溶液中离子浓度由大到小的顺序为:____________________________________。
(3)向④中加入少量氯化铵固体,此时c(NH4+)/c(OH-)的值_____(填“增大”、“减小”、或“不变”)。
(4)若将③和④的溶液混合后溶液恰好呈中性,则混合前③的体积________④的体积(填“大于”、“小于”或“等于”),此时溶液中离子浓度由大到小的顺序是________________________。
(5)取10 mL溶液③,加水稀释到500 mL,则此时溶液中由水电离出的c(H+)=________。
在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:
(1)当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是________。
(2)同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是________。
(3)若三者c(H+)相同时,物质的量浓度由大到小的顺序是______________________________。
(4)将c(H+)相同的这三种酸均加水稀释至原来的100倍后,c(H+)由大到小的顺序是________。
(5)在不同温度下的水溶液中c(H+)=10x mol/L,c(OH-)=10y mol/L,x与y的关系如下图所示。请回答下列问题:
①曲线Ⅰ代表的温度下,水的离子积为_____,曲线Ⅰ所代表的温度_____(填“高于”“低于”或“等于”)曲线Ⅱ所代表的温度。你判断的依据是_________________________。
②曲线Ⅰ所代表的温度下,0.01 mol/L的NaOH溶液的pH为________。
如图曲线a和b是盐酸与氢氧化钠溶液相互滴定的滴定曲线,下列叙述正确的是 ( )

| A.盐酸的物质的量浓度为1 mol·L-1 | B.P点时恰好完全中和,溶液呈中性 |
| C.曲线a是盐酸滴定氢氧化钠溶液的滴定曲线 | D.酚酞不能用作本实验的指示剂 |
下列说法错误的( )
| A.0.1 mol·L-1的CH3COOH溶液中,由水电离的c(H+)为10-13mol·L-1 |
| B.pH=2与pH=1的CH3COOH溶液中c(H+)之比为1∶10 |
| C.等体积pH=12的NaOH溶液和pH=2的CH3COOH溶液混合,混合后溶液pH<7 |
| D.1 mol甲烷分子中含有共价键的个数为4NA |
有等体积、氢氧根离子浓度相等的Ba(OH)2、NaOH和NH3·H2O三种碱溶液,滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为V1、V2、V3,则三者的大小关系正确的是( )
| A.V3>V2>V1 | B.V3=V2=V1 | C.V3>V2=V1 | D.V1=V2>V3 |
某烧碱溶液中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行以下滴定操作:
| A.在250ml的容量瓶中定容成250ml烧碱溶液; |
| B.用碱式滴定管取25ml烧碱溶液于锥形瓶中并滴加几滴甲基橙指示剂; |
| C.在天平上准确称取烧碱样品Wg,在烧杯中加蒸馏水溶解; |
| D.将物质的量浓度为Mmol/L的标准硫酸溶液装入酸式滴定管,调整液面,记下开始刻读数为V1ml |
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点刻读数为V2 ml
回答下列问题:
①正确的操作步骤的顺序是 → → →D → .
②操作E中在锥形瓶下垫一张白纸的作用 。
③操作D中液面应调整到 ,尖嘴部分应 。
④滴定终点时瓶内溶液的PH约为 ,终点时颜色变化是 。
⑤若酸式滴定管没有用标准硫酸溶液润洗,会对测定结果有何影响? (填偏高、偏低、无影响,其他操作均正确)
⑥该烧碱样品的纯度计算式为 。
要使10ml0.05mol/L的H2SO4溶液PH变为7,应采用的方法是( )
| A.加水稀释到1000ml | B.加入10ml0.1mol/L的氨水 |
| C.加入100ml0.005mol/L的Ba(OH)2溶液 | D.加入100ml0.05mol/L的NaOH溶液 |
若1体积硫酸恰好与10体积PH=11的氢氧化钠溶液完全反应,则二者的物质的量浓度值比应为( )
| A.10:1 | B.5:1 | C.1:1 | D.1:10 |
试题篮
()