在25℃时,有pH为a的HCl溶液和pH为b的NaOH溶液,取VaL该盐酸溶液用该NaOH溶液中和,需VbLNaOH溶液,(题中a≤b,b≥8)。
(1)若a+b=14,则Va/Vb=__________;
(2)若a+b=13,则Va/Vb=__________;
(3)若a+b>14,则Va/Vb=__________,且Va________ Vb(填“>”“<”“=”)。
实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH4++6HCHO═3H++6H2O+(CH2)6N4H+[滴定时,1mol (CH2)6N4H+与1mol H+相当],然后用NaOH标准溶液滴定反应生成的酸.某兴趣小组用甲醛法进行了如下实验:
步骤I:称取样品1.500g.
步骤Ⅱ:将样品溶解后,完全转移到250mL容量瓶中,定容,充分摇匀.
步骤Ⅲ:移取25.00mL样品溶液于250mL锥形瓶中,加入10mL 20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点.按上述操作方法再重复2次.
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数_________(填“偏高”、“偏低”或“无影响”);
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积_________(填“偏高”、“偏低”或“无影响”);
③滴定时边滴边摇动锥形瓶,眼睛应观察_________;
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由_________色;
(2)滴定结果如下表所示:
| 滴定次数 |
待测溶液的体积/mL |
标准溶液的体积 |
|
| 滴定前刻度/mL |
滴定后刻度/mL |
||
| 1 |
25.00 |
1.02 |
21.03 |
| 2 |
25.00 |
2.00 |
21.99 |
| 3 |
25.00 |
0.20 |
20.20 |
若NaOH标准溶液的浓度为0.1010mol•L-1,则该样品中氮的质量分数为_________。
某学生欲用已知物质的量浓度的盐酸来滴定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂。请填写下列空白:
(1)用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视______________________。直到____________ _ 。
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是_______________
| A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液 |
| B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥 |
| C.酸式滴定管在滴定前有气泡,滴定后气泡消失 |
| D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数 |
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,请将数据填入下面表格的空白处。
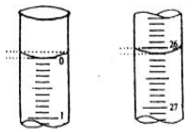
| 滴定次数 |
待测氢氧化钠溶液的体积/mL |
0.1000mol/L盐酸的体积(mL) |
||
| 滴定前刻度 |
滴定后刻度 |
溶液体积/mL |
||
| 第一次 |
25.00 |
|
|
|
| 第二次 |
25.00 |
1.56 |
28.08 |
26.52 |
| 第三次 |
25.00 |
0.22 |
26.34 |
26.12 |
(4)请根据上表中数据列式计算该氢氧化钠溶液的物质的量浓度:c(NaOH)= 。
室温下,用0.100 mol·L-1 NaOH溶液分别滴定20.00ml 0.100 mol·L-1的盐酸和醋酸,滴定曲线如图所示。下列说法正确的是
| A.II表示的是滴定醋酸的曲线 |
| B.pH=7时,滴定醋酸消耗V(NaOH)小于20ml |
| C.V(NaOH) =20.00ml时,两份溶液中c(Cl—)=c(CH3COO—) |
| D.V(NaOH) =10.00ml时,醋酸溶液中:c(Na+)>c(CH3COO—)>c(H+)>c(OH—) |
在T ℃时, Ba(OH)2的稀溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,已知a+b=12。向该溶液中逐滴加入pH=4的盐酸,测得混合溶液的部分pH如下表所示:
| 序号 |
氢氧化钡溶液的体积/mL |
盐酸的体积/mL |
溶液的pH |
| ① |
22.00 |
0.00 |
8 |
| ② |
22.00 |
18.00 |
c |
| ③ |
22.00 |
22.00 |
d |
假设溶液混合前后的体积变化可忽略不计,则下列说法不正确的是
A.a = 8 B.b = 4 C.c = 5 D.d = 6
室温下向10mL0.1 mol•L-1NaOH溶液中加入0.1 mol•L-1的一元酸HA溶液,pH的变化曲线如图所示。下列说法正确的是
A.a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
B.a、b两点所示溶液中水的电离程度相同
C.b点所示溶液中c(A-)>c(HA)
D.滴定过程中不可能出现c(Na+)>c(OH-)>c(A-)>c(H+)
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。下列关于离子共存说法中正确的是( )

| A.d点对应的溶液中大量存在:Na+、K+、ClO-、Cl- |
| B.b点对应的溶液中大量存在:Fe2+、Ba2+、K+、NO3- |
| C.c点对应的溶液中大量存在:Na+、Ba2+、Cl-、Fe3+ |
| D.a点对应的溶液中大量存在:CO32-、Na+、Cl-、SO42- |
现代传感信息技术在化学实验中有广泛的应用。

Ⅰ.某小组用传感技术测定喷泉实验中的压强变化来认识喷泉实验的原理(图1)。
(1)制取氨气。烧瓶中制取NH3的化学方程式为 ,
检验三颈瓶集满NH3的方法是将 靠近瓶口C处,若 ,则证明已收满。
(2)关闭a,将吸有2mL水的胶头滴管塞紧颈口c,打开b,完成喷泉实验,电脑绘制三颈瓶内气压变化曲线(图2)。图2中 点时喷泉最剧烈。
Ⅱ.室温下,测定NH3•H2O的浓度及电离平衡常数Kb
(3)从三颈瓶中用 (填仪器名称)量取25.00mL氨水至锥形瓶中,用0.050 mol•L-1HCl滴定。用pH计采集数据、电脑绘制滴定曲线如下图(已知NH4Cl溶液pH值约为5.5)。
(4)据下图,计算氨水的浓度为 mol•L-1(结果保留两位有效数字);当pH=11.0时,计算NH3•H2O的电离平衡常数Kb的近似值(结果保留两位有效数字,Kb的计算过程在答卷纸相应区域写出)。

(5)关于该滴定实验的说法中,正确的是 。
| A.锥形瓶中有少量蒸馏水不影响测定结果 |
| B.未滴加酸碱指示剂,实验结果不科学 |
| C.酸式滴定管未用盐酸润洗会导致测得氨水的浓度偏高 |
| D.滴定终点时俯视读数会导致测得氨水的浓度偏高 |
化学中常借助曲线图来表示某种变化过程,如有人分别画出了下列的四个曲线图。有关曲线图的说法正确的是
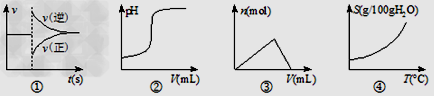
| A.曲线图①可以表示对某化学平衡体系改变温度后反应速率随时间的变化 |
| B.曲线图②可以表示向一定量的盐酸中滴加一定浓度的氢氧化钠溶液时的pH的变化 |
| C.曲线图③可以表示向一定量偏铝酸钠溶液中滴加稀盐酸时产生沉淀的物质的量变化 |
| D.曲线图④可以表示所有的固体物质溶解度和温度的变化 |
25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL浓度均为0.1000mol/L的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法正确的是( )
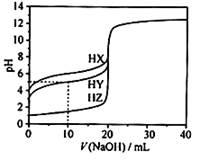
| A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX |
| B.根据滴定曲线,可得Ka(HY)≈10—5 |
| C.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X—)>c(Y—)>c(OH—)>c(H+) |
D.HY与HZ混合,达到平衡时: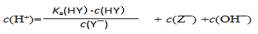 |
某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH=-lgc[OH-])与pH的变化关系如图所示,则
| A.M点所示溶液导电能力强于Q点 |
| B.N点所示溶液中c(CH3COO-)>c(Na+) |
| C.M点和N点所示溶液中水的电离程度相同 |
| D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积 |
室温下,将1.000mol•L-1盐酸滴入20.00mL 1.000mol•L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法正确的是( )

| A.a点由水电离出的c(H+)=1.0×10-14mol•L-1 |
| B.b点:c(NH4+)+c(NH3•H2O)=c(Cl-) |
| C.c点:c(Cl-)=c(NH4+) |
| D.d点后,容易温度略下降的主要原因是NH3•H2O电离吸热 |
常温下,向100ml0.01mol/L的HA溶液中逐滴加入0.02mol/L的MOH溶液,图中所示曲线表示混合溶液的pH的变化情况,下列说法正确的是( )

| A.HA为弱酸 |
| B.在N到K间任意一点对应的溶液中:c(M+)+c(H+)=c(OH-)+c(A-) |
| C.K点对应的溶液中:c(M+)+c(MOH)=c(A-) |
| D.常温下,MA溶液的pH>7 |
一定体积的KMnO4溶液恰好能氧化一定质量的KHC2O4•H2C2O4•2H2O.若用0.10mol•L-1的NaOH溶液中和相同质量的KHC2O4•H2C2O4•2H2O,所需NaOH溶液的体积恰好为KMnO4溶液的3倍,则KMnO4溶液的浓度为( )(提示:①H2C2O4是二元弱酸)
②10[KHC2O4•H2C2O4]+8KMnO4+17H2SO4═8MnSO4+9K2SO4+40CO2↑+32H2O)
| A.0.008889 | B.0.08000 | C.0.1200 | D.0.2400 |
用中和滴定的方法测定NaOH和Na2CO3的混合溶液中NaOH的含量,可先在混合液中加入过量的BaCl2溶液,使Na2CO3完全转变成BaCO3沉淀,然后用标准盐酸滴定(已知几种酸碱指示剂变色的pH范围:①甲基橙3.1~4.4 ②甲基红4.4~6.2 ③酚酞8.2~10)。
(1)滴定时应选用 作指示剂;
(2)判断到达滴定终点的实验现象是 。
(3)下列操作会导致烧碱样品中NaOH含量测定值偏高的是
| A.锥形瓶用蒸馏水洗后未用待测液润洗 | B.酸式滴定管用蒸馏水洗后未用标准液润洗 |
| C.在滴定前有气泡,滴定后气泡消失 | D.滴定前平视读数,滴定结束俯视读数 |
(4)为测定某烧碱样品中NaOH的含量(设样品中杂质为Na2CO3),某同学进行如下实验:准确称取5.0g样品配制成250mL溶液,然后分三次各取配制好的烧碱溶液20.00mL于三个用蒸馏水洗净的锥形瓶中,分别加入过量的BaCl2溶液,并向锥形瓶中各加入1~2滴指示剂,用浓度为0.2000mol·L-1的盐酸标准液进行滴定,相关数据记录如下:
| 实验编号 |
V(烧碱溶液)/mL |
V(HCl)/mL |
|
| 初读数 |
末读数 |
||
| 1 |
20.00 |
0.80 |
21.00 |
| 2 |
20.00 |
1.00 |
20.80 |
| 3 |
20.00 |
0.20 |
22.80 |
依据表中数据,计算出烧碱样品中含NaOH的质量分数为 %。(小数点后保留两位数字)
(5)若某样品可能由NaOH、Na2CO3、NaHCO3中的一种或两种组成,为确定其组成,某同学进行下列实验:
准确称取mg样品配制成250mL溶液,取配制好的溶液20.00mL于锥形瓶中,加入2滴酚酞作指示剂,用浓度为cmol·L-1的盐酸标准液进行滴定至终点,消耗盐酸标准液v1ml,然后再滴加2滴甲基橙继续用浓度为cmol·L-1的盐酸标准液进行滴定至终点,消耗盐酸标准液v2ml(v1和v2均不为0),
根据v1和v2数值大小判断样品的组成(用化学式表示):
①v1>v2 ②v1=v2 ③v1<v2
试题篮
()