相同条件下,同浓度的下列溶液,其pH值最大的是
| A.Na2CO3 | B.CH3COONa | C.NaCl | D.NaHSO4 |
有①Na2CO3溶液;②CH3COONa溶液;③NaOH溶液各25 mL,物质的量浓度均为0.1 mol/L,下列说法正确的是( )
| A.3种溶液pH的大小顺序是③>②>① |
| B.若将3种溶液稀释相同倍数,pH变化最大的是② |
| C.若分别加入25 mL 0.1 mol/L盐酸后,pH最大的是① |
| D.若3种溶液的pH均为9,则物质的量浓度的大小顺序是③>①>② |
下列溶液中微粒浓度关系一定正确的是( )
| A.氨水与氯化铵的pH=7的混合溶液中:c(Cl-) >c(NH4+) |
| B.pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)=c(H+) |
| C.0.1 mol•L-1的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+) |
| D.0.1 mol/L的磷酸钠溶液中:c(Na+)>c(OH-)>c(PO43-)>c(H+) |
下列物质中不能发生水解反应的是
| A.蛋白质 | B.淀粉 | C.葡萄糖 | D.脂肪 |
常温时,0.1mol/LHA溶液的pH>1,0.1mol/L BOH溶液中c(OH-): c(H+)=1012,将这两种溶液等体积混合,以下离子浓度关系判断正确的是( )
| A.c(H+)<c(OH-)=c(A-)<c(B+) |
| B.c(OH-)<c(H+)<c(B+)<c(A-) |
| C.c(H+)<c(OH-)<c(A-)<c(B+) |
| D.c(A-)= c(B+)>c(H+)=c(OH-) |
已知:甲酸的酸性比乙酸强。则物质的量浓度相等的下列物质①C6H5ONa ②CH3COONa ③Na2CO3④NaHCO3⑤HCOONa ⑥NaOH的溶液的pH 按由大到小的顺序排列正确的是 ( )
| A.③⑥①④②⑤ | B.⑥③①④②⑤ | C.⑤②①④③⑥ | D.⑥③④②①⑤ |
下列关于0.1 mol·L-1 CH3COONa溶液的说法正确的是
| A.加入少量FeCl3固体,c(CH3COO-)增大 |
| B.加入少量NaOH固体,c(CH3COO-)增大 |
| C.稀释溶液,溶液的pH增大 |
| D.加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-) |
为了除去氯化镁酸性溶液中的Fe3+,可在加热搅拌的条件下加入一种过量的试剂,过滤后再加入适量的盐酸。这种试剂( )
| A.氨水 | B.氢氧化钠 | C.碳酸钠 | D.碳酸镁 |
关于0.1mol·L-1NaHCO3溶液,下列说法正确的是
A.溶质水解反应:HCO3- +H2O H3O++CO32- H3O++CO32- |
| B.离子浓度关系:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) |
| C.微粒浓度关系:c(Na+)>c(HCO3-) >c(H2CO3)>c(CO32-) |
| D.微粒浓度关系:c(Na+)=2[c(H2CO3)+c(HCO3-)+c(CO32-)] |
“84”消毒夜在日常生活中被广泛使用。该消毒液无色,pH大于7,对某些有色物质有漂白作用。你认为它可能的有效成分是
| A.SO2 | B.Na2CO3 | C.KMnO4 | D.NaClO |
下列离子方程式中,属于水解反应的是
A.HCOOH + H2O HCOO-+ H3O+ HCOO-+ H3O+ |
B.CO2 + H2O HCO3-+ H+ HCO3-+ H+ |
C.CO32-+ H2O HCO3-+ OH- HCO3-+ OH- |
D.HS-+ H2O S2-+ H3O+ S2-+ H3O+ |
对于相同体积的K2CO3溶液(浓度为c1)和(NH4)2CO3溶液(浓度为c2),若其中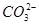 的物质的量浓度相同,则c1和c2的关系是
的物质的量浓度相同,则c1和c2的关系是
| A.c1=2c2 | B.c1>c2 | C.c1=c2 | D.c1<c2 |
室温时,将浓度和体积分别为c1、V1的NaOH溶液和c2、V2的CH3COOH溶液相混合,下列关于该混合溶液的叙述正确的是( )
| A.若pH>7,则一定是c1V1>c2V2 |
| B.在任何情况下都是c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
| C.当pH=7时,若V1=V2,则一定是c2=c1 |
| D.若V1=V2,c1=c2,则c(CH3COO-)+c(CH3COOH)=c(Na+)+c(H+) |
下列各离子方程式属于水解反应,且可使溶液呈酸性的是 ( )
A.HS +H +H 0 0 H H O O +s +s |
B.NH +2H +2H O O NH3·H NH3·H O+H O+H O+ O+ |
C.HCO +OH +OH  CO CO +H +H O O |
D.CO +2H +2H O O H H CO CO +2OH +2OH |
试题篮
()