下图所示三个烧瓶中分别装入含酚酞的0.01 mol·L-1CH3COONa 溶液,并分别放置在盛有水的烧杯中,
然后向烧杯①中加入生石灰,向烧杯③中加入NH4NO3晶体,烧杯②中不加任何物质。
(1)含酚酞的0.01 mol·L-1CH3COONa溶液显浅红色的原因为(用离子方程式表达)________.
(2)实验过程中发现烧瓶①中溶液红色变深,烧瓶③中溶液红色变浅,则下列叙述正确的是______。
| A.水解反应为放热反应 |
| B.水解反应为吸热反应 |
| C.NH4NO3溶于水时放出热量 |
| D.NH4NO3溶于水时吸收热量 |
(3)向0.01 mol·L-1CH3COONa溶液中分别加入NaCl固体、Na2CO3固体、FeSO4固体,使CH3COO-水解平衡移动的方向分别为___________、______、_________。(填“左”、“右”或“不移动”)
25℃时,电离平衡常数:
| 化学式 |
CH3COOH |
H2CO3 |
HClO |
| 电离平衡常数 |
1.8×10﹣5 |
K1=4.3×10﹣7 K2=5.6×10﹣11 |
3.0×10﹣8 |
回答下列问题:
(1)物质的量浓度为0.1mol/L的下列四种物质:a.Na2CO3,b.NaClO,c.CH3COONa d.NaHCO3;pH由大到小的顺序是: ;(填编号)
(2)常温下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是: ;
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)•c(OH﹣) D.c (OH﹣)/ c(H+)
(3)体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如图.
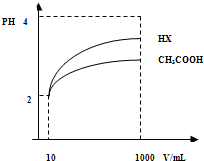
则HX的电离平衡常数 (填“大于”、“等于”或“小于”)醋酸的平衡常数;理由是 ,
稀释后,HX溶液中水电离出来的c(H+) 醋酸溶液水电离出来c(H+)(填“大于”、“等于”或“小于”)
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO﹣)﹣c(Na+)= .(填准确数值).
现有九种物质(1)铝线(2)石墨(3)氯气(4)硫酸镁晶体(5)无水乙酸(6)金刚石(7)石灰水(8)乙醇(9)熔融的硝酸钾
其中能导电的是 ;
属于电解质的是 ;
既不是电解质也不是非电解质的是 .
乙酸的电离方程式是
乙酸钠水解的离子方程式是
(1)0.010 mol/L的HCN(aq)与0.010 mol/L NaCN(aq)等体积混合,已知该混合溶液中c(Na+) > c(CN-),则溶液中c(OH -) c(H +)( 用“>、<、=”符号填空)。
(2)溶质的物质的量浓度相同的 HCl(aq) 、H2SO4(aq) 、CH3COOH(aq)各100 mL,①水的电离程度最大的是 溶液 ②分别与同样的锌粒反应,开始时反应速率最快的是 溶液(写名称)。
(3)某温度下,纯水中的c(H +) = 2.0×10-6mol/L,则此时PH=3的硫酸溶液中,c(OH -) = ,水电离的H+的物质的量浓度是 。
(1)1.00g CH4完全燃烧生成液态水和CO2,放出55.6 kJ热量,写出表示CH4的燃烧热的热化学方程式 。
(2)等物质的量浓度的下列溶液:①(NH4)2SO4 ②NH4HCO3 ③NH4Cl ④NH4Fe(SO4)2中 ,c(NH4+)由大到小的顺序为 。
(3)写出符合要求的方程式
①饱和的FeCl3溶液滴入沸水中 (写离子方程式)
②NaHCO3在水溶液中存在的所有电离过程
(4)某温度下的溶液中,c(H+)=10xmol•L-1,c(OH-)=10ymol•L-1。x与y的关系如图所示:

①该温度下,NaCl溶液的pH= 。
②该温度下,pH=8的Ba(OH)2溶液与pH=6的盐酸混合,并保持恒温,欲使混合溶液的pH=7,则Ba(OH)2溶液与盐酸的体积比为 。(忽略溶液混合时体积变化)
常温下,向25mL 0.1mol/L MOH溶液中逐滴加入0.2mol/L HA溶液,曲线如图所示(体积变化忽略不计).回答下列问题: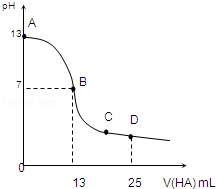
(1)写出MOH的电离方程式:____________________
(2)MOH与HA恰好完全反应时,混合溶液中由水电离出的c(H+)__________0.2mol/L HA溶液中由水电离出的c(H+)(填“>”“<”或“=”).
(3)分别写出B、C两点,混合溶液中各离子浓度的大小关系B点______________;C点___________;
(4)若D点测得混合溶液的pH=3,则 c(HA)+c(H+)=_____________
(1)体积相同,浓度均为0.2 mol·L-1的盐酸和CH3COOH溶液,分别加水稀释m倍、n倍,溶液的pH都变成3,则m与n的关系为_____________。
(2)体积相同,pH均等于13的氨水和NaOH溶液,分别加水稀释m倍、n倍,溶液的pH都变成9,则m与n的关系为_____________。
(3)25℃下,某Na2SO4溶液中c(SO42-)=5×10-4mol·L-1,取该溶液1 mL,加水稀释至10 mL,则稀释后溶液中c(Na+):c(OH-)=_____________。
(4)t℃下,KW=1×10-12时,将pH=11的苛性钠溶液V1 L与pH=1的稀硫酸V2 L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH =2,此溶液中各种离子的浓度由大到小的排列顺序是__________________。
(5) 0.1 mol·L-1的(NH4)2SO4溶液中离子浓度由大到小的顺序为__________。
已知:H2CO3在水中分两步电离,常温时的电离常数分别为K1=4.3×10-7,K2=4.0×10-11
(1)请写出H2CO3第一步电离的电离方程式__________,K2的表达式是K2= _____________
(2)计算常温时,0.1mol/L的Na2CO3溶液CO32-中的水解常数(忽略第二步水解)Kh=______________,溶液的pH= _______________。
常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
| 实验编号 |
HA物质的量 浓度(mol/L) |
NaOH物质的 量浓度(mol/L) |
混合溶液的pH |
| 甲 |
0.2 |
0.2 |
pH=a |
| 乙 |
c1 |
0.2 |
pH=7 |
| 丙 |
0.2 |
0.1 |
pH>7 |
| 丁 |
0.1 |
0.1 |
pH=9 |
请回答下列问题:
(1)不考虑其他组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱酸 。
(2)不考虑其他组的实验结果,单从乙组情况分析,c1是否一定等于0.2___________(填“是”或“否”)。混合溶液中离子浓度c(A-)与c(Na+)的大小关系是___________。
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HA是__________酸(填“强”或“弱”)。该混合溶液中离子浓度由大到小的顺序是 。
(4)丁组实验所得混合溶液中由水电离出的c(OH-)=________mol/L。写出该混合溶液中下列算式的精确结果(不能做近似计算,回答准确值,结果不一定要化简)。c(Na+)-c(A-)=________mol/L。
现有25℃时0.1mol•L-1的氨水,请回答以下问题:
(1)若向氨水中加入少量硫酸铵固体,一水合氨的电离平衡___________移动(填“向左”、“向右”或“不”);此时溶液中C(OH-)/C(NH3·H2O)___________(填“增大”、“减小”或“不变”)。
(2)若向氨水中加入稀硫酸至溶液的pH=7,此时C(NH4+)="a" mol•L-1,则C(SO42-)=_______________。
(3)若向氨水中加入稀硫酸,使其恰好中和,写出反应的离子方程式:__________________;所得溶液的pH___________7(填“>”、“<”或“=”),用离子方程式表示其原因______________,所得溶液中各离子的物质的量浓度由大到小的顺是______________________。
已知某溶液中存在OH-、H+、NH4+、Cl-四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
①c(Cl-)>c(NH4+)>c(H+)>c(OH-)
②c(Cl-)>c(NH4+)>c(OH-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+)
④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
填写下列空白:
(1)若溶液中只溶解了一种溶质,则该溶质是________,上述四种离子浓度的大小顺序为________(选填序号)。
(2)若上述关系中③是正确的,则溶液中的溶质为________;
若上述关系中④是正确的,则溶液中的溶质为________。
(3)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)________c(NH3·H2O)(填“大于”“小于”或“等于”,下同),混合前酸中
c (H+)和碱中c(OH-)的关系为c(H+)________c(OH-)。
(10分)常温下,向25mL 0.1mol/L MOH溶液中逐滴加入0.2mol/L HA溶液,曲线如图所示(体积变化忽略不计).回答下列问题: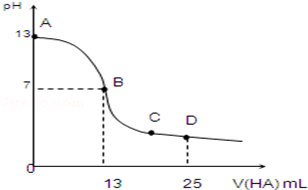
(1)写出MOH的电离方程式:__________________
(2)MOH与HA恰好完全反应时,溶液呈________性(填“酸”、“碱”或“中”),理由是(用离子方程式表示):__________;此时,混合溶液中由水电离出的c(H+)_________0.2mol/L HA溶液中由水电离出的c(H+)(填“>”“<”或“=”).
(3)写出B点,混合溶液中各离子浓度的大小关系B点____________.
(4)D点时,溶液中c(A﹣)+c(HA)__________2c(M+)(填“>”、“<”或“=”).
对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施之一。
请回答以下问题:
(1)硫酸工厂的酸性废水中砷(As)元素(主要以弱酸H3As03形式存在)含量极高,为控制砷的排放,某工厂采用化学沉降法处理含砷废水。
①已知砷是氮的同族元素,比氮原子多2个电子层,砷在元素周期表的位置为 ,AsH3的稳定性比NH3的稳定性 (填“强’’或“弱’’)。
②工业上采用硫化法(通常用硫化钠)去除废水中的砷,生成难溶的三硫化二砷,该反应的离子方程式为 。
(2)今年8月1 2日晚,天津滨海新区危险品仓库发生爆炸事故,少量氰化物因爆炸冲击发生泄漏,CN一有剧毒,泄露会污染水源和空气,需要处理。
①包知HCN为一元弱酸,则NaCN溶液的pH 7(填“>”“=”或“<”)。
②处理含CN一废水的方法之一是在微生物的作用下,CN-被氧气氧化成HC03一,同时生成NH3,该反应的离子方程式为
(3)电渗析法处理厨房垃圾发酵液,同时得到乳酸的原理如右图所示(图中“HA’’表示乳酸分子,A--表示乳酸根离子)。

阳极的电极反应式为 简述浓缩室中得到浓乳酸的原理
FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。请回答下列问题:
(1)FeCl3净水的原理是 。FeCl3溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示) 。
(2)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3。
①若酸性FeCl2废液中c(Fe2+)=2.0×10-2mol·L-1, c(Fe3+)=1.0×10-3mol·L-1, c(Cl-)=5.3×10-2mol·L-1,则该溶液的PH约为 。
②完成NaClO3氧化FeCl2的离子方程式:
 ClO3-+
ClO3-+ Fe2++
Fe2++ =
= Cl-+
Cl-+ Fe3++
Fe3++ .
.
(3)FeCl3在溶液中分三步水解:
Fe3++H2O  Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)++H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反应的平衡常数K1、K2、K3由大到小的顺序是 。
通过控制条件,以上水解产物聚合,生成聚合氧化铁,离子方程式为:
xFe3++yH2O Fex(OH)y(3x-y)++yH+
Fex(OH)y(3x-y)++yH+
欲使平衡正向移动可采用的方法是(填序号) 。
a.降温 b.加水稀释 c.加入NH4Cl d.加入NaHCO3
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是 。
(4)天津某污水处理厂用氯化铁净化污水的结果如下图所示。由图中数据得出每升污水中投放聚合氯化铁[以Fe(mg·L-1)表示]的最佳范围约为 mg·L-1。

(14分)
Ⅰ.为了除去KCl溶液中少量的Mg2+、SO42-,可选用Ba(OH)2、HCl和K2CO3三种试剂,按如下步骤操作:
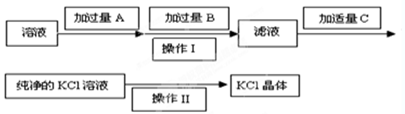
(1)上述试剂中, B是 ,
(2)操作Ⅱ的名称是 。
(3)加过量A时发生有关反应的离子方程式为 、 。
Ⅱ.一份溶液中可能含有K+、Al3+、H+、NH4+、Cl-、Br-、I-、ClO―、AlO2― 等离子中的若干种。为了确定溶液的组成,进行了如下操作:
(1)往该溶液中逐滴加入NaOH溶液并适当加热,产生沉淀和气体的物质的量(n)与加入NaOH溶液的体积关系如图所示;
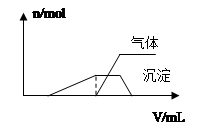
则该溶液中一定存在的离子是 ,
(2)经检测后,该溶液中含有大量的Cl-、Br-、I-,若向1L该混合溶液中通入一定量的氯气,则溶液中Cl-、Br-、I-与通入氯气的体积(标况下)关系如图所示,回答下列问题:
| Cl2的体积(标况下) |
2.8L |
5.6L |
11.2L |
| n(Cl- ) |
1.25mol |
1.5 mol |
2 mol |
| n(Br- ) |
1.5 mol |
1.4mol |
0.9 mol |
| n(I- ) |
a mol |
0 |
0 |
① 则a为
② 原溶液中Cl-、Br-、I-的物质的量浓度之比为
试题篮
()