下列实验操作、现象和结论均正确的是
| 选项 |
实验操作 |
现象 |
结论 |
| A |
铜放入稀硫酸中,再加入硝酸钠固体 |
开始无明显现象,后溶液变蓝,有气泡放出,铜溶解 |
硝酸钠可以加快铜与稀硫酸的反应速率 |
| B |
在KIO3溶液中加入HI溶液,并加入淀粉 |
溶液变成蓝色 |
KIO3的氧化性比I2强 |
| C |
向CH2=CHCH2OH中滴入酸性高锰酸钾溶液 |
紫红色褪去 |
证明CH2=CHCH2OH中含有碳碳双键 |
| D |
向Na2S溶液中加入酚酞,再滴加稀盐酸 |
溶液先变红,后红色变浅直至消失 |
证明非金属性:Cl>S |
(每空2分,共12分)非金属元素H、C、O、S、Cl能形成多种用途很广泛的单质和化合物,试完成下列填空。
(1)O2-的电子式为__________;
(2)O、Cl两元素形成的单质和化合物常用来杀菌消毒,试举例__________(写化学式,任写两种);
(3)H2O在常温下为液态,H2S为气态,H2O的沸点高于H2S的主要原因是__ _;
(4)Cl2是一种大气污染物,液氯储存区贴有的说明卡如下(部分):
| 危险性 |
 |
| 储运要求 |
远离金属粉末、氨、烃类、醇类物质;设置氯气检测仪 |
| 泄漏处理 |
NaOH、NaHSO3溶液吸收 |
| 包装 |
钢瓶 |
①用离子方程式表示“泄漏处理”中NaHSO3溶液的作用__ __。
②若液氯泄漏后遇到苯,在钢瓶表面氯与苯的反应明显加快,原因是__ __。
③将Cl2通入适量KOH溶液中,产物中可能有KCl、KClO、KClO3。当溶液中c(Cl-)∶c(ClO-)===11∶1时,则c(ClO-)∶c(ClO )比值等于___。
)比值等于___。
对溶液中的反应,如图像中m表示生成沉淀的物质的量,n表示参加反应的某一种反应物的物质的量,则下列叙述中错误的是:
| A.符合甲图像的两种反应物可以是AlCl3和NaOH |
| B.符合乙图像的两种反应物可以是Ca(OH)2和CO2 |
| C.符合丙图像的反应可以是在Ca(OH)2和KOH的混合溶液中通入CO2 |
| D.符合丙图像的反应可以是在NH4Al(SO4)2溶液中加入NaOH |
已知NH4++AlO2-+2H2O=Al(OH)3↓+NH3·H2O。向含有等物质的量的NH4Cl、AlCl3和HCl混合溶液中慢慢滴加NaOH溶液至过量,并不断搅拌,可能发生以下离子反应:
①H++OH-=H2O; ②Al(OH)3+OH-=AlO2-+2H2O; ③Al3++3OH-=Al(OH)3↓;
④NH4++OH-=NH3·H2O; ⑤NH4++AlO2-+2H2O=Al(OH)3↓+NH3·H2O。
其正确的离子反应顺序是
| A.①③②④ | B.①③④② | C.①③②⑤ | D.①④③② |
一定条件下,中学化学常见物质甲、乙之间存在如下转化关系,乙是
| A.HCl | B.FeCl2 | C.KOH | D.NaHCO3 |
下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
| 选项 |
实验 |
现象 |
结论 |
| A. |
将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液 |
有气体生成,溶液呈血红色 |
稀硝酸将Fe氧化为Fe3+ |
| B. |
将铜粉加1.0mol·L-1Fe2(SO4)3溶液中 |
溶液变蓝、有黑色固体出现 |
金属铁比铜活泼 |
| C. |
用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 |
熔化后的液态铝滴落下来 |
金属铝的熔点较低 |
| D. |
将0.1mol·L-1MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol·L-1CuSO4溶液 |
现有白色沉淀生成后变为浅蓝色沉淀 |
Cu(OH)2的溶度积比Mg(OH)2的小 |
根据下图海水综合利用的工业流程图,判断下列说法正确的是
已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。
| A.除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为: NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 |
| B.在过程②中将MgCl2·6H2O灼烧即可制得无水MgCl2 |
| C.从能量角度来看,氯碱工业中的电解饱和食盐水是一个将化学能转化为电能的过程 |
| D.从第③步到第④步的目的是为了浓缩富集溴 |
某Na2CO3、NaAlO2的混合溶液中逐滴加入1mol/L的盐酸,测得溶液中的CO32-、HCO3-、AlO2-、Al3+离子的物质的量与加入盐酸溶液的体积变化关系如图所示,则下列说法正确的是: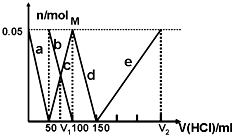
| A.原混合溶液中的CO2-3与AlO-2的物质的量之比为1:2 |
| B.V1:V2=1:5 |
| C.M点时生成的CO2为0.05mol |
| D.a曲线表示的离子方程式为:AlO-2+H++H2O=Al(OH)3↓ |
已知X、M都是中学教材常见元素,下列对两个离子反应通式的推断中,其中正确的是
(甲)XO3n+Xn+H+--X单质+H2O(未配平);(乙)Mm++mOH-→M(OH)m↓
①若n=1,则XO3n中X元素为+5价,X位于周期表第VA族
②若n=2.则X最高价氧化物的水化物可能与它的氢化物反应
③若m=2,则在空气中蒸干、灼烧MSO4溶液一定能得到MSO4
④若m=3,则MCl3与氢氧化钠溶液互滴时的现象可能不同
| A.②③ | B.②④ | C.①② | D.①③ |
海水资源的利用具有广阔前景。海水中主要离子的含量如下:
| 成分 |
Cl- |
Na+ |
SO42- |
Mg2+ |
Ca2+ |
HCO3- |
Br- |
| 含量/(mg·L-1) |
18980 |
10560 |
2560 |
1272 |
400 |
142 |
64 |
(1)以食盐为原料进行生产并综合利用的某些过程如下图所示。

①除去粗盐中的Ca2+、Mg2+和SO 离子,加入沉淀剂a.Na2CO3 b.NaOH c.BaCl2,
离子,加入沉淀剂a.Na2CO3 b.NaOH c.BaCl2,
合理的一种顺序是(填序号) 。将滤液的pH调至酸性除去的离子是 。
②电解饱和食盐水的化学方程式是 ;
③侯德榜向饱和食盐水中通入NH3、CO2气体制NaHCO3晶体的化学方程式为 。
其依据是 。
④工业上可用纯碱代替烧碱生产某些化工产品。如用饱和纯碱溶液与Cl2制取有效成分为NaClO的消毒液,反应的化学方程式是 。(碳酸的酸性强于次氯酸)。
(2)利用海水可以提取溴和镁,提取过程如下:

① 从MgCl2溶液中得到MgCl2·6H2O晶体的主要实验操作是 、洗涤、烘干。从MgCl2·6H2O晶体中得到无水MgCl2的主要方法是
②用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为_____________,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是_____________。
③依据上述流程,若将5 m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为 L(忽略Cl2溶解)。
将2aL Al2(SO4)3和(NH4)2SO4的混合溶液分成两等份,其中一份加入b mol BaCl2,恰好使溶液中的SO42-离子完全沉淀;另一份加入足量强碱并加热可得到c mol NH3,则原混合溶液中的Al3+离子浓度(mol/L)为( )
A. |
B. |
C. |
D. |
根据下图海水综合利用的工业流程图,判断下列说法正确的是
已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。
| A.过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质 |
| B.在过程③中将MgCl2·6H2O灼烧即可制得无水MgCl2 |
| C.在过程④、⑥反应中每氧化0.2 mol Br- 需消耗2.24 L Cl2 |
| D.过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题 |
将1.52 g铜镁合金完全溶解于50 mL密度为1.40 g·mL-1、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120 mL (标准状况),向反应后的溶液中加入浓度为1.0 mol·L-1的 NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀,下列说法不正确的是
| A.该合金中铜与镁的物质的量之比是16∶3 |
| B.该浓硝酸中HNO3的物质的量浓度是14.0 mol·L-1 |
| C.NO2和N2O4的混合气体中,NO2的体积分数是80% |
| D.反应中转移电子的物质的量为0.06 mol |
有一种混合气体,它可能由CO、CO2、SO2、HCl中的一种或多种气体组成。该气体依次通过下列物质的现象如下:通过一定量的澄清石灰水无白色沉淀析出;通过品红溶液,溶液红色褪去;通过炽热的CuO,固体变为红色;通过澄清石灰水,出现白色沉淀。该混合气体组成的各说法中,正确的是
| A.肯定不含有CO2 |
| B.只含有SO2和CO |
| C.含有SO2、CO和CO2,可能含HCl |
| D.含HCl、SO2和CO,可能含CO2 |
试题篮
()