化学中常用类比的方法可预测许多物质的性质。如根据H2+Cl2=2HCl推测:H2+Br2=2HBr。但类比是相对的,要遵循化学原理。如根据2Na2O2+2CO2=2Na2CO3+O2,类推2Na2O2+2SO2=Na2SO3+O2是错误的,应该是Na2O2+SO2=Na2SO4。下列各组类比中正确的是 ( )
A.由NH4Cl NH3↑+HCl↑,推测:NH4I NH3↑+HCl↑,推测:NH4I NH3↑+HI↑ NH3↑+HI↑ |
| B.由CO2+Ca(ClO)2+H2O=CaCO3↓+2HClO,推测:SO2+Ca(ClO)2+H2O=CaSO3↓+2HClO |
C.由2CO2+Ca(ClO)2+2H2O=C a(HCO3)2+2HClO,推测:CO2+NaClO+H2O=NaHCO3+HClO a(HCO3)2+2HClO,推测:CO2+NaClO+H2O=NaHCO3+HClO |
D.由Na2SO 3+2HCl=2NaCl+H2O+SO2↑,推测:Na2SO3+2HNO3=2NaNO3+H2O+SO2↑ 3+2HCl=2NaCl+H2O+SO2↑,推测:Na2SO3+2HNO3=2NaNO3+H2O+SO2↑ |
下列示意图与对应的反应情况正确的是
| A.含0.01molKOH 和0.01mol Ca(OH)2的混合溶液中缓慢通入CO2 |
| B.KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液 |
| C.n(O2)=1mol时,高温下C和O2在密闭容器中的反应产物 |
D.n(NaOH)=1 mol时,CO2和NaOH溶液反应生成的盐 mol时,CO2和NaOH溶液反应生成的盐 |
金属钙线是炼制优质钢材的脱氧脱磷剂,某钙线的主要成分为金属M和Ca。
(1)Ca的原子结构示意图 。
(2)配平用钙线氧脱鳞的化学方程式:
P + FeO + CaO  Ca3(PO4)2 + Fe
Ca3(PO4)2 + Fe
(3)将钙线试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n。则金属M为_________,检测Mn+ 的方法是_____________________(用离子方程式表达)。
(4)取1.6g钙线试样,与水充分反应,生成224ml H2(标准状况),再向溶液中通入适量的CO2,最多能得到CaCO3 g。
(5)处理炼钢厂含CO、SO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质S。
已知:CO(g) + 1/2 O2(g) ="=" CO2(g)  H = -283.0 kJ·mol-2
H = -283.0 kJ·mol-2
S(s) + O2(g) ="=" YO2(g)  H = -296.0 kJ·mol-1
H = -296.0 kJ·mol-1
此反应的热化学方程式是 。
碘在工农业生产和日常生活中有重要用途。
(1)上图为海带制碘的流程图。步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是 (从下列仪器中选出所需的仪器,用标号字母填写)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
步骤④发生反应的离子方程式为 。
若步骤⑤采用四氯化碳来提取碘,将四氯化碳加入含碘水溶液并振荡,将观察到的现象是 。
操作⑥可用的方法是: 。
A、加碱洗涤法 B、过滤法 C、萃取分液法 D、蒸馏或分馏法
(2)溴化碘(IBr)的化学性质类似于卤素单质,如能与大多数金属反应生成金属卤化物,跟
水反应的方程式为:IBr+H2O==HBr+HIO等,下列有关IBr的叙述中错误的是:
A.跟溴、碘相似,固体溴化碘熔沸点也很低
B.在许多反应中,溴化碘是强氧化剂
C.跟卤素单质相似,跟水反应时,溴化碘既是氧化剂,又是还原剂
D.溴化碘跟NaOH溶液反应生成NaBr、NaIO和H2O
(3)为实现中国消除碘缺乏病的目标。卫生部规定食盐必须加碘盐,其中的碘以碘酸钾(KIO3)形式存在。可以用硫酸酸化的碘化钾淀粉溶液检验加碘盐,请写出反应的离子方程式:
下表各组物质中,物质之间通过一步反应就能实现如右图所示转化的是( )
| 物质选项 |
a |
b |
c |
d |
| A |
Al |
Al(OH)3 |
NaAlO2或NaAl(OH)4 |
NaOH |
| B |
CH3CH2OH |
CH3CHO |
CH3COOH |
O2 |
| C |
Na2CO3 |
NaHCO3 |
NaOH |
CO2 |
| D |
Cl2 |
FeCl3 |
FeCl2 |
Fe |
(12分)某固体混合物可能含Al、(NH4)2SO4、MgCl2、A1Cl3、FeCl2、NaCl中的一种或几种,现对该混合物作如下实验,所得现象和有关数据如图(气体体积已换算成标况下体积):
回答下列问题:
(1)混合物中是否存在FeCl2 ___ (填“是”或“否”);你的判断依据是:
.
(2)混合物中是否存在(NH4)2SO4 ___ (填“是”或“否”),你的判断依据是:
。
(3)写出反应④的离子反应式: 。
(4)请根据计算结果判断混合物中是否含有AlCl3 __ _(填“是”或“否”),你的判断依据是:
。
下列图象能正确表示相关反应中产物物质的量的变化的是(横、纵坐标单位:mol)
| A.图l:n(HCl)=lmol,K2CO3逐步加入到HCl溶液中,在敞口容器中生成的气体 |
| B.图2:n(NaOH)="1" mol,CO2逐步通人到NaOH溶液中反应生成的盐 |
| C.图3:n(O2)=1mol,高温下C和O2在密闭容器中的反应产物 |
| D.图4:n(HNO3,)=lmol,Fe和稀HNO3反应生成的氧化产物(还原产物为NO) |

空气中的自由电子附着在气体分子或原子上形成的空气负离子(也叫阴离子)被人们称为“空气维生素”。下列各微粒中肯定不属于空气负离子的是( )
| A.O2- | B.O2-.(H2O)n |
| C.CO4-.(H2O)2 | D.PO43- |
太平洋岛国瑙鲁盛产一种高品位的磷矿石——鸟粪石,其化学式为MgNH4PO4,下列关于该物质的叙述中不正确的是
| A.鸟粪石既属于镁盐又属于磷酸盐 |
| B.鸟粪石既能与强酸反应,又能与强碱反应 |
| C.鸟粪石中既含有离子键又含有共价键 |
D.鸟粪石中两种阳离子的电子式分别为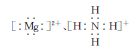 |
在室温时,下列各组中的物质分别与过量NaOH溶液反应,能生成5种盐的是:
| A.A12O3、SO2、CO2、SO3 | B.C12、A12O3、N2O5、SO3 |
| C.CO2、C12、CaO、SO3 | D.SiO2、N2O5、CO、C12 |
下列各组物质中,满足右图物质一步转化关系的选项是
| 选项 |
X |
Y |
Z |
| A |
Na |
NaOH |
NaHCO3 |
| B |
Cu |
CuSO4 |
Cu(OH)2 |
| C |
C |
CO |
CO2 |
| D |
Si |
SiO2 |
H2SiO3 |
下列图象能正确表示相关反应中产物物质的量的变化的是(横、纵坐标单位:mol)
| A.图1:n(HCl)=1mol,K2CO3逐步加入到HCl溶液中,在敞口容器中生成的气体 |
| B.图2:n(NaOH)=1mol,CO2逐步通入到NaOH溶液中反应生成的盐 |
| C.图3:n(O2)=1mol,高温下C和O2在密闭容器中的反应产物 |
| D.图4:n(HNO3)=1mol,Fe和稀HNO3反应生成的氧化产物(还原产物为NO) |

向CuSO4溶液中逐滴加入过量KI溶液,观察到产生白色沉淀,溶液变为棕色。再向反应后的混合物中不断通入SO2气体,溶液逐渐变成无色。则下列分析中正确的是( )
| A.白色沉淀是CuI2,棕色溶液含有I2 |
| B.滴加KI溶液时,转移1mole-时生成2mol白色沉淀 |
| C.上述实验条件下,物质的氧化性:Cu2+>I2>SO2 |
| D.通入SO2时,SO2与I2反应,I2作还原剂 |
下列各组物质按右图所示转化关系每一步都能一步实现的是( )
 |
甲 |
乙 |
丙 |
丁 |
] |
| A |
FeCl3 |
FeCl2 |
Fe2O3 |
Fe(OH)3 |
|
| B |
Cu |
CuO |
CuSO4 |
CuCl2 |
|
| C |
NO |
HNO3 |
NO2 |
NH3 |
|
| D |
Si |
Na2SiO3 |
SiO2 |
SiF4 |
试题篮
()