有A、B、C、D、E、F六种元素,原子序数依次增大,A、B、C、D、E均为短周期元素,A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759g•L-1,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族.均含D元素的乙(金属阳离子)、丙、丁微粒间的转化全为非氧化还原反应:均含F元素的乙(单质)、丙、丁微粒间的转化全为氧化还原反应.
请回答下列问题:
(1)单质B的结构式:________________________。
(2)F元素周期表中的位置:_______________________。
(3)均含有F元素的乙与丁在溶液中发生反应的离子方程式___________________;均含有D元素的乙与丁在溶液中发生反应的离子方程式________________________。
(4)由A、C元素组成化合物良和A、E元素组成的化合物辛,式量均为34.其中庚的溶沸点比辛_______(填“高”或“低”),原因是_________________。
物质A、B、C、D、E、F、G、H、I、J、K有下图转化关系,其中气体D、E为单质,
请按要求回答下列问题。

(1)金属A元素在周期表的位置是 ,G的化学式是__________。
(2)写出反应“C→F”的离子方程式 ;
(3)写出反应“I→J”的离子方程式 ;
(4)写出金属 H与水蒸气在高温下反应的化学方程式 。
A.B C.D.E.F六种物质的转化关系如图所示(反应条件和部分产物未标出)

(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A D反应都有红棕色气体生成,则A为 ,反应④的化学方程式为 .
(2)若A为常见的金属单质,D F是气态单质,反应①在水溶液中进行,则反应②(在水溶液中进行)的离子方程式是 .
(3)若A.D.F都是短周期非金属元素单质,且A.D所含元素同主族,A.F所含元素同周期,则反应①的化学方程式为 .
A是用途最广的金属,B、C是两种常见气体单质,E溶液为常见强酸,D溶液中滴加KSCN溶液显红色,它们相互转化关系如图所示.

请回答:
(1)写出B物质的化学式: .
(2)写出第③步反应的化学方程式为 .
(3)第④步反应的离子方程式是 .
(4)写出SO2在水中与B反应的离子方程式 .
(5)F溶液中滴入NaOH溶液可能产生的实验现象是 .
(每空2分,共14分)A、B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如图所示(部分产物已略去)。

(1)若A为金属单质,D是某强酸的稀溶液,则反应C+D→B的离子方程式为 。
(2)若A、B为盐,D为强碱,A的水溶液显酸性,则①C的化学式为 ;②反应B+A→C的离子方程式为 ;
(3)若A为强碱,D为气态氧化物。常温时,将B的水溶液露置于空气中,其pH随时间t变化可能如上图的图b或图c所示(不考虑D的溶解和水的挥发)。
①若图b符合事实,则D为 (填化学式),此时图b中x 7(填“﹥”“﹤”“﹦”)②若图c符合事实,则其pH变化的原因是 (用离子方程式表示)。
(4)若A为非金属单质,D是空气的主要成分之一。它们之间转化时能量变化如上图a,请写出A+D→C的热化学方程式: 。
在下列物质转化关系中,A是(NH4)2S,D的相对分子质量比C的相对分子质量大16,E是酸,当X无论是强酸还是强碱时,都有如图的转化关系:
请回答:
(1)当X是强酸时A、B、C、D、E均含同一种元素。则E是__________________,写出B生成C的化学方程式________________。
(2)当X是强碱时,A、B、C、D、E均含另外同一种元素。则E是_____________,写出B生成C的化学方程式________________。
(3)X无论是强酸还是强碱,上述转化中Z是同一种物质,写出Z的电子式_________________。
(4)同温同压下,分别在强酸和强碱条件下生成的气体B在等质量时的体积比为______________。
(共12分)各物质之间的转化关系如下图,部分生成物省略。C、D是由X、Y、Z中两种元素组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10。D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷线路板。请回答下列问题:

(1)G元素在周期表中的位置______________。
(2)写出实验室制备G的离子反应方程式 。
(3)气体D与NaOH溶液反应可生成两种盐P和Q,在P中Na的质量分数为43%,其俗名为 。
(4)实验室中检验L溶液中的阳离子常选用 溶液,现象是 。
(5)A中包含X、Y、Z元素,A的化学式为 。
下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出)。其中I是由第三周期元素组成的单质中熔点最高的金属,K是一种红棕色气体。(已知:一定条件下FeS2能被空气氧化为氧化铁和二氧化硫)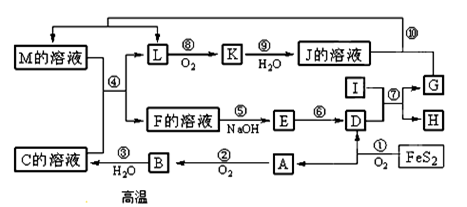
请填写下列空白:
(1)在周期表中,组成单质G的元素位于第________周期_________族。
(2)在反应⑦中氧化剂与还原剂的物质的量之比为___________________。
(3)在②、③、⑥、⑨中既属于化合反应又属于非氧化还原反应的是___________(填序号)
(4)反应④的离子方程式是:_________________________________________。
(5)将化合物D与KNO3、KOH共融,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾),同时还生成KNO2和H2O。该反应的化学方程式是:____________________________。
下图中X、Y、Z为单质,其他化合物,它们之间存在有如下转化关系(部分产物已略去)。其中,A俗称磁性氧化铁;E是不溶于水的酸性氧化物,能与氢氟酸反应.回答下列问题:
(1)组成单质Y的元素在周期表中的位置是________________;R的化学式是________。
(2)写出A和D的稀溶液反应生成G的离子方程式______________________。
(3)向含4mol D的稀溶液中,逐渐加入X粉末至过量.假设生成的气体只有一种,请在坐标系中画出n(X2+)随n(X)变化的示意图,并标出n(X2+)的最大值_____________。
A、B、C、D、E、F六种物质在一定条件下有如图所示的相互转化关系,所有反应物和生成物均已给出。

(1)若反应①、②、③均为水溶液中的置换反应,A、D、E为卤素单质,则A、D、E的化学式分别为 、 、 。
(2)若B是水,C是生产生活中应用最广泛的金属所对应的一种具 有 磁性的黑色氧化物,D是相同条件下密度最小的气体,E是一种无色、无味的有毒气体,则反应①的化学方程式是 。
(3)若B为一种淡黄色固体。绿色植物的光合作用和呼吸作用可实现自然界中D和E 的循环。则反应①的离子方程式是 。在反应③中,若生成1 mol D,则转移电子的物质的量为 。
下面是有关物质的转化关系图(部分产物已省略),其中A为单质,E在常温下为液体,D是一种气体,C的相对分子质量为78。请回答下列有关问题:

(1)下列对C的结构、性质推断中不正确的是 。
| A.久置于空气中会变成白色 | B.具有强氧化性 |
| C.晶体中存在离子键与共价键 | D.是一种碱性氧化物 |
(2)A的原子结构示意图为_______________;G→H的化学方程式________________。
(3)C和E反应生成H的离子方程式为______________________,反应中氧化剂与还原剂的物质的量之比为______ 。
已知A、B、C、D、E均为中学化学中常见物质,在一定条件下相互转化关系如下图所示(反应条件和部分产物已省略)。已知:

①A常温下为黄绿色的气体单质。
②B为一种常见变价金属单质,在冷的浓硫酸中会被钝化。
③C的水溶液是一种无氧酸,且C的组成中含有与A相同的元素。
请回答下列问题:
(1)A的化学式为 ,构成非金属单质A的元素的最高价氧化物的分子式为 ,C的名称为 。
(2)A与水反应的化学方程式为 。
(3)A与E反应生成D的离子方程式为 。
(4)在E的水溶液中加入足量氢氧化钠溶液,观察到的现象为 。
某新型无机非金属材料K由两种非金属元素组成,它是一种超硬物质,具有耐磨、耐腐蚀、抗冷热冲击、抗氧化的特性。它是以中学化学中常见物质为原料来生产的,图中C、M、K均含A元素,M的分子式为A(NH2)4;E为不含A 元素的氢化物,在空气中易形成白雾;G、F均为难溶于水的白色沉淀,H为氧化物,J为气体;其余物质均为中学化学中常见物质。(提示:NH3和H2O的化学性质在某些方面相似)

请回答下列问题:
(1)写出指定物质的化学式:A ,C ,F 。
(2)K的化学式为 。
(3)写出图中下列序号的化学方程式:
反应④ ;
反应⑤ 。
(4)写出图中反应⑥的离子方程式: 。
已知D、M、H是常见得非金属单质,其中M是无色气体,H是有色气体。J是一种金属单质(其同族的某种元素是形成化合物种类最多的元素),A、C是金属氧化物,C和J均是某种常见电池的电极材料,J元素的+2价化合物比+4价化合物稳定,B与C反应时,每生成1molH同时消耗4molB和1molC。K只知含有CO或CO2中的一种或两种。它们关系如下图所示:
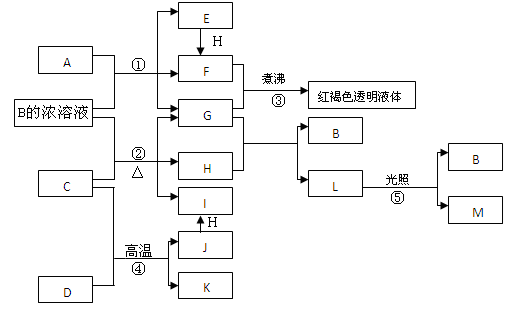
(1)写出A物质中所含金属元素在周期表中的位置:_________________。
(2)写出化合物L的电子式:______________ 反应②的化学方程式为_________________。
(3)向图中的红褐色透明液体中逐滴滴入HI溶液,可以观察到先产生红褐色沉淀,后红褐色沉淀溶解,红褐色沉淀溶解的离子方程式为_______________。
(4)由金属氧化物A和C得到其相应的金属,在冶金工业上一般可用_______________(填序号)方法
①热还原法 ②电解法 ③热分解法
其中从A得到其相应金属也可用铝热法,若反应中1molA参加反应,转移电子的物质的量为________mol。
(5)用C、J作电极,与硫酸构成如图所示原电池,负极的电极反应为__________,当反应转移2mol电子时,负极质量增加______克。

试题篮
()