按下面的实验过程填空:
写出上述反应的化学方程式:
(1)_________________________________________________________
(2)_________________________________________________________
(3)_________________________________________________________
海水占地球总储水量的97.2%,若把海水淡化和化工生产结合起来,既可解决淡水资源缺乏的问题,又可充分利用海洋资源。

(1)目前,国际上实用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经冷却而得高纯度淡水。由此可判断蒸馏法是 (填:物理变化或化学变化)。
(2)工业上利用电解饱和食盐水可制得重要化工产品。反应式为:食盐+H2O ® NaOH+H2+Cl2(未配平),该反应中食盐的化学式是 ;利用电解所得气体制36.5%的浓盐酸1000 t,最少需消耗食盐 t。
(3)近年来,有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法。该方法流程如下:
请写出②④的化学反应方程式: 、 。
用干燥的高锰酸钾可以制得极纯而干燥的氧气:KMnO4→MnO2+K2O+O2(240 ℃)。下列说法不正确的是( )
| A.每生成16 g氧气转移4 mol电子 |
| B.相同质量的KMnO4分解,生成MnO2的反应比生成K2MnO4的反应放出更多氧气 |
| C.O2是氧化产物,MnO2是还原产物 |
| D.在此条件下,KMnO4的氧化性强于O2 |
在已经提取氯化钠、溴、镁等化学物质的富碘卤水中,采取下面的工艺流程生产单质碘。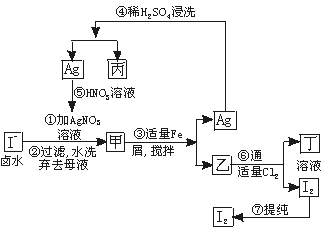
试回答下列问题:
(1)乙、丁中溶质的化学式:乙________________;丁_____________________。
(2)第④步操作中用稀H2SO4浸洗的目的是_____________________(填写字母编号)
| A.除去未反应的NO3- |
| B.除去未反应的I |
| C.除去未反应的Fe |
| D.除去碱性物质 |
(3)第⑦步操作可供提纯I2的两种方法是___________和______________(不要求写具体步骤)。
(4)实验室检验I2的方法是_______________________________________。
(5)甲物质见光易变黑,其原因是(用化学方程式表示)______________________。
下列物质分别与100mL 2mol/L的盐酸恰好反应时,所得溶液的溶质的物质的量浓度的大小关系是:①镁粉 ②氧化镁 ③氢氧化镁 ④碳酸镁
| A.①>②>③>④ | B.①>②=④>③ |
| C.①>④>③=② | D.④>①>②=③ |
氯化溴是由两种卤素互相结合而成的卤素化合物,其化学性质与Cl2相似,能与金属和非金属反应生成卤化物,能与水反应:BrCl+H2O====HBrO+HCl,下列有关BrCl的性质的叙述中不正确的是( )
| A.是较强的氧化剂 |
| B.是一种化合物 |
| C.能使湿润的淀粉碘化钾试纸变蓝 |
| D.BrCl与水反应,BrCl既是氧化剂又是还原剂 |
某无色气体可能含有HCl、 HBr 、SO2、CO2中的一种或几种。将气体通入到适量氯水中,恰好完全反应,不再剩余气体。将所得的无色溶液分装在两个试管中,分别加入酸化的AgNO3溶液和酸化的BaCl2溶液,均产生白色沉淀。则下列判断正确的是( )
| A.原气体中一定有SO2 ,一定无HBr | B.原气体中可能有SO2 |
| C.原气体中一定有HCl | D.不能确定有无HCl,但一定无CO2 |
向一定量的FeO、Fe、Fe3O4的混合物中加入100 mL 1 mol·L-1的盐酸,恰好使混合物完全溶解,并放出224 mL(标准状况)的气体,在所得溶液中加入KSCN溶液无血红色出现。若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量是
| A.11.2 g | B.5.6 g | C.2.8 g | D.无法计算 |
关于卤化银分解实验的设计
有关卤化银的感光性,可按以下方法来进行实验:
试剂和仪器: 0.1 mol·L-1的NaCl、NaBr、KI溶液,2%的AgNO3溶液。500 mL圆底烧瓶、大烧杯、聚光电筒。
实验步骤:
(1)将3只预先注有4/5容积蒸馏水的圆底烧瓶用大烧杯垫托安置于讲台上,使之处于较好的视觉高度,编号。
(2)依次往上述烧瓶中加入2至5 mL NaCl、NaBr和KI溶液,振荡摇匀。
(3)慢慢地往烧瓶中滴加AgNO3溶液,边滴边振荡,可三名同学同时操作,3种胶体同时制作,便于比较。注意观察胶体形成的效果,要求胶体颜色明显,无浑浊状态。
(4)胶体制备好后,记录时间,用聚光电筒进行爆光(或置于阳光下),观察分解反应的速度及颜色等现象的变化,做好记录。
结论:分解速率:在同样光照条件下,AgBr分解最快,先由浅黄色透明状变成灰黑色浑浊态,时间约2 min;AgCl次之,由乳白透明状变成灰白浑浊态;AgI最慢,较长时间才略有变化。
问题:
1.你认为本实验有何优点?
2.18世纪70年代.瑞典化学家舍勒在研究一种白色、难溶于水的盐时发现,在黑暗中此盐并无气味,而在光照时开始变黑并有刺激性气味的气体产生。此盐是
A.氟化银 A.氯化银 C.溴化银 D.碘化银
有一种碘的氯化物可以称为碘酸碘,其中碘元素呈+3、+5两种价态,则这种化合物的化学式是( )
| A.I2O4 | B.I3O5 | C.I4O7 | D.I4O9 |
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下图:
(1)指出制取碘的过程中有关的实验操作名称:
① ;② 。
(2)提取碘的过程中.可供选择的有机试剂是 。
| A.甲苯、酒精 | B.四氯化碳、苯 | C.汽油、乙酸 | D.汽油、甘油 |
(3)为使海藻灰中碘离子转化为碘的有机溶液.实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品.尚缺少的玻璃仪器是 。
(4)从含碘的有机溶液中提取碘和回收有机溶液,还需要经过蒸馏。观察上述实验装置指出其错误之处,并加以改正。
(5)进行上述蒸馏操作时.使用水浴的原因是
。最后晶态碘在 里聚集。
试题篮
()