下列说法正确的是 ( )。
| A.凡是中心原子采取sp3杂化的分子,其立体构型都是正四面体型 |
| B.在SCl2中,中心原子S采取sp杂化轨道成键 |
| C.杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对 |
| D.凡AB3型的共价化合物,其中心原子A均采用sp3杂化轨道成键 |
下列说法不正确的是( )
| A.σ键比π键重叠程度大,形成的共价键强 |
| B.两个原子之间形成共价键时,最多有一个σ键 |
| C.气体单质中,一定有σ键,可能有π键 |
| D.N2分子中有一个σ键,2个π键 |
下列说法不正确的是
| A.发展核电、煤中加入生石灰、利用二氧化碳制造全降解塑料都能有效减少环境污染 |
| B.物质变化中炭化、钝化、皂化、酯化、熔化都属于化学变化 |
| C.氢键、分子间作用力、离子键和共价键均为微粒间的相互作用力 |
| D.农业废弃物、城市工业有机废弃物及动物粪便中都蕴藏着丰富的生物质能 |
下列关于化学键的说法,正确的是
| A.化合物中一定没有非极性键 |
| B.单质中不可能含有离子键 |
| C.金属元素与非金属元素间形成的键均是离子键 |
| D.CO2、CH4分子中每个原子最外层均形成了8电子结构 |
下列过程中,破坏的作用力相同的是
| A.干冰升华和碘升华 | B.HCl溶于水和NaCl溶于水 |
| C.石英熔化和冰熔化 | D.NH4Cl受热分解和HI受热分解 |
下列说法正确的是
A.分子内共价键越强,分子越稳定,其熔沸点也越高
B.C、H、O、N四种元素组成的化合物一定是离子化合物
C.HF分子间存在着氢键,所以HF比HCl稳定
D.由原子构成的晶体可能是原子晶体,也可能是分子晶体
下列说法正确的是
A.质子数为6,中子数为7的原子的元素符号可表示为 |
| B.H2、SO2、CO三种气体都可用浓硫酸干燥 |
| C.共价化合物溶于水,分子内共价键被破坏,单质溶于水,分子内共价键不被破坏 |
| D.陶瓷、玻璃、水泥、大理石的主要成分都是硅酸盐 |
下列有关作用力的说法正确的是( )
| A.金属键、离子键、分子间作用力、氢键都没有方向性和饱和性 |
| B.键能、金属的原子化热、晶格能分别可以衡量氢键、金属键、离子键的强弱 |
| C.离子键、金属键、氢键、范德华力本质上都是静电作用 |
| D.乙酸、丙醇、丙酮的沸点都比丁烷高是因为前三者分子间都存在氢键 |
砷(As)在地壳中含量不大,但砷的化合物却是丰富多彩。
(1)基态砷原子的电子排布式为 ;砷与溴的第一电离能较大的是 。
(2)AsH3是无色稍有大蒜味气体。AsH3的沸点高于PH3,其主要原因是 。
(3)Na3AsO4可作杀虫剂。AsO43-的空间构型为 ,与其互为等电子体的一种分子为 。
(4)某砷的氧化物俗称“砒霜”,其分子结构如图所示。该化合物的分子式为 ,As原子采取 杂化。
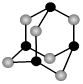
(5)GaAs等是人工合成的新型半导体材料,其晶体结构与金刚石相似。GaAs晶体中,每个As与 个Ga相连,As与Ga之间存在的化学键有 (填字母)。
| A.离子键 | B.σ键 | C.π键 | D.氢键 E.配位键 F.金属键 G.极性键 |
“暖冰”是韩国首尔大学科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成的。某老师在课堂上做了一个如右图所示的实验,发现烧杯中溶液褪色。若将烧杯中的溶液换成含有少量KSCN的FeCl2溶液,则溶液呈血红色。则下列说法中不正确的是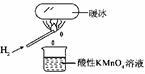
A水凝固形成20~C时的“暖冰”所发生的变化是化学变化
B.在电场作用下,水分子间更易形成氢键,因而可以制得“暖冰”
C.该条件下H2燃烧生成了既具有氧化性又具有还原性的物质
D.该条件下H2燃烧的产物中可能含有一定量的H2O2
下列叙述正确的是
①任何化学反应都有反应热 ②化合物MgO、SiO2、Al2O3中化学键的类型相同 ③有些化学键断裂时吸收能量,有些化学键断裂时放出能量 ④PH3分子稳定性和沸点均低于NH3分子 ⑤O3和NO2都是共价化合物 ⑥有热量变化的过程一定有化学键的断裂与形成 ⑦单质中不可能有离子键 ⑧有化学键断裂的变化属于化学变化
| A.①④⑦ | B.②③ | C.③⑤ | D.②⑤⑥ |
试题篮
()