在下列化学反应中既有离子键、极性键、非极性键断裂,又有离子键、极性键、非极性键形成的是( )
| A.Cl2+H2O=HClO+HCl |
| B.Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑ |
| C.2Na2O2+2H2O=4NaOH+O2↑ |
D.NH4Cl+NaOH NaCl+NH3↑+H2O NaCl+NH3↑+H2O |
下列对分子结构叙述不正确的是( )
| A.H2O2分子中,两个O之间形成1对共用电子对 | B.N2的电子式是N┇┇N |
| C.CCl4和甲烷都是正四面体型分子 | D.CO2和CS2都是直线型分子 |
一定条件下,氨气与氟气发生反应:4NH3+3F2  NF3+3NH4F,其中NF3分子构型与NH3相似。下列有关说法错误的是( )
NF3+3NH4F,其中NF3分子构型与NH3相似。下列有关说法错误的是( )
| A.NF3是极性分子 |
| B.NF3既是氧化产物,又是还原产物 |
| C.NH4F中既含有离子键又含有共价键 |
| D.上述反应中,反应物和生成物均属于分子晶体 |
科学家已经合成出氧的一种单质O4,下列关于该物质的说法正确的是 ( )
| A.摩尔质量是64g | B.是氧的一种同位素 |
| C.分子中含有离子键 | D.是氧的一种同素异形体 |
下列说法或表达正确的是
| A.乙醇、糖类和蛋白质都是人体必需的营养物质 |
B.NH41的电子式: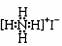 |
| C.石油是混合物,其分馏产品汽油也是混合物 |
| D.陶瓷、水晶、水泥、玻璃都属于硅酸盐 |
下列说法正确的是
| A.含极性键的分子一定是极性分子 |
| B.键能越小,表示该分子受热越难分解 |
| C.在分子中,两个成键原子间的距离叫做键长 |
| D.H-Cl的键能为431.8kJ/mol,H-I的键能为298.7kJ/mol,说明HCl分子比HI分子稳定 |
a为乙二胺四乙酸(EDTA),易与金属离子形成螯合物。b为EDTA与Ca2+形成的螯合物。下列叙述正确的是( )

A.a和b中的N原子均为sp3杂化
B.b中Ca2+的配位数为4
C.b含有分子内氢键
D.b含有共价键、离子键和配位键
下列每组分子主要能形成分子间氢键的是( )
| A.HClO4 和 H2SO4 | B.CH3COOH和H2Se |
| C.C2H5OH和NaOH | D.H2O2和HNO3 |
下列说法正确的是
| A.福岛核电站泄漏的放射性物质131I和127I互为同位素,化学性质几乎相同 |
| B.分子晶体中,共价键键能越大,该分子晶体的熔、沸点一定高 |
| C.CO2、H2O、N2这些分子中所有原子都满足最外层为8电子的结构 |
| D.原子结构模型的演变经历了 : |

下列晶体熔化时不需要破坏化学键的是
| A.金刚石 | B.氟化镁 | C.冰醋酸 | D.金属钾 |
试题篮
()