下列有关实验的原理、方法和结论都正确的是
| A.将等体积、等pH的氢氧化钠溶液和氨水分别稀释相同倍数,氨水的pH变化大 |
| B.用CH3COOH溶液作导电性实验,灯光较暗,说明CH3COOH是弱电解质 |
| C.向滴有酚酞的Na2CO3溶液中逐滴加入Ba(NO3)2,红色逐渐褪去,说明Na2CO3溶液中存在水解平衡 |
| D.沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强 |
下列说法正确的是
| A.NaHCO3和Na2CO3混合溶液中,一定有 c(Na+)+c(H+)=c(OH-)+c(HCO3-) +c(CO32-) |
| B.浓度均为0.1 mol·L-1的下列溶液,pH由大到小排列顺序为 NaOH>Na2CO3>NaHSO4>(NH4)2SO4 |
| C.向冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小 |
| D.pH=3的硫酸与醋酸溶液,c(SO42-)与c(CH3COO-)之比为1∶2 |
对于(NH4)2SO4溶液,下列说法正确的是
A.溶液中存在电离平衡:(NH4)2SO4 2NH4+ + SO42- 2NH4+ + SO42- |
| B.向溶液中滴加少量浓硫酸,c(NH4+)与c(SO42-)均增大 |
| C.加水稀释,溶液中所有离子的浓度均减小 |
| D.溶液中:c(SO42-)=2c(NH4+) + 2c(NH3·H2O) |
下列说法正确的是
| A.中和等体积、等物质的量浓度盐酸和醋酸溶液,盐酸所需NaOH溶液多于醋酸 |
| B.常温下,20 LpH=12的Na2CO3溶液中含有的OH-离子数为0.2NA |
C.向0.1 mol/LCH3COOH溶液中加入少量CH3COONa固 体,溶液中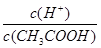 增大 增大 |
| D.一定温度下,10mL 0.50mol·L—1 NH4Cl溶液与20mL 0.25mol·L—1 NH4C1溶液含NH4+物质的量相同 |
已知:H2SO3的Ka1=1.3×10-2,Ka2=6.3×10-8;H2CO3的Ka1=4.2×10-7,Ka 2=5.6×10-11。现将标准状况下2.24L的CO2和2.24L的SO2分别通入两份150mL1mol/LNaOH溶液中,关于两溶液的比较下列说法正确的是
| A.c(HCO3-)<c(CO32-) |
| B.两溶液都能使酸性高锰酸钾溶液褪色 |
| C.c(HCO3-)>c(HSO3-) |
| D.c(CO32-)+c(HCO3-)=c(SO32-)+c(HSO3-) |
下列有关溶液中离子浓度的关系,不正确的是
| A.NaHCO3溶液中存在:c(OH-)=c(H2CO3)+c(H+) |
| B.常温下,pH=3的盐酸和pH=ll的氨水等体积混合后,溶液中:c(NH4+)>c(Cl-) |
| C.0.2 mol/LNH4Cl溶液与0.1 mol/L NaOH溶液等体积混合后,溶液中:c(NH4+)>c(Na+) |
| D.0.2 mol/L 的 CH3COOH 溶液中c(H+)小于0.1 mol/L 的 CH3COOH 中c(H+)的两倍 |
下列关于电解质溶液说法正确的是 ( )
| A.水的离子积常数Kw随着温度的升高而增大,说明水的电离是放热反应 |
| B.等体积的pH都为3的酸HA和HB分别与足量的Mg反应,HA放出的H2多,说明酸性:HA>HB |
| C.常温下,弱酸酸式盐NaHA溶液的pH=6,说明HA‾的电离程度大于其水解程度 |
| D.pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水的电离程度相同 |
下列叙述正确的是( )
| A.饱和的食盐水中通入HCl气体会有白色晶体析出 |
| B.同浓度的(NH4)2SO4、(NH4)2CO3、NH4Cl、NH4HSO4溶液中,c(NH4+)逐渐减小 |
| C.加入盐酸出现白色沉淀,则原溶液中一定含Ag+ |
| D.既能溶解Al(OH)3又能溶解H2SiO3的溶液可以大量共存NO3-、HCO3-、I-、K+ |
下列叙述中,正确的一组是( )
①SO2的水溶液能导电,所以SO2是电解质
②相同温度下,pH相同、体积相同的盐酸和醋酸溶液分别与足量的锌粒反应,醋酸生成的氢气较多
③在0.1mol/L CH3COOH溶液中加水稀释或加入少量CH3COONa晶体,溶液pH均增大
④室温下,将稀氨水逐滴加入到稀硫酸中,当pH=7时,c(NH4+)=c(SO42-)
⑤室温下,将pH=5的硫酸溶液稀释1000倍后,溶液中的SO42-与H+的物质的量浓度之比为1:20
| A.①③④ | B.②④⑤ | C.②③⑤ | D.②③④⑤ |
化学中常借助图像来表示某种变化过程,下列关于4个图像的说法正确的是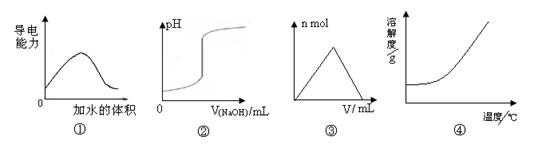
| A.图①可表示t℃时,冰醋酸稀释过程中溶液导电性的变化 |
| B.图②可表示向一定量盐酸中滴加一定浓度氢氧化钠溶液时,溶液pH的变化 |
| C.图③可表示向一定量明矾溶液中滴加一定浓度氢氧化钡溶液时,产生沉淀的物质的量的变化 |
| D.图④可表示所有的固体物质溶解度随温度的变化 |
下列叙述正确的是
| A.将SO2通入酸性高锰酸钾溶液中,溶液褪色,说明SO2具有漂白性 |
| B.相同温度下,完全中和相同PH、相同体积的氨水和NaOH溶液,所需相同浓度的盐酸体积相等 |
| C.0.1mol·L-1的酸式盐NaHA溶液中,c(Na+)=0.1mol·L-1≥c(A2-) |
D.向KI溶液中加入氯化银,沉淀逐渐变黄色,说明同温下 |
下列叙述正确的是
| A.当温度升高时,弱酸的电离平衡常数Ka变小 |
| B.某温度下的醋酸铵溶液呈中性,则溶液中必有c(H+)=c(OH-)=10-7mol·L-1 |
| C.pH=12氨水与pH=2盐酸等体积混合,则溶液中c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D.由Ksp(AgCl)>Ksp(AgI)可判断AgCl(s)+I-(aq)=AgI(s)+Cl-(aq)能发生 |
下列有关溶液的说法正确的是
| A.向10mLpH=3的酣酸溶液中加入10mLpH=l1的NaOH溶液,混合液的pH=7 |
| B.实验测定NH4HCO3溶液显碱性,CH3COONH4溶液显中性,说明酸性CH3COOH>HCO3 |
| C.NH4CI溶液加水稀释过程中c(H+)+c(NH3·H2O)=c(OH一) |
| D.向AgI沉淀中加人饱和KCl溶液,有白色沉淀生成,说明AgCl比AgI更难溶 |
下列有关说法正确的是
| A.Hg(l) + H2SO4(aq) = HgSO4(aq) + H2(g)常温下不能自发进行,说明△H<0 |
| B.用惰性电极电解1L1mol/L的CuSO4溶液,当阴极析出3.2 g铜时,加入0.05 molCu(OH)2固体可将溶液恢复至原浓度 |
| C.已知25℃时,Ksp(AgCl)=1.8×10-10、Ksp(Ag2CrO4)=2.0×10-12,所以AgCl的溶解度大于Ag2CrO4的溶解度 |
| D.25℃时,向0.1 mol/L CH3COOH溶液中加入少量CH3COONa固体,该溶液中水的电离程度将增大,且Kw不变 |
胆矾是一种常见的化合物,工业上它也是一种制取其它含铜化合物的原料,现有废铜(主要杂质为Fe)来制备胆矾。有人设计了如下流程: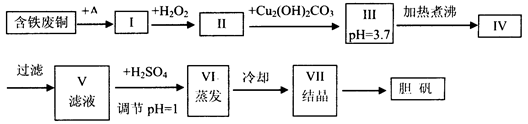
pH值控制可参考下列数据
| 物质 |
开始沉淀时的pH值 |
完全沉淀时的pH值 |
| 氢氧化铁 |
2.7 |
3.7 |
| 氢氧化亚铁 |
7.6 |
9.6 |
| 氢氧化铜 |
5.2 |
6.4 |
请根据上述流程回答下列问题:
(1)A可选用________(填字母)
a.稀H2SO4 b.浓H2SO4、加热 c.浓FeCl3溶液 d.浓HNO3
(2)Ⅰ中加H2O2的目的___________________________________________________。
(3)Ⅱ中加Cu2(OH)2CO3的目的是___________________________________,
其优点是_____________________________________________________________。
(4)Ⅲ加热煮沸时发生的化学反应的离子方程式为___________________________。
(5)V中加H2SO4调节pH=1是为了_________________________________________,
某工程师认为上述流程中所加的A物质并不理想,需作改进,其理由是______________,
若你是工程师,将对所加的A物质作何改进?请提出建议______________________。
试题篮
()