溴化碘(IBr)的化学性质很像卤素的单质,它能与大多数金属、非金属化合生成卤化物,它也能与水发生以下反应:IBr+H2O====HBr+HIO。下列有关IBr的叙述不正确的是( )
| A.在很多反应中IBr是强氧化剂 |
| B.IBr与水反应时既作氧化剂,又作还原剂 |
| C.IBr与AgNO3溶液反应会生成AgBr沉淀 |
| D.IBr与NaOH溶液反应时,生成NaBr和NaIO |
在如下图所示的装置中,a的金属性比氢要强,b为碳棒,关于此装置的各种叙述不正确的是( )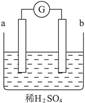
| A.碳棒上有气体放出,pH变大 |
| B.a是正极,b是负极 |
| C.导线中有电子流动,电子从a极到b极 |
| D.a极上发生了氧化反应 |
pH=1的两种酸溶液A、B各1 mL,分别加水稀释到1000mL,其pH值与溶液体积的关系如图,下列说法正确的是 ( )
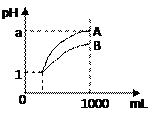 |
A.A、B两种酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液强
C.若1< a < 4,则A、B都是弱酸
D.若a = 4,则A是弱酸,B是强酸。
酸碱指示剂一般是有机弱酸(用Hln表示)或弱碱,其分子形式与电离出的ln—形式颜色不同,在pH值不同的溶液中至所以能表现出不同的颜色,是因为其电离平衡发生移动的结果。甲基橙是一种常用的酸碱指示剂,溶于水后发生如下电离:Hln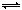 H++ln—,已知在pH<3.1的溶液中呈红色,在pH>4.4的溶液中呈黄色,下列判断中不正确的是 ( )
H++ln—,已知在pH<3.1的溶液中呈红色,在pH>4.4的溶液中呈黄色,下列判断中不正确的是 ( )
| A.Hln呈红色 |
B.ln—呈黄色 |
| C.遇pH值介于3.1~4.4的溶液可能呈橙色 |
| D.Hln呈黄色 |
常温下,向一定浓度的氨水中逐滴加入盐酸,关于溶液中各离子浓度大小关系叙述最准确的是 ( )
| A.c(Cl—)> c(NH4+) > c(H+) > c(OH—) |
| B.c c(NH4+) = c(Cl—) > c(H+) = c(OH—) |
| C.c(NH4+) > c(Cl—) > c(OH—) > c(H+) |
| D.以上说法都有可能 |
如果直接蒸干某些盐的溶液,则无法得到相应的盐晶体,在空气中直接蒸发下列盐的溶液时:①Al2(SO4)3、②Na2CO3③KCl ④CuCl2 ⑤NaHCO3,可以得到相应盐晶体(可以含有结晶水)的是 ( )
| A.①③⑤ | B.①②③ | C.②④ | D.①③④⑤ |
25℃时,下列各种溶液中碱性最强的是 ( )
| A.pH=12的溶液 |
B.c(H+)=1×10—13mol/L 的溶液 |
| C.c(OH-):c(H+)=1010的溶液 |
| D.c(OH-)=0.2mol/L的氨水 |
将物质的量浓度为Xmol/L的稀盐酸与物质的量浓度为Ymol/L的稀NaOH溶液等体积混合,所得溶液的pH=2(混合后体积为混合前之和),则X和Y的关系是( )
| A.X=Y+0.0l | B.X="2Y" | C.Y="2X" | D.X=Y+0.02 |
下面的是某同学实验报告中记录的一些内容:①用量筒量值25.00mLNaOH 溶液②用碱式滴定管量取20.00mL KMnO4溶液③用pH试试测得氨水pH=10.2 ④向Na2CO3溶液加入足量BaCl2溶液后,溶液的pH="7" ⑤用托盘天平称量所得沉淀质量为5.21g,其中不正确的是 ( )
| A.①②③④⑤ | B.①②③⑤ | C.②③④ | D.④⑤ |
一种矿泉水标签上印有主要矿物成份(单位:mg.L-1):Ca:60.00、K:39.00、Mg:3.100、Zn:0.08、F:0.02等,则对此矿泉水的叙述正确的是 ( )
①该矿泉水不导电
②该矿泉水导电
③该矿泉水是电解质
④该矿泉水是非电解质
| A.②③ | B.② | C.②④ | D.①④ |
莫尔盐[(NH4)2Fe(SO4)2·6H2O]常作氧化还原滴定法的基准物质,在0.1mol/L的该盐的溶液中,下列有关比较不正确的是( )
A.c(SO )> c(NH )> c(NH )>c(Fe2+)>c(H+)>c(OH-) )>c(Fe2+)>c(H+)>c(OH-) |
B.c(NH3·H2O)+c(NH )= 0.2mol/L )= 0.2mol/L |
| C.c(H+)= c(OH-)+c(NH3·H2O) |
D.2 c(SO )+ c(OH-)= c(NH )+ c(OH-)= c(NH )+2 c(Fe2+)+c(H+) )+2 c(Fe2+)+c(H+) |
下列有关滴定操作的顺序正确的是 ( )
①用标准溶液润洗滴定管 ②往滴定管中注入标准溶液
③检查滴定管是否漏水 ④滴定 ⑤洗涤
| A.⑤①②③④ | B.③⑤①②④ | C.⑤②③①④ | D.②①③⑤④ |
常温时,某溶液中由水电离出的H+和OH-的物质的量浓度乘职为1×10-26,该溶液中一定能大量存在的离子组是 ( )
| A.K+、Ba2+、Cl-、NO3- |
| B.Fe3+、Cu2+、Cl-、HCO3- |
| C.K+、Na+、SO32-、SO42- |
| D.Ca2+、Al3+、H+、NO3- |
试题篮
()