在一定条件下,密闭容器中进行的反应:H2 + I2  2HI对于下列示意图所表示的涵义解释正确的是( )
2HI对于下列示意图所表示的涵义解释正确的是( )
| A.反应开始时,容器中投入了H2、I2、HI三种气体 |
| B.0到t1时刻,反应向逆反应方向进行 |
| C.t1时刻后,正、逆反应的速率均为零 |
| D.t1时刻后,H2、I2、HI三种气体的浓度达到相等 |
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。
(1)在250C、101KPa时,3.2克甲醇(CH30H)完全燃烧生成CO2和液态水时放热72.576kJ,则能表示甲醇燃烧的热化学方程式为___________________。
(2)为探究反应原理,现进行如下实验,在体积为2 L的密闭容器中,充入2mol CO2和6mol H2,一定条件下发生反应:CO2(g)+3H2(g)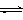 CH3OH(g)+H2O(g) △H=—49kJ/mol,测得CO2和H2O (g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) △H=—49kJ/mol,测得CO2和H2O (g)的浓度随时间变化如图所示。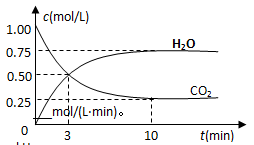
①从反应开始到平衡,氢气的平均反应速率v(H2)=__________mol/(L·min)。
②下列措施中能使n(H2O)/n(CO2)增大的是________。
A.升高温度 B.再充入3mol H2
C.将CH3OH (g)从体系中分离 D.充入He(g),使体系压强增大
某同学为试验CuS在不同酸中的溶解性,取4份黑色CuS粉末试样置于试管中,分别加入醋酸、浓盐酸、浓硫酸、浓硝酸溶液。观察到如下现象:
①CuS不溶于醋酸溶液;②CuS不溶于浓盐酸;③CuS不溶于浓硫酸;④CuS在浓硝酸中溶解,溶液变蓝,并有红棕色刺激性气体产生。
根据上述现象,该同学得出了以下结论,其中正确的是( )
| A.CuS不溶于弱酸,能溶于强酸 |
| B.CuS不溶于非氧化性酸,能溶于氧化性酸 |
| C.CuS溶于硝酸,是因为硝酸氧化性强于硫酸,S2-被氧化,使沉淀溶解平衡往溶解方向 移动 |
| D.CuS溶于硝酸,是因为硝酸的酸性大于硫酸和盐酸的酸性,S2-结合H+,放出H2S气体, |
使溶解沉淀平衡往溶解方向移动
PCl5(气)  PCl3(气) +Cl2(气) △H>0 当反应达到平衡时,下列措施:①降温②恒容通入惰性气体③增加Cl2的浓度④加压⑤加催化剂⑥恒压通入惰性气体,能提高PCl5质量分数的是
PCl3(气) +Cl2(气) △H>0 当反应达到平衡时,下列措施:①降温②恒容通入惰性气体③增加Cl2的浓度④加压⑤加催化剂⑥恒压通入惰性气体,能提高PCl5质量分数的是
| A.①②④ | B.①③④ | C.②③⑥ | D.③⑤⑥ |
已知某可逆反应:
mA(g) + nB(g)  pC(g) ∆H=" Q" kJ·mol-1,在密闭容器中进行,右图表示在不同时间t、温度T和压强P与生成物C的百分含量的关系曲线,下列判断正确的是
pC(g) ∆H=" Q" kJ·mol-1,在密闭容器中进行,右图表示在不同时间t、温度T和压强P与生成物C的百分含量的关系曲线,下列判断正确的是
| A.T1 <T2 P1>P2 m+n<P Q<0 | B.T1>T2 P1<P2 m+n>P Q>0 |
| C.T1<T2 P1<P2 m+n<P Q>0 | D.T1>T2 P1<P2 m+n>P Q<0 |
下列变化不能用勒夏特列原理解释的是
| A.红棕色的NO2加压后颜色先变深再变浅 |
| B.H2、I2、HI混合气体加压后颜色变深 |
| C.向H2S水溶液中加入NaOH有利于S2-增多 |
| D.打开汽水瓶,看到有大量的气泡逸出 |
对于已达到平衡状态的可逆反应:A+B C+D,若t1时增大压强,正、逆反应速率变化如图所示,下列有关A、B、C、D四种物质的状态叙述中正确的是( )
C+D,若t1时增大压强,正、逆反应速率变化如图所示,下列有关A、B、C、D四种物质的状态叙述中正确的是( )

A.A、B、C、D一定都是气体
B.A、B一定都是气体,C、D只有一种是气体
C.C、D一定都是气体,A、B只有一种是气体
D.C、D至少有一种是气体,A、B也至少有一种是气体
将0.5 mol SO2和0.2 mol O2置于密闭容器中发生反应:2SO2+O2 2SO3。下列关于该反应的说法正确的是
2SO3。下列关于该反应的说法正确的是
| A.最终可生成0.4 mol SO3 | B.当v正(O2)= v逆(SO2) = 0时一定达化学平衡 |
| C.升高温度反应速率减小 | D.缩小体积增大压强反应速率增大 |
某温度下,恒容密闭容器中发生如下可逆反应:2 E(g)  F(g) + x G(g)(正反应放热);若起始时E浓度为a mol/L,F、G浓度均为0,达平衡时E浓度为0.5amol/L,若E的起始浓度改为2amol/L,F、G 浓度仍为0,当达到新的平衡时,下列说法正确的是( )
F(g) + x G(g)(正反应放热);若起始时E浓度为a mol/L,F、G浓度均为0,达平衡时E浓度为0.5amol/L,若E的起始浓度改为2amol/L,F、G 浓度仍为0,当达到新的平衡时,下列说法正确的是( )
| A.升高温度时,正反应速率加快,逆反应速率减慢,平衡逆向移动 |
| B.若x=1,新平衡下E转化率为50% |
| C.若x=2,新平衡下F的平衡浓度为0.5a mol/L |
| D.若x=2,换成恒压容器,则达到平衡所需时间比恒容容器所需时间短 |
一定温度时,向容积为2L的密闭容器中充入一定量的SO2和O2,发生反应:2SO2(g)+O2(g) 2SO3(g) ∆H=−196kJ·moL−1,一段时间后达平衡,反应过程中测定的部分数据见下表:
2SO3(g) ∆H=−196kJ·moL−1,一段时间后达平衡,反应过程中测定的部分数据见下表:
| 反应时间/min |
n(SO2)/mol |
n(O2)/mol |
| 0 |
2 |
1 |
| 5 |
1.2 |
|
| 10 |
|
0.4 |
| 15 |
0.8 |
|
下列说法不正确的是
A.反应在前5min的平均速率为v (SO2)=0.08mol·L−1·min−1
B.保持温度不变,向平衡后的容器中再充入0.2molSO2和0.2mol SO3时,v (正)>v (逆)
C.保持其他条件不变,若起始时向容器中充入2molSO3,达平衡时吸收78.4kJ的热量
D.相同温度下,起始时向容器中充入1.5mol SO3,达平衡时SO3的转化率为40%
某一反应物在一定条件下的平衡转化率为25.3%,当使用了催化剂时,其转化率为
| A.大于25.3% | B.小于25.3% | C.等于25.3% | D.不能确定 |
体积相同的甲、乙两个容器中,分别充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2+O2 2SO3并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为
2SO3并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为
| A.等于p% | B.大于p% | C.小于p% | D.无法判断 |
在恒温时,一固定容积的容器内发生如下反应:2NO2(g) N2O4(g) 达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数
N2O4(g) 达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数
| A.不变 | B.增大 | C.减小 | D.无法判断 |
试题篮
()