一定条件下,体积为10L的密闭容器中,1molX和1mol Y进行反应:2X(g)+2Y(g) Z(g),经60s达到平衡,生成0.3mol Z.下列说法正确的是( )
Z(g),经60s达到平衡,生成0.3mol Z.下列说法正确的是( )
A.以X浓度变化表示的反应速率为0.001mol/(Ls)
B.将容器体积变为20L,Z的平衡浓度变为原来的1/2
C.若增大压强,则物质Y的转化率减小
D若升高温度,X的体积分数增大,则正反应的△H>0
一定条件下,合成氨反应达到平衡时,测得混合气体中氨气的体积分数为20.0%,与反应前的体积相比,反应后体积缩小的百分率是( )
| A.16.7% | B.20.0% | C.80.0% | D.83.3% |
如图是恒温下某化学反应的反应速率随反应时间变化的示意图.下列叙述与示意图不相符合的是( )

| A.反应达平衡时,正反应速率和逆反应速率相等 |
| B.该反应达到平衡态Ⅰ后,增大反应物浓度,平衡发生移动,达到平衡态Ⅱ |
| C.该反应达到平衡态后,减小反应物浓度,平衡发生移动,达到平衡态Ⅱ |
| D.同一种反应物在平衡态Ⅰ和平衡Ⅱ时浓度不相等 |
在一定温度下体积固定的密闭容器中,当下列物理量:①混合气体的压强 ②气体的总物质的量③混合气体的密度④B的物质的量浓度不再变化时,能表明可逆反应A(s)+2B(g)⇌C(g)+D(g)已达平衡的是( )
| A.①② | B.①④ | C.③④ | D.只有④ |
下列事实中,不能用平衡移动原理解释的是
| A.开启啤酒瓶后,瓶中马上泛起大量泡沫 |
B.对CO(g)+NO2(g) CO2(g)+NO(g)平衡体系增大压强可使其颜色变深 CO2(g)+NO(g)平衡体系增大压强可使其颜色变深 |
| C.常温下,将1mLpH=3的醋酸溶液加水稀释到100mL,测得其pH<5 |
| D.实验室中常用排饱和食盐水的方法收集氯气 |
低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:发生的化学反应为:
2NH3(g)+NO(g)+NO2(g) 2N2(g)+3H2O(g) △H<0
2N2(g)+3H2O(g) △H<0
在恒容的密闭容器中,下列有关说法正确的是( )
| A.平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 |
| B.平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小 |
| C.其他条件不变,充入惰性气体,正逆反应速率均不发生变化,平衡不移动 |
| D.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 |
某化学反应中,反应混合物A、B、C的物质的量浓度(c)与时间(t)关系如下表所示:
下列说法正确的是:
A.该反应的化学方程式为A 2B+C
2B+C
B.4min末A的转化率约为31%
C.4~6min时,反应停止了
D.正反应是吸热反应
在一密闭容器中,反应aA(气) bB(气)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )
bB(气)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )
| A.平衡向逆反应方向移动了 | B.物质B的质量分数增加了 |
| C.物质A的转化率减少了 | D.a>b |
下列事实中不能用勒夏特列原理加以解释的是( )
| A.压缩氢气与碘蒸气反应的平衡混合气体,颜色变深 |
| B.浓氨水中加入氢氧化钠固体时产生较多的刺激性气味的气体 |
| C.夏天,打开啤酒瓶时会在瓶口逸出气体 |
| D.将盛有二氧化氮和四氧化二氮混合气的密闭容器置于冷水中,混合气体颜色变浅 |
下列对化学平衡移动的分析中,不正确的是 ( )
(1)已达平衡的反应

 ,当增加反应物物质的量时,平衡一定向正反应方向移动
,当增加反应物物质的量时,平衡一定向正反应方向移动
(2)已达平衡的反应

 ,当增大
,当增大 的浓度时,平衡向正反应方向移动,
的浓度时,平衡向正反应方向移动, 的转化率一定升高
的转化率一定升高
(3)有气体参加的反应达平衡时,若减小反应器容积时,平衡一定向气体体积增大的方向移动
(4)有气体参加的反应达平衡后,在恒压反应器中充入稀有气体,平衡一定不移动
| A.(1)(4) | B.(1)(2)(3) |
| C.(2)(3)(4) | D.(1)(2)(3)(4) |
臭氧是理想的烟气脱硝试剂,其脱硝反应为2NO2(g)+O3(g) N2O5(g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是
N2O5(g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是
| A |
B |
C |
D |
 |
 |
 |
 |
| 0~3s内,反应速率v(O3)=0.2mol·L-1·s-1 |
降低温度,平衡常数增大 |
t1时仅加入催化剂,平衡正向移动 |
达平衡时,仅改变x,则x为c(O2) |
(1)在一定条件,可逆反应:mA+nB pC达到平衡状态。
pC达到平衡状态。
①若A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡向______(填“正”或“逆”)反应方向移动。
②若A、B、C均为气体,且m+n<p,加热后,可使混合气体平均摩尔质量增加,则正反应是______(填“吸热”或“放热”)反应。
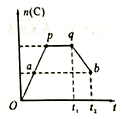
③若在反应过程中,C的物质的量n(C)随时间的变化关系如右图所示(从t1时间开始对反应体系升高温度)。则a、b两点的正反应速率:v(a)______v(b)(填“>”、“<”或“=”);
(2)Na2CO3溶液呈碱性,其原因是(用离子方程式表示)___________________;由同浓度的Na2CO3和NaHCO3组成的混合溶液中离子浓度由大到小的顺序为____________________;
(3)某温度下,纯水的c(H+)=3×10-7mol/L,Na2S和NaOH两溶液的pH均为12,则两溶液中由水电离出的c(OH-)的比值为_________________;
(4)下列事实一定能说明HF是弱酸的是__________;
①常温下NaF溶液的pH大于7 ②常温下0.1mol/L的HF溶液pH=2.3
③HF能与Na2CO3溶液反应,产生CO2气体 ④1mol/L的HF水溶液能使紫色石蕊试液变红
下列事实能用勒夏特列原理解释的是( )
A.FeCl3+3KSCN Fe(SCN)3+3KCl平衡体系中加入少量KSCN固体,溶液颜色加深
Fe(SCN)3+3KCl平衡体系中加入少量KSCN固体,溶液颜色加深
B.工业合成氨中,将氨气液化分离
C.A、B两支试管中分别加入等体积5%的H2O2溶液,在B试管中加入2~3滴FeCl3溶液,B中试管中产生气泡快
D.对于反应2NO2(g) N2O4(g) △H<0,升高温度可使体系颜色变深
N2O4(g) △H<0,升高温度可使体系颜色变深
在密闭容器中,一定条件下进行如下反应2NO(g)+2CO(g) N2(g)+2CO2(g),△H=-373.2kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
N2(g)+2CO2(g),△H=-373.2kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
| A.加催化剂同时升高温度 | B.加催化剂同时增大压强 |
| C.升高温度同时充入N2 | D.降低温度同时增大压强 |
(1)采取一定措施可防止钢铁腐蚀。下列装置中的烧杯里均盛有等浓度、等体积的NaCl溶液。
①在abc装置中能保护铁的是 (填字母)
②若用d装置保护铁,X极的电极材料应是 (填名称)
 |
(2)25℃时有关物质的溶度积如下:Ksp[Mg(OH)2]=5.61×10-12,Ksp[Fe (OH)3]=2.64×10-39
25℃时,向含有Mg2+,Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Fe3+)= 。
高炉炼铁是冶炼铁的主要方法,发生的主要反应为:
Fe2O3(s)+3CO(g)  2Fe(s)+3CO2(g) ΔH =" a" kJ·mol-1
2Fe(s)+3CO2(g) ΔH =" a" kJ·mol-1
(3)已知:①Fe2O3(s)+ 3C(石墨) = 2Fe(s)+3CO(g) ΔH1=" +" 489.0 kJ·mol-1
②C(石墨)+CO2(g)= 2CO(g)ΔH2 =" +" 172.5 kJ·mol-1则a = kJ·mol-1。
(4)冶炼铁反应的平衡常数表达式K = ,温度升高后,K值 (填“增大”、“不变”或“减小”)。
(5)在T℃时,该反应的平衡常数K=64,在 2L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
| |
Fe2O3 |
CO[ |
Fe |
CO2 |
| 甲/mol |
1.0 |
1.0 |
1.0 |
1.0 |
| 乙/mol |
1.0 |
2.0 |
1.0 |
1.0] |
① 甲容器中CO的平衡转化率为 。
② 下列说法正确的是 (填字母)。
a.若容器内气体密度恒定时,标志反应达到平衡状态
b.增加Fe2O3可以提高CO的转化率
c.甲容器中CO的平衡转化率大于乙的平衡转化率
d.甲、乙容器中,CO的平衡浓度之比为2∶3
试题篮
()