可逆反应:3A(g)  3B(?)+ C(?);△H>0,升高温度,气体的平均相对分子质量变小, 则下列判断正确的是
3B(?)+ C(?);△H>0,升高温度,气体的平均相对分子质量变小, 则下列判断正确的是
| A.B和C一定都是固体 | B.B和C一定都是气体 |
| C.若C为固体,则B一定是气体 | D.B和C不可能都是气体 |
在一密闭容器中,反应aA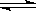 bB达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡后,A的浓度变为原来的60%,则
bB达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡后,A的浓度变为原来的60%,则
| A.A一定是气体 | B.平衡向正反应方向移动了 |
| C.物质B的质量分数增加了 | D.a<b |
在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g) nY(g),ΔH=Q kJ/mol。反应达到平衡时,Y的物质的量浓度与温度、容器体积的关系如下表所示:
nY(g),ΔH=Q kJ/mol。反应达到平衡时,Y的物质的量浓度与温度、容器体积的关系如下表所示:
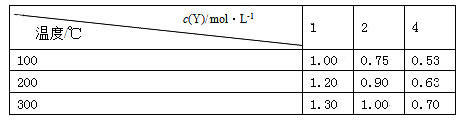
下列说法正确的是( )
| A.m>n |
| B.温度不变,压强增大,Y的质量分数减少 |
| C.Q<0 |
| D.体积不变,温度升高,平衡向逆反应方向移动 |
下列事实不能用平衡移动原理来解释的是( )
| A.打开啤酒瓶盖,产生大量气泡 |
| B.稀释CH3COOH时,溶液中CH3COO—数目增多 |
| C.工业合成氨常用500℃左右的温度 |
| D.热的纯碱溶液的去污效果比冷的好 |
某化学反应中,反应混合物A、B、C的物质的量浓度(c)与时间(t)关系如下表所示:
| |
初始 |
2 min |
4 min |
6 min |
| c (A)(mol/L) |
1.45 |
1.28 |
1.00 |
1.00 |
| c (B)(mol/L) |
0.38 |
0.72 |
1.28 |
1.28 |
| c (C)(mol/L) |
0.095 |
0.18 |
0.32 |
0.32 |
下列说法正确的是( )
A.该反应的化学方程式为A = 2B+C
B.4 min末A的转化率约为31%
C.4~6min时,反应停止了
D.正反应是吸热反应
某温度下的定容密闭容器中,进行可逆反应:A(s)+2B(g)  C(g)+D(g),当下列物理量不发生变化时: ①混合气体的密度 ②容器内气体的压强 ③混合气体的平均相对分子质量 ④B的物质的量浓度 则能表明该反应一定已达到平衡状态的是( )
C(g)+D(g),当下列物理量不发生变化时: ①混合气体的密度 ②容器内气体的压强 ③混合气体的平均相对分子质量 ④B的物质的量浓度 则能表明该反应一定已达到平衡状态的是( )
| A.只有④ | B.②③ | C.②③④ | D.①③④ |
下列事实不能用勒夏特列原理来解释的是( )
| A.高压有利于氢气与氮气合成氨 |
| B.实验室中常用排饱和食盐水的方法收集Cl2 |
| C.用V2O5催化二氧化硫氧化为三氧化硫 |
| D.Cl2在水中的溶解度大于在饱和NaCl溶液中的溶解度 |
将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s) 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。

①b<f;②915℃、2.0MPa时E的转化率为60%;③该反应的ΔS>0;④K(1000℃)>K(810℃)
上述①~④中正确的有( )
| A.4个 | B.3个 | C.2个 | D.1个 |
温度为T时;向2.0 L恒容密闭容器中充入1.0 mol PCl5;反应PCl5(g)  PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
| t/s |
0 |
50 |
150 |
250 |
350 |
| n(PCl3)/mol |
0 |
0.16 |
0. 19 |
0.20 |
0.20 |
下列说法正确的是( )
A.反应在前50 s的平均速率v(PCl3)="0.0032" mol·L-1·s-1
B.保持其他条件不变;升高温度;平衡时c(PCl3)="0.11" mol·L-1;则反应的ΔH<0
C.相同温度下;起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3和0.20 mol Cl2;反应达到平衡前v(正)>v(逆)
D.相同温度下;起始时向容器中充入2.0 mol PCl3和2.0 mol Cl2;达到平衡时;PCl3的转化率小于80%
化学中常用图像直观地描述化学反应的进程或结果。下列对图像的描述正确的是
A.根据图①可判断可逆反应A2(g)+3B2(g) 2AB3(g),正反应是吸热反应 2AB3(g),正反应是吸热反应 |
B.图②表示压强对反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强大 3C(g)+D(s)的影响,乙的压强大 |
| C.图③可表示乙酸溶液中通入氨气至过量的过程中溶液导电性的变化 |
| D.根据图④可知,若除去CuSO4溶液中的Fe3+,可向溶液中加入CuO,调节pH在4~5之间即可 |
温度为t ℃,压强为1.01×106Pa的条件下,某密闭容器内,下列反应达到化学平衡:A(g)+B(g)  3C,测得此时c(A)=0.022 mol·L-1;压缩容器使压强增大到2.02×106 Pa,第二次达到平衡时,测得c(A)=0.05 mol·L-1;若继续压缩容器,使压强增大到4.04×107 Pa,第三次达到平衡时,测得c(A)=0.075 mol·L-1,则下列关于C物质状态的推测正确的是( )
3C,测得此时c(A)=0.022 mol·L-1;压缩容器使压强增大到2.02×106 Pa,第二次达到平衡时,测得c(A)=0.05 mol·L-1;若继续压缩容器,使压强增大到4.04×107 Pa,第三次达到平衡时,测得c(A)=0.075 mol·L-1,则下列关于C物质状态的推测正确的是( )
A.C为非气态 B.C为气态
C.第二次达到平衡时C为气态 D.第三次达到平衡时C为气态
在一个固定体积的密闭容器中,保持一定温度,进行以下反应:H2(g)+I2(g)  2HI(g)。已知起始时加入1 mol H2和2 mol I2(g),当达到平衡时H2的体积分数为φ。下列四种情况分别投入上述容器,且始终保持原温度,平衡时H2的体积分数也为φ的是( )
2HI(g)。已知起始时加入1 mol H2和2 mol I2(g),当达到平衡时H2的体积分数为φ。下列四种情况分别投入上述容器,且始终保持原温度,平衡时H2的体积分数也为φ的是( )
| A.2 mol H2(g)和1 mol I2(g) | B.3 mol HI(g) |
| C.2 mol H2(g)和2 mol I2(g) | D.1 mol I2(g)和2 mol HI(g) |
已知反应A2(g)+2B(s) A2B2(g) △H<0,下列说法正确的是( )
A2B2(g) △H<0,下列说法正确的是( )
| A.升高温度,化学平衡向正反应方向移动 |
| B.增大压强,正反应与逆反应速率均增大 |
| C.增大压强,化学平衡向正反应方向移动 |
| D.增大B的物质的量,化学平衡向正反应方向移动 |
一定条件下,下列反应中水蒸气含量随反应时间的变化趋势符合如图的是( )
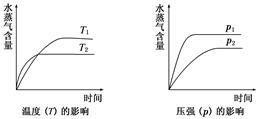
A.CO2(g)+2NH3(g) CO(NH2)2(s)+H2O(g)ΔH<0 CO(NH2)2(s)+H2O(g)ΔH<0 |
B.CO2(g)+H2(g) CO(g)+H2O(g)ΔH>0 CO(g)+H2O(g)ΔH>0 |
C.CH3CH2OH(g) CH2===CH2(g)+H2O(g)ΔH>0 CH2===CH2(g)+H2O(g)ΔH>0 |
| D.2C6H5CH2CH3(g)+O2(g)===2C6H5CH===CH2(g)+2H2O (g)ΔH<0 |
试题篮
()