下列叙述中一定能判断某化学平衡发生移动的是( )
| A.混合物中各组分的浓度改变 | B.正、逆反应速率改变 |
| C.混合物中各组分的含量改变 | D.混合体系的压强发生改变 |
一定条件下合成乙烯6H2(g) + 2CO2(g)  CH2=CH2(g) + 4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法错误的是
CH2=CH2(g) + 4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法错误的是

| A.生成乙烯的速率:v(M)有可能小于v(N) |
| B.平衡常数:KM >KN |
| C.催化剂可能会影响CO2的平衡转化率 |
| D.若投料比n(H2) : n(CO2)=3: 1,则图中M点时,乙烯的体积分数为7.7% |
对于化学反应的限度的叙述不正确的是( )
| A.任何可逆反应都有一定的限度 |
B.对于反应2SO2(g)+O2(g) 2SO3(g)只有达到限度时才有2v(O2)=v(SO3) 2SO3(g)只有达到限度时才有2v(O2)=v(SO3) |
C.对于反应2SO2(g)+O2(g) 2SO3(g)达到限度时,增大容器容积能减小正反应速率 2SO3(g)达到限度时,增大容器容积能减小正反应速率 |
| D.化学反应达到限度时,正逆反应速率相等 |
以下物理量只与温度有关的是
| A.合成氨工业中,氢气的转化率 | B.醋酸钠的水解程度 |
| C.水的离子积 | D.氢气的溶解度 |
向某恒容密闭容器中充入一定量C02和H2,发生反应: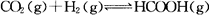 测得平衡体系中C02的百分含量(C02%)与反应温度变化的关系如图所示。下列物理量 中,a点大于b点的是
测得平衡体系中C02的百分含量(C02%)与反应温度变化的关系如图所示。下列物理量 中,a点大于b点的是

①:正反应速率 ②逆反应速率 ③HCOOH(g)的浓度 ④对应温度时的平衡常数
| A.①② | B.①③ | C.②④ | D.③④ |
在一密闭容器中,反应 :aA(气)  bB(气)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则
bB(气)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则
| A.平衡向逆反应方向移动了 | B.物质A的转化率减少了 |
| C.物质B的质量分数增加了 | D.a>b |
一定条件下,在体积为10L的密闭容器中,1molX和1molY进行反应:2X(g)+Y(g) Z(g),经60s达到平衡,生成0.3molZ,下列说法正确的是
Z(g),经60s达到平衡,生成0.3molZ,下列说法正确的是
| A.若增大压强,平衡向正方向移动,平衡常数变大 |
| B.将容器体积变为20 L,Z的平衡浓度变为0.015mol/L |
| C.达到平衡时X浓度为0.04 mol/L |
| D.若升高温度,X的体积分数增大,则该反应的DH>0 |
在一密闭容器中进行如下反应:3H2(气)+N2(气) 2NH3(气),已知反应过程中某一时 刻 H2、N2、NH3的浓度分别为 0.3mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是( )
2NH3(气),已知反应过程中某一时 刻 H2、N2、NH3的浓度分别为 0.3mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是( )
| A.H2为 0.6mol/L、N2为 0. 2mol/L | B.NH3为 0.25mol/L |
| C.N2、NH3均为 0.15mol/L | D.NH3为 0.4mol/L |
可逆反应2SO2 (g)+ O2 (g)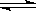 2SO3(g)达到平衡的标志是
2SO3(g)达到平衡的标志是
① 消耗2 mol SO2的同时生成2 mol SO3
②SO2、O2与SO3的物质的量之比为2∶1∶2
③ 反应混合物中,SO3的质量分数不再改变
| A.①② | B.①③ | C.只有③ | D.只有① |
对于反应2CO(g)+ O2(g) 2CO2(g)(ΔH<0),在一定条件下建立化学平衡后,下列各条件变化时,能使平衡向正方向移动的是
2CO2(g)(ΔH<0),在一定条件下建立化学平衡后,下列各条件变化时,能使平衡向正方向移动的是
| A.恒容通入少量He | B.恒容通入少量CO2 |
| C.升高温度 | D.缩小容器体积 |
下列各物质的颜色变化不是由平衡移动引起的是( )
| A.H2、I2、HI平衡混合气体加压颜色变深 |
| B.氯水光照颜色变浅 |
| C.NO2、N2O4混合气体加热颜色变深 |
| D.FeCl3和KSCN的混合溶液中加入FeCl3固体,溶液颜色加深 |
对已经达到化学平衡状态的下列反应2X(g)+Y2(g) Z(g),减小压强时,对反应产生的影响是( )
Z(g),减小压强时,对反应产生的影响是( )
| A.v正、v逆都减小,平衡逆向移动 | B.v正、v逆都增大,平衡正向移动 |
| C.v逆增大,v正减小,平衡逆向移动 | D.v逆减小,v正增大,平衡正向移动 |
下列生产、生活等实际应用,不能用勒夏特列原理解释的是( )
| A.实验室配制FeCl3溶液时,应向其中加入少量浓盐酸 |
| B.合成氨工业中使用铁触媒做催化剂 |
| C.饱和FeCl3溶液滴入沸水中可制得氢氧化铁胶体 |
| D.热的纯碱溶液去油污效果好 |
试题篮
()