在一定条件下,可逆反应A2+B2 2C,达到化学平衡状态,经测得平衡时:c(A2)="0.5" mol·L-1,c(B2)="0.1" mol·L-1,c(C)="1.6" mol·L-1,若A2,B2,C的起始浓度分别用a mol·L-1,b mol·L-1,c mol·L-1表示,要维持相同的平衡状态,请计算后完成下列问题:
2C,达到化学平衡状态,经测得平衡时:c(A2)="0.5" mol·L-1,c(B2)="0.1" mol·L-1,c(C)="1.6" mol·L-1,若A2,B2,C的起始浓度分别用a mol·L-1,b mol·L-1,c mol·L-1表示,要维持相同的平衡状态,请计算后完成下列问题:
(1)a、b应满足的关系是什么?
(2)计算a的取值范围。
某温度下在密闭容器中发生如下反应:
2M(g)+N(g) 2E(g)
2E(g)
开始时只充入2 mol E(g),达平衡时,混合气体的压强比起始时增大了20%。若开始时只充入2 mol M和1 mol N的混合气体,达平衡时M的转化率为多少?
在密闭容器中充入PCl5(g) PCl3(g)+Cl2(g),反应一段时间后又向体系中加入37Cl2含量较多的氯气,问在没有达平衡之前PCl3(g)中37Cl的含量是否会增加?为什么?
PCl3(g)+Cl2(g),反应一段时间后又向体系中加入37Cl2含量较多的氯气,问在没有达平衡之前PCl3(g)中37Cl的含量是否会增加?为什么?
在10L密闭容器中,放入8.0gSO3在一定条件下反应:2SO3(g)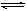 2SO2(g)+O2(g)并达到平衡状态,SO3的分解率为40%,求平衡混合气密度是相同条件下H2密度的多少倍?
2SO2(g)+O2(g)并达到平衡状态,SO3的分解率为40%,求平衡混合气密度是相同条件下H2密度的多少倍?
在一定条件下将物质的量相等的NO和O2混合发生如下反应:2NO+O2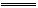 2NO2,2NO2
2NO2,2NO2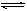 N2O4。所得混合气体中NO2的体积分数为40%,混合气体的平均相对分子质量。
N2O4。所得混合气体中NO2的体积分数为40%,混合气体的平均相对分子质量。
某化学反应2A(g) B(g)+D(g)在密闭容器中分别在下列四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
B(g)+D(g)在密闭容器中分别在下列四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
| 时间/min 反应温度/℃ 实验 |
1 |
10 |
20 |
30 |
40 |
50 |
60 |
|
| 1 |
800 |
1.0 |
0.80 |
0.67 |
0.57 |
0.50 |
0.50 |
0.50 |
| 2 |
800 |
c2 |
0.60 |
0.50 |
0.50 |
0.50 |
0.50 |
0.50 |
| 3 |
800 |
c3 |
0.92 |
0.75 |
0.63 |
0.60 |
0.60 |
0.60 |
| 4 |
820 |
1.0 |
0.20 |
0.20 |
0.20 |
0.20 |
0.20 |
0.20 |
(1)实验1中,反应在10至20分钟时间内平均化学反应速率为v(A)=_________。
(2)实验2中,A的初始浓度c2="_________" mol·L-1,反应经20 min就达到平衡,可推测实验2中隐含的条件可能是___________________________。
(3)若实验3的化学反应速率为v3,实验1的化学反应速率为v1,则v3________v1(填“>”“=”或“<”=,且c3________(填“>”“=”或“<”) 1.0 mol·L-1。
(4)比较实验4和实验1,可推测该反应的正反应是_________(填“吸热”或“放热”)反应。理由是_____________________________________________。
运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。
(1)已知:1/2O2(g)=1/2O2+(g)+1/2e- △H1=587.9kJ/mol K1
PtF6(g)+e-=PtF6-(g) △H2=-771.1kJ/mol K2
O2+PtF6-(s)=O2+(g)+PtF6-(g) △H3=482.2kJ/mol K3
则反应O2(g)+PtF6(g)=O2+PtF6-(s)的△H=________,K=_______(用K1、K2、K3表示)
(2)一定条件下,铁可以和CO2发生反应:Fe(s)+CO2(g)  FeO(s)+CO(g),已知该反应的平衡常数K 与温度T 的关系如图甲所示。
FeO(s)+CO(g),已知该反应的平衡常数K 与温度T 的关系如图甲所示。

①T℃、p Pa压强下,在体积为VL的容器中进行反应,下列能说明反应达到平衡状态的是_____。
A.混合气体的平均相对分子质量不再变化
B.容器内压强不再变化
C.v正(CO2)=v逆(FeO)
②T1温度下,向体积为VL的密闭容器中加入足量铁粉并充入一定量的CO2,反应过程中CO和CO2物质的量与时间的关系如图乙所示.则CO2的平衡转化率为_____,平衡时混合气体的密度与起始时气体的密度之比为_______。
(3)在恒温条件下起始时容积均为5L的甲、乙两密闭容器中(甲为恒容容器、乙为恒压容器),均进行反应:N2+3H2 2NH3,有关数据及特定平衡状态见下表。
2NH3,有关数据及特定平衡状态见下表。
| 容器 |
起始投入 |
达平衡时 |
|||
| 甲 |
2molN2 |
3molH2 |
0molNH3 |
1.5molNH3 |
同种物质的体积分数相同 |
| 乙 |
amolN2 |
bmolH2 |
0molNH3 |
1.2molNH3 |
起始时乙容器中的压强是甲容器的____倍。
在一密闭容器中发生反应: 2A(g)+B(g) E(g)
E(g)
(1)写出该反应的平衡常数表达式___________ ____,已知升高温度时,v(正)>v(逆),此时K值__ __(填“变大”“变小”或“不变”);该反应的△H_____0(填“>”、“=”、“<”);
(2)将1.0mol A和1.0mol B混合后装入2L容器中发生反应,E的物质的量的变化如图所示。
①3分钟内E的平均反应速率为________ _________;
②求此温度下该反应的平衡常数K= (结果保留小数后1位);
③请在图中画出5分钟内A的物质的量变化的曲线;
(3)已知在如图所示的变化中,平衡常数K保持不变,则在5~7min内引起E的物质的量变化的原因可能是____________(填编号)。
①降低了温度 ②升高了温度 ③使用了催化剂 ④增大了容器的体积 ⑤缩小了容器的体积 ⑥减少了A的物质的量。
在2L的密闭容器中放入4molN2O5,发生如下反应:2N2O5(g) 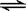 4NO2(g)+ O2(g)。反应5min后,测得N2O5转化了20%,求:
4NO2(g)+ O2(g)。反应5min后,测得N2O5转化了20%,求:
(1)υ(NO2)、υ(O2)分别为多少?
(2)5min时,N2O5占混合气体总体积的百分比是多少?
(要求写出计算过程)
吸热反应N2(g)+O2(g) 2NO(g),在2000℃时K=6.2×10-4。2000℃时,向10L密闭容器中放入3×10-3molNO、2.50×10-1molN2和4.00×10-2molO2。
2NO(g),在2000℃时K=6.2×10-4。2000℃时,向10L密闭容器中放入3×10-3molNO、2.50×10-1molN2和4.00×10-2molO2。
通过计算回答:
(1)此反应的初始状态是否为化学平衡状态?
(2)若非化学平衡状态,反应将向哪个方向进行以达到化学平衡状态?
某温度下,将氢气和碘蒸气各1mol的气态混合物充入10L的密闭容器中。发生反应H2(g)+I2(g) = 2HI(g)。2分钟后达到平衡后。测得C(H2)=0.08 mol.L-1,求(1)该反应的平衡常数。(2)2分钟内的H2的反应速率 (3)在上述温度下,该容器中若通入氢气和碘蒸气各3mol,求达到平衡后各物质的浓度(提示:K不变)。
一定温度下,在密闭容器中,发生反应: 2NO2 2NO+O2,经过一定时间后,测得混合气中NO2浓度为0.06 mol·L-1, O2的浓度为0.12 mol·L-1,且各物质的浓度不再发生变化。
2NO+O2,经过一定时间后,测得混合气中NO2浓度为0.06 mol·L-1, O2的浓度为0.12 mol·L-1,且各物质的浓度不再发生变化。
求:
(1)NO2的起始浓度? ;
(2)此时NO2的转化率? 。
将相同物质的量的SO3充入下面的两个容器中,已知甲容器有活塞可以上下移动,乙容器体积固定,在相同的温度、压强下开始发生反应:2SO3(g) 2SO2(g)+O2(g),在反应过程中维持体系温度不变。
2SO2(g)+O2(g),在反应过程中维持体系温度不变。
(1)求达到平衡状态时SO3气体的转化率的大小关系?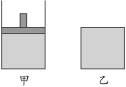 图2-2
图2-2
(2)达到平衡状态时分别充入一定量的Ar气,平衡是否会移动?会怎样移动?
试题篮
()