由乙醛和丁酸、乙酸乙酯三种有机物按一定比例组成的混合物中,若含氧的质量分数为A%,则此混合物中含碳的质量分数为( )
| A.6A%/7 | B.(1-A%)/7 | C.6(1-A%)/7 | D.(100-7A/6)% |
用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.2 g H2所含原子数目为NA |
| B.64 g SO2中含有的原子数为3 NA |
| C.常温常压下,11.2 L Cl2含有的分子数为0.5 NA |
| D.1 mol/L NaOH溶液中Na+的数目为NA |
在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。下表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
| 成分 |
质量(g) |
摩尔质量(g ·mol-1) |
| 蔗糖 |
25.00 |
342 |
| 硫酸钾 |
0.87 |
174 |
| 阿司匹林 |
0.17 |
180 |
| 高锰酸钾 |
0.316 |
158 |
| 硝酸银 |
0.075 |
170 |
(1)下列“鲜花保鲜剂”的成分中,属于非电解质的是__________。
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)硫酸钾在水中的电离方程式为______________________。
(3)配制1L上述“鲜花保鲜剂”所需的仪器有:量筒、玻璃棒、药匙、烧杯、__________、__________、_________。(在横线上填写所缺仪器的名称),需要高锰酸钾________mol
(4)在溶液配制过程中,下列操作对配制结果没有影响的是___________。
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(5)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为_______ mol/L。
NA为阿伏加德罗常数,下列叙述正确的是( )
| A. 11.2 L氧气中所含有的原子数为NA |
| B.标准状况下,22.4LCCl4所含分子数为NA |
| C.7.8g的Na2O2中含有的阴离子的数目为0.2NA |
| D.27gAl分别与足量的稀硫酸及氢氧化钠溶液反应失去的电子数都是3NA、 |
下列叙述中正确的是( )
| A.硫酸的摩尔质量是98g |
| B.铁原子的摩尔质量等于铁的相对原子质量 |
| C.标准状况下,22.4L的O2质量是32g |
| D.2gH2所含原子物质的量为1mol |
下列说法中错误的是
| A.0.3 mol H2SO4 | B.1 molH2O | C.0.5 mol硫 | D.3 mol氢原子 |
向一定量的NaOH固体中加入由硫酸铜和硫酸组成的混合物的溶液,充分搅拌,恰好完全反应,有蓝色沉淀生成,过滤,所得滤液的质量与加入的原混合物溶液的质量相等。则与硫酸铜反应的氢氧化钠和与硫酸反应的的氢氧化钠的物质的量之比为?
下列各组物质中,所含分子数相等的是( )
| A.10g H2和10g O2 | B.5.6g N2(标准状况)和 11g CO2 |
| C.9g H2O 和0.5mol Br2 | D.224mL H2(标准状况)和0.1mol N2 |
标准状况下4.48 L HCl的质量是__________g,将其溶于水配成100mL的溶液,所得溶液的物质的量浓度为 mol/L。
设NA表示阿伏加德罗常数的值,25℃,1.01×105 Pa时,64g SO2含有的分子数为
| A.2NA | B.NA | C.略小于NA | D.6.02×1022 |
用NA表示阿伏加德罗常数的值。下列判断正确的是
| A.常温常压下,32 g O3含有的氧原子数目为2 NA |
| B.56 g的Fe与足量的稀盐酸完全反应转移电子数为3NA |
| C.0.1 mol·L-1 Na2SO4溶液含有的钠离子数目为0.2 NA |
| D.标准状况下,22.4 L 四氯化碳(CCl4)含有的碳原子数目为NA |
设NA为阿伏加德罗常数的值,下列说法中正确的是
| A.0.1 mol溴苯中含有双键的数目为0.3NA |
| B.标准状况下,22.4 L己烷中含己烷分子数目为NA |
| C.1mol甲醇中含有C—H键的数目为4NA |
| D.标准状况下,11.2 L由CH4和C2H4组成的混合气体中含有氢原子的数目为2NA |
明矾石是制取钾肥和氢氧化铝的重要原料。明矾石的组成和明矾相似,此外还含有氧化铝和少量氧化铁杂质。具体实验步骤如下图所示: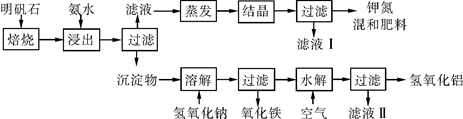
根据上述图示,完成下列填空。
(1)明矾石焙烧后用稀氨水浸出。配制500 mL稀氨水(每升含有39.20 g氨)需要取浓氨水(每升含有250.28 g氨)__________mL,用规格为__________mL量筒量取。
(2)写出沉淀物中所有物质的化学式:____________________。
(3)滤液Ⅰ的成分是水和________________________________。
(4)为测定混合肥料 K2SO4、(NH4)2SO4中钾的含量,完善下列步骤:
①称取钾氮肥试样并溶于水,加入足量__________溶液,产生白色沉淀。
②__________、__________、__________(依次填写实验操作名称)。
③冷却、称重。
④若试样为m g,沉淀的物质的量为n mol,则试样中K2SO4的物质的量为___________mol(用含m、n的代数式表示)。
1.5mol N2、H2的混合气体和1.5mol NH3相比较,下列叙述中,一定正确的是
| A.体积相等 | B.原子数相等 | C.分子数相等 | D.质量相等 |
试题篮
()