在t℃时,10L 0.4mol·L-1H2O2溶液发生催化分解:2H2O2 = 2H2O + O2↑,不同时刻测得生成O2的体积如下表,已知反应至6min时,H2O2分解了50%(已折算为标准状况)
| t /min |
0 |
2 |
4 |
6 |
| V(O2)/L |
0.0 |
9.9 |
17.2 |
V=? |
下列叙述正确的是(溶液体积变化忽略不计)
A.0~2min H2O2平均反应速率比4~6min慢
B.反应至6min时,共产生O2 44.8L
C.0~6min的平均反应速率 v(H2O2)≈3.3×10-2mol·L-1·min-1
D.反应至6min时,c(H2O2) = 0.3mol·L-1
恒温恒容下,向2 L密闭容器中加入MgSO4(s)和CO(g),发生反应:
MgSO4(s)+CO(g) MgO(s)+CO2(g)+SO2(g)
MgO(s)+CO2(g)+SO2(g)
反应过程中测定的部分数据见下表:
| 反应时间/min |
n(MgSO4)/mol |
n(CO)/mol |
n(SO2) / mol |
| 0 |
2.0 |
2.0 |
0 |
| 2 |
|
0.8 |
|
| 4 |
|
|
1.2 |
| 6 |
|
1.2 |
2.8 |
下列说法正确的是
A.0~2 min内的平均速率为υ(CO)=0.6 mol/(L·min)
B.4 min后,平衡移动的原因可能是向容器中加入了2.0 mol的SO2
C.若升高温度,反应的平衡常数变为1.0,则正反应为放热反应
D.其他条件不变,若起始时容器中MgSO4、CO均为1.0 mol,则平衡时n(SO2)="0.6" mol
下列对图象描述正确的是
| A.图①表示体积和pH值均相同的稀硫酸和醋酸,与足量的镁反应生成H2量的关系 |
| B.图②表示向NaOH溶液中滴加稀盐酸,溶液导电性变化的关系 |
C.图③表示2SO2(g)+O2(g) 2SO3(g)反应过程中,SO2和O2反应速率大小关系 2SO3(g)反应过程中,SO2和O2反应速率大小关系 |
| D.图④表示向氨水中滴加稀硫酸时,溶液的pH大小变化关系 |
在2 L的密闭容器中发生反应xA(g)+yB(g) zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是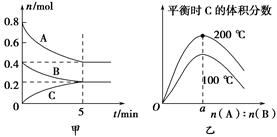
A.200 ℃时,反应从开始到平衡的平均速率v(B)=0.04 mol·L-1·min-1
B.200℃时,该反应的平衡常数为25 L2/mol2
C.当外界条件由200℃降温到100℃,原平衡一定被破坏,且正逆反应速率均增大
D.由图乙可知,反应xA(g)+yB(g) zC(g)的ΔH<0,且a=2
zC(g)的ΔH<0,且a=2
在一定温度下,将气体X和Y各1.6mol充入10L恒容密闭容器中,发生如下反应:
在反应过程中,X的物质的量与时间的关系如下表所示:
| t/min |
0 |
2 |
4 |
6 |
8 |
…… |
16 |
18 |
| n(X)/mol |
1.600 |
1.200 |
1.100 |
1.075 |
…… |
…… |
1.000 |
1.000 |
下列说法不正确的是
A.4~6min时间段内Z的平均反应速率为2.5×10-3mol/(L·min)
B.此温度下该反应的平衡常数K=1.44
C.达平衡后,升高温度, 减小,则正反应
减小,则正反应
D.若保持其他条件不变,再充入1.6mol Z,达新平衡后Z的体积分数不变
在一定温度下,将气体X和气体Y各0.16 mol充入10 L恒容密闭容器中,发生反应:X(g)+Y(g) ⇌2Z(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表:
下列说法不正确的是
| A.该温度下此反应的平衡常数K=1.44 |
| B.其他条件不变,升高温度,反应达到新平衡前V(逆)< V (正) |
| C.反应前2 min的平均速率v (Z)=4.0×10-3mol/(L·min) |
| D.其他条件不变,再充入0.2 mol Z,平衡时X的体积分数不变 |
温度为T时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,反应 PCl5(g) PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据如图
PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据如图
下列说法正确的是
| A.反应在前50 s 的平均速率v(PCl3)=0.0032 mol·L-1·s-1 |
| B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol·L-1,则反应的△H<0 |
| C.相同温度下,起始时向容器中充入2.0 mol PCl3和2.0 mol Cl2,达到平衡时,PCl3的转化率小于80% |
| D.相同温度下,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3和0.20 mol Cl2,反应达到平衡前v(正)>v(逆) |
在10L密闭容器中,A、B、C三种气态物质构成了可逆反应的体系;当在某一温度时,A、B、C物质的量与时间的关系如图一,C的百分含量与温度的关系如图二。

下列分析不正确的是:
A.0~4分钟时,A的平均反应速率为0.02mol/(L•min)
B.该反应的平衡常数表达式K=
C.由T1向T2变化时,正反应速率大于逆反应速率
D.此反应的正反应为放热反应
将4 molA气体和2 molB气体在2 L的容器中发生如下反应:2A(g)+B(g) 2C(g)。若经2s后测得C的浓度为0.6 mol/L,现有下列几种说法,其中正确的是
2C(g)。若经2s后测得C的浓度为0.6 mol/L,现有下列几种说法,其中正确的是
①用物质A表示的反应的平均速率为0.3 mol / (L·s)
②用物质B表示的反应的平均速率为0.6 mol / (L·s)
③2 s时物质A的转化率为70%
④2 s时物质B的浓度为0.7 mol / L
| A.①③ | B.①④ | C.②③ | D.③④ |
高炉炼铁中发生的基本反应之一如下:FeO(s)+CO(g)  Fe(s)+CO2(g)(正反应是吸热反应),其平衡常数可表示为: K = c(CO2)/c(CO),已知1100 ℃时K =0.263。
Fe(s)+CO2(g)(正反应是吸热反应),其平衡常数可表示为: K = c(CO2)/c(CO),已知1100 ℃时K =0.263。
(1)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比值______;平衡常数K值______(选填“增大”“减小”或“不变”)。
(2)1100 ℃时测得高炉中c(CO2)="0.025" mol/L、c(CO)="0.1" mol/L,在这 种情况下,该反应是否处于化学平衡状态______(选填“是”或“否”),此时,化学反应速率是v正______v逆(选填“大于”“小于”或“等于”);
(3) 目前工业上可用CO2来生产燃料甲醇,有关反应为:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=—49.0 kJ·mol-1。现向体积为1L的密闭容器中,充入1mol CO2和3mol H2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
CH3OH(g)+H2O(g) ΔH=—49.0 kJ·mol-1。现向体积为1L的密闭容器中,充入1mol CO2和3mol H2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
①从反应开始到平衡,氢气的平均反应速率v(H2)=_____________;
②若改变条件使平衡向正反应方向移动,则平衡常数______________(填序号)
| A.可能不变 | B.可能减小 | C.可能增大 | D.不变、减小、增大皆有可能 |
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)  2C(g)。
2C(g)。
各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和下图表示:
下列说法正确的是
A.10min内甲容器中反应的平均速率v(A)=0.025mol/(L·min)
B.由图可知:T1<T2,且该反应为吸热反应
C.x=1,若平衡时保持温度不变,改变容器体积平衡不移动
D.T1℃,起始时甲容器中充入0.5molA、1.5molB,平衡时A的转化率为25%
T℃时在2 L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积分数与时间的关系如图2所示。则下列结论正确的是
| A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol/(L·min) |
| B.平衡时容器内的压强为反应前的0.9倍 |
| C.保持其他条件不变,升高温度,反应的化学平衡常数K减小 |
| D.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强 |
PCl3和PCl5都是重要的化工原料。将PCl3(g)和Cl2(g)充入体积不变的2 L密闭容器中,在一定条件下发生下述反应,并于10 min时达到平衡:PCl3(g)+Cl2(g)  PCl5(g)。有关数据如下:
PCl5(g)。有关数据如下:
| |
PCl3(g) |
Cl2(g) |
PCl5(g) |
| 初始浓度/(mol/L) |
2.0 |
1.0 |
0 |
| 平衡浓度/(mol/L) |
c1 |
c2 |
0.4 |
下列判断不正确的是( )
A.10 min内,v(Cl2)=0.04 mol/(L·min)
B.当容器中Cl2为1.2 mol时,反应达到平衡
C.升高温度,反应的平衡常数减小,则平衡时PCl3的转化率变大
D.平衡后移走2.0 mol PCl3和1.0 mol Cl2,在相同条件下再达平衡时, c(PCl5)<0.2 mol/L
一定条件下,在体积为10 L的固定容器中发生反应:N2(g)+3H2(g)  2NH3(g) ΔH<0,反应过程如图:下列说法正确的是
2NH3(g) ΔH<0,反应过程如图:下列说法正确的是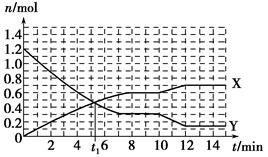
| A.t1 min时正、逆反应速率相等。 |
| B.X曲线表示NH3的物质的量随时间变化的关系 |
C.0~8 min,H2的平均反应速率v(H2)= mol·L-1·min-1 mol·L-1·min-1 |
| D.10~12 min,升高温度使反应速率加快,平衡正向移动 |
试题篮
()