反应N2O4(g) 2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。正确的是
2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。正确的是
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C. A、C两点气体的平均相对分子质量:A>C
D.由状态B到状态A,可以用加热的方法
对于下列各组反应,反应开始时,产生氢气速率最快的是
| A.70℃,将0.1 mol 镁粉加入到10 mL 6 mol•L﹣1 的硝酸溶液中 |
| B.60℃,将0.2 mol 镁粉加入到20 mL 3 mol•L﹣1 的盐酸溶液中 |
| C.60℃,将0.1 mol 镁粉加入到10 mL 3 mol•L﹣1 的硫酸溶液中 |
| D.60℃,将0.2 mol 铁粉加入到10 mL 3 mol•L﹣1 的盐酸溶液中 |
反应4NH3+5O2 4NO+6H2O在一定体积的密闭容器中进行,20s后NO的物质的量浓度增加了2mol/L,则下列反应速率正确的是
4NO+6H2O在一定体积的密闭容器中进行,20s后NO的物质的量浓度增加了2mol/L,则下列反应速率正确的是
| A.v (NO)="0.02" mol•(L•s)﹣1 |
| B.v (NO)=0.2mol•(L•s)﹣1 |
| C.v (NH3)="0.1" mol•(L•s)﹣1 |
| D.v (NH3)="0.01" mol•(L•s)﹣1 |
下面四个选项是四位同学在学习过化学反应速率和化学平衡理论以后,联系化工生产实际所发表的看法,你认为不正确的是
| A.化学反应速率理论可指导怎样提高原料的转化率 |
| B.化学反应速率理论可指导怎样在一定时间内快出产品 |
| C.化学平衡理论可指导怎样使用有限原料多出产品 |
| D.正确利用化学反应速率和化学平衡理论都可提高化工生产的综合经济效益 |
在一定条件下,A气体与B气体反应生成C气体。反应过程中,反应物与生成物的浓度随时间变化的曲线如图,则

(1)、该反应的化学方程式为: ;
(2)、t1 s时反应物A的转化率为: ;
(3)、0~t1 s内A的反应速率为v(A)= ;
将0.05molSO2(g)和0.03molO2(g)放入容积为1L的密闭容器中,反应2SO2(g)+O2(g) 2SO3(g),在一定条件下2min时达到平衡,测得c(SO3)=0.04mol·L-1。以下表述正确的是
2SO3(g),在一定条件下2min时达到平衡,测得c(SO3)=0.04mol·L-1。以下表述正确的是
| A.若恒容下,充入氮气,则c(SO3)小于0.04mol·L-1 |
| B.该条件下反应的平衡常数为1.6×103 |
| C.v(O2)= 0.02 mol·L-1.min-1 |
| D.使用催化剂若平衡没有移动,则该反应达到化学平衡状态 |
将4 mol A 气体和2 mol B 气体在2 L 的密闭容器中混合并在一定条件下发生如下反应2A(g)+B(g) 2C(g);△H <0。4 s(秒)后反应达到平衡状态,此时测得 C 的浓度为0.6 mol·L-1。下列说法中正确的是
2C(g);△H <0。4 s(秒)后反应达到平衡状态,此时测得 C 的浓度为0.6 mol·L-1。下列说法中正确的是
A.当A、B、C物质的量浓度之比为 2:1:2时,反应即达到平衡状态
B.4s内用物质B表示的反应速率为0.075 mol·L-1·s-1
C.达平衡后若通入一定量氦气,A的转化率降低
D.达平衡后若升高温度,C的浓度将增大
对反应4A+5B 4C+6D,以下化学反应速率的表示中,所表示反应速率最快的
4C+6D,以下化学反应速率的表示中,所表示反应速率最快的
A.v (A)=0.40mol•L-1•s-1 B.v (B)=0.48mol•L-1•s-1
C.v (C)=0.36mol•L-1•s-1 D.v (D)=0.55mol•L-1•s-1
反应4A(s)+3B(g)  2C(g)+D(g),经2min,B的浓度减少0.6 mol•L-1。对此反应速率的表示,正确的是
2C(g)+D(g),经2min,B的浓度减少0.6 mol•L-1。对此反应速率的表示,正确的是
①用A表示的反应速率是0.4 mol•L-1•min-1
②分别用B、C、D表示的反应速率其比值为3:2:1
③在2 min末的反应速率,用B表示是0.3 mol•L-1•min-1
④反应的过程中,只增加A的量,反应速率不变
A.①② B.③ C.① D.②④
反应4A(g)+5B(g) 4C(g)+6D(g) 在5L的密闭容器中进行反应,30min后,C的物质的量增加了0.30mol.下列叙述正确的是
4C(g)+6D(g) 在5L的密闭容器中进行反应,30min后,C的物质的量增加了0.30mol.下列叙述正确的是
A.30min中A的平均反应速率是0.010mol·L﹣1·min﹣1
B.容器中D的物质的量一定增加了0.45mol
C.容器中A、B、C、D的物质的量的比一定是4:5:4:6
D.容器中A的物质的量一定增加0.30mol
苯硫酚(PhSH)是一种用途广泛的有机合成中间体。工业上用常用氯苯(PhCl)和硫化氢(H2S)在高温下反应来制备苯硫酚,但会有副产物苯(PhH)生成。
I: PhCl(g)+H2S(g) PhSH(g)+HCl(g) △H1=—16.8kJ·mol-1
PhSH(g)+HCl(g) △H1=—16.8kJ·mol-1
II: PhCl(g)+H2S(g) ==PhH(g)+ HCl(g)+ S8(g) △H2
S8(g) △H2
回答下列问题:
(1)反应I为可逆反应,写出平衡常数的表达式K=_______________________,
反应II为不可逆反应,△H2=___________0。(填写“>”,“<”,“=”)

(2)上述两个反应的能量变化如图一所示,则在某温度时反应速度v(I)__________v(II)(填写“>”,“<”,“=”)
(3)现将一定量的氯苯和硫化氢置于一固定容积的容器中模拟工业生产过程,在不同温度下均反应20分钟测定生成物的浓度,得到图二和图三。
①请解释图二中两条曲线的变化_______________________。
②若要提高主产物苯硫酚的产量,可采取的措施是______________________。
(4)请根据图二、图三,画出恒温恒容条件下反应主产物苯硫酚的物质的量随时间变化的曲线图。

某密闭容器中,有A、B两种气体,反应按下式进行A(g)+B(g)=2C(g)反应经过2s后浓度不再发生变化时,测得容器中各物质的浓度分别为c(A)=0.5mol/L,c(B)=0.75 mol/L,c(C)=0.5 mol/L。
(1)B物质的起始浓度各为
(2)2s时A的转化率
(3)用物质A表示反应的平均速率
将固体NH4Br置于密闭容器中,在某温度下,发生下列可逆反应:NH4Br(s) 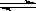 NH3(g)+HBr(g) 2HBr(g)
NH3(g)+HBr(g) 2HBr(g) 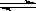 Br2(g)+H2(g),2min后,测得c(H2)=0.5mol/L,c(HBr)=4mol/L,若上述反应速率用
Br2(g)+H2(g),2min后,测得c(H2)=0.5mol/L,c(HBr)=4mol/L,若上述反应速率用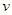 (NH3)表示,下列反应速率正确的是
(NH3)表示,下列反应速率正确的是
| A.0.5mol/(L·min) | B.2.5 mol/(L·min) |
| C.2 mol/(L·min) | D.5 mol/(L·min) |
一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。下列描述正确的是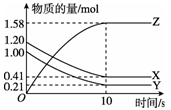
| A.反应开始到10 s时,用Z表示的反应速率为0.158 mol·(L·s)-1 |
| B.反应开始到10 s时,X的物质的量浓度减少了0.79 mol·L-1 |
| C.反应开始到10 s时,Y的转化率为39.5% |
D.反应的化学方程式为X(g)+Y(g) 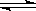 2Z(g) 2Z(g) |
试题篮
()