用6 g CaCO3与100 mL稀盐酸反应制取少量的CO2,反应过程中生成的CO2的体积(已折算为标准状况)随反应时间变化的情况如右图所示。下列说法正确的是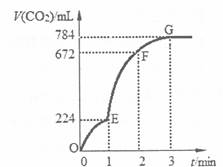
| A.OE段表示的平均反应速率最快,可能的原因是该反应是放热反应 |
| B.EF段用HC1浓度的减小表示的该反应的平均反应速率为0.2 mol/(L·min) |
| C.在F点收集到的CO2的体积最大 |
| D.在G点以后收集的CO2的量不再增多,原因是稀盐酸已反应完全 |
文献报道某课题组利用CO2催化氢化制甲烷的研究过程如下:
反应结束后,气体中检测到CH4和H2,滤液中检测到HCOOH,固体中检测到镍粉和Fe3O4。
CH4、HCOOH、H2的产量和镍粉用量的关系如右图所示(仅改变镍粉用量,其他条件不变):
研究人员根据实验结果得出结论:HCOOH是CO2转化为CH4的中间体,即:
由图可知,镍粉是反应Ⅰ、Ⅱ的催化剂,当镍粉用量从1mmol增加到10mmol,反应速率的变化情况是
| A.反应Ⅰ的速率增加,反应Ⅱ的速率不变 |
| B.反应Ⅰ的速率不变,反应Ⅱ的速率增加 |
| C.反应Ⅰ、Ⅱ的速率均增加,且反应Ⅰ的速率增加得快 |
| D.反应Ⅰ、Ⅱ的速率均增加,且反应Ⅱ的速率增加得快 |
试题篮
()