下列说法正确的是
| A.增大反应物浓度可以增大活化分子百分数,从而使反应速率增大 |
| B.汽车尾气的催化转化装置可将尾气中的NO和CO等有害气体快速地转化为N2和CO2,其原因是催化剂可增大NO和CO反应的活化能 |
| C.在“反应热的测量实验”中测定反应后温度的操作方法:将量筒中的NaOH溶液经玻璃棒引流缓缓倒入盛有盐酸的简易量热计中,立即盖上盖板,并用环形玻璃搅拌棒不断搅拌,准确读出并记录反应体系的最高温度 |
| D.研制性能优良的催化剂既可以提高化学反应速率,又能起到很好的节能效果 |
在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g) 2Z(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表:
| t/min |
2 |
4 |
7 |
9 |
| n(Y)/mol |
0.12 |
0.11 |
0.10 |
0.10 |
下列说法正确的是( )
A.反应前2min的平均速率v(Z)=2.0×10-5mol/(L•min)
B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2mol Z,平衡时X的体积分数增大
已知:2CH3OH(g) CH3OCH3(g)+H2O(g) △H=" -25" kJ•mol-1。某温度下的平衡常数为400。此温度下,在1L体积不变的密闭容器中加入CH3OH,某时刻测得各组分的物质的量浓度如下表,下列说法中不正确的是( )
CH3OCH3(g)+H2O(g) △H=" -25" kJ•mol-1。某温度下的平衡常数为400。此温度下,在1L体积不变的密闭容器中加入CH3OH,某时刻测得各组分的物质的量浓度如下表,下列说法中不正确的是( )
| 物质 |
CH3OH |
CH3OCH3 |
H2O |
| c/(mol•L-1) |
0.08 |
1.6 |
1.6 |
A.此时刻反应达到平衡状态
B.容器内压强不变时,说明反应达平衡状态
C.平衡时,再加入与起始等量的CH3OH,达新平衡后CH3OH转化率不变
D.平衡时,反应混合物的总能量降低40kJ
在容积一定的密闭容器中,置入一定量的NO(g)和足量C(s),发生反应C(s)+2NO(g) CO2(g)+N2(g),平衡状态时NO(g)的物质的量溶液c(NO)与温度T的关系如下图所示,则下列说法中,正确的是( )
CO2(g)+N2(g),平衡状态时NO(g)的物质的量溶液c(NO)与温度T的关系如下图所示,则下列说法中,正确的是( )
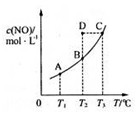
| A.该反应的△H>0 |
| B.若该反应在T1、T2时的平衡常数分别为K1、K2,则K1<K2 |
| C.在T2时,若反应体系处于状态D,则这时一定有v正<v负 |
| D.在T3时,若混合气体的密度不再变化,则可以判断反应达到平衡状态C |
某化学研究小组探究外界条件对化学反应mA(g)+nB(g) pC(g)的速率和平衡的影响图像如下,下列判断正确的是( )
pC(g)的速率和平衡的影响图像如下,下列判断正确的是( )
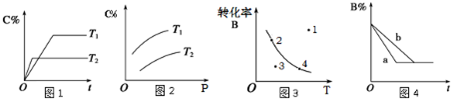
| A.由图1可知,T1<T2,该反应正反应为吸热反应 |
| B.由图2可知,该反应m+n<p |
| C.图3中,表示反应速率v正>v逆的是点3 |
| D.图4中,若m+n=p,则a曲线一定使用了催化剂 |
下列说法正确的是( )
| A.自发反应在任何条件下都能实现 |
| B.化学反应不一定都有能量变化 |
| C.升高温度,活化分子百分数增大,化学反应速率一定增大 |
| D.一般使用催化剂可以降低反应的活化能,增大活化分子百分数,从而提高反应物的转化率 |
等质量的三份铁a、b、c,分别加入足量的等量稀H2SO4中,a中同时加入适量CuSO4溶液,c中加入适量CH3COOK。下列各图中表示产生氢气总体积(V)与时间(t)的关系,其中可能正确的是( )


高温下,某可逆反应达到平衡,其平衡常数为K= ,恒容时,升高温度,H2的浓度减小,则下列说法正确的是( )
,恒容时,升高温度,H2的浓度减小,则下列说法正确的是( )
| A.该反应的焓变为正值 |
| B.升高温度,K值减小 |
| C.升高温度,逆反应速率减小 |
D.该反应的化学方程式为CO(g)+H2O(g) CO2(g)+H2(g) CO2(g)+H2(g) |
在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g) 2SO3(g)△H<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )
2SO3(g)△H<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )

| A.图Ⅰ表示的是t1时刻增大O2的浓度对反应速率的影响 |
| B.图Ⅱ表示的是t1时刻加入催化剂后对反应速率的影响 |
| C.图Ⅲ表示的是催化剂对化学平衡的影响,且甲的催化效率比乙高 |
| D.图Ⅲ表示的是压强对化学平衡的影响,且乙的压强较高 |
可使C(s)+ CO2(g)=2CO(g)反应速率增大的措施是( )
①增大压强 ②增加炭的量 ③通入CO2
④恒压下充入N2 ⑤恒容下充入N2 ⑥升温
| A.①③④ | B.②④⑥ | C.①③⑥ | D.③⑤⑥ |
已知反应:2CH3COCH3(l)⇌CH3COCH2COH(CH3)2(l).取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y﹣t)如图所示.下列说法正确的是( )

| A.b代表0℃下CH3COCH3的Y﹣t曲线 |
B.反应进行到20min末,CH3COCH3的 |
| C.升高温度可缩短反应达平衡的时间并能提高平衡转化率 |
D.从Y=0到Y=0.113,CH3COCH2COH(CH3)2的 |
100mL浓度为2mol/L的盐酸跟略过量的锌片反应,为减慢反应速率,又不影响生成氢气的总量,可采用的方法是( )
| A.加入适量的6mol/L的盐酸 | B.加入数滴氯化铜溶液 |
| C.加入适量醋酸钠溶液 | D.加入适量的NaOH固体 |
试题篮
()