将纯锌片和纯铜片按图示 方式插入同浓度的稀硫酸中一段时间,叙述正确的是
方式插入同浓度的稀硫酸中一段时间,叙述正确的是
| A.两烧杯中铜片表面均无气泡产生 |
| B.甲中铜片是正极,乙中铜片是负极 |
| C.甲中铜被氧化,乙中锌被氧化 |
| D.产生气泡的速率甲比乙快 |
钒()及其化合物广泛应用于工业催化、新材料和新能源等领域.
(1)是接触法制硫酸的催化剂.
①一定条件下,与空气反映t
后,
和
物质的量浓度分别为
和
, 则
起始物质的量浓度为mol/L ;生成
的化学反应速率为
.
②工业制硫酸,尾气用吸收.
(2)全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如题29图所示.

①当左槽溶液逐渐由黄变蓝,其电极反应式为
②充电过程中,右槽溶液颜色逐渐由色变为色.
③放电过程中氢离子的作用是和;充电时若转移的电子数为3.01 1023个,左槽溶液中
1023个,左槽溶液中的变化量为.
铜锌原电池(如图所示)工作时,下列叙述正确的是:

| A. |
正极反应是:
|
| B. |
电池反应是:
|
| C. | 在外电路中电子从负极流向正极 |
| D. |
盐桥中的
|
对于锌、铜和稀硫酸组成的原电池(如图),下列有关说法不正确的是( )
| A. Zn是负极 | B.Cu是正极 |
| C.负极上发生氧化反应 | D.正极上发生氧化反应 |
Ⅰ、某同学根据离子方程式:2Fe3++Cu===2Fe2++Cu2+设计了一套原电池装置,从而实现了该反应。在下面画出该原电池的示意简图(正极材料为碳棒,标明正、负极及电极材料和电解质溶液)。
II 、锌锰干电池是应用最普遍的电池之一(如图所示),其基本反应为:
X极:Zn—2e-====Zn2+
Y极:2MnO2+2NH4++2e-====Mn2O3+2NH3+H2O
Y极是电池的_________(填“正”或“负”)极,若反应消耗16.25gZn,则电池中转移电子的物质的是为________________。
银锌电池是广泛用做各种电子仪器的电源,其放电过程可表示为Ag2O+Zn==ZnO+2Ag,此电池放电时,负极上发生反应的物质是( )
| A.Ag | B.ZnO | C.Ag2O | D.Zn |
据报道,最近摩托罗拉公司研发出一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。其电池反应为: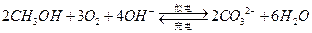 ,则下列说法错误的是( )
,则下列说法错误的是( )
A.放电时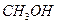 参与反应的电极为正极 参与反应的电极为正极 |
| B.充电时电解质溶液的pH逐渐增大 |
C.放电时负极的电极反应为: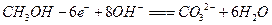 |
D.充电时每生成1 mol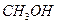 转移6 mol电子 转移6 mol电子 |
固体氧化物燃料电池(SOFC)以固体氧化物作为电解质,O2-可以在其内部自由通过。其工作原理如图所示。下列关于固体燃料电池的有关说法正确的是 ( )

A.电极b为电池负极,电极反应式为O2+4e- 2O2-
2O2-
B.固体氧化物的作用是让电子在电池内通过
C.若H2作为燃料气,则接触面上发生的反应为H2+2OH--4e- 2H++H2O
2H++H2O
D.若C2H4作为燃料气,则接触面上发生的反应为C2H4+6O2--12e- 2CO2+2H2O
2CO2+2H2O
把a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连可以组成几个原电池。若a、b 相连时a为负极;c、d相连时电流由d到c;a、c相连时c极上产生大量气泡;b、d相连时b上有大量气泡产生,则四种金属的活动性顺序由强到弱为 ( )
| A.a>b>c>d | B.a>c>d>b | C.c>a>b>d | D.b>d>c>a |
有A、B、C、D四种金属,当A、B组成原电池时,电子流动方向A →B ;当A、D组成原电池时,A为正极;B与E构成原电池时,电极反应式为:E2-+2e-=E,B-2e-=B2+则A、B、D、E金属性由强到弱的顺序为
A.A>B>E>D B.A>B>D>E C.D>E>A>B D.D>A>B>E
据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱作电解质溶液的新型手机电池,电量可达现在使用的镍氢或锂电池的十倍,可连续使用一个月才充一次电,其电池反应为:2CH3OH+3O2+4OH-====2 +6H2O,则下列有关说法不正确的是( )
+6H2O,则下列有关说法不正确的是( )
| A.放电时化学能转变为电能 |
| B.放电时CH3OH参与正极反应 |
| C.充电时阴极产生CH3OH |
| D.充电时每生成1 mol CH3OH,则转移6 mol电子 |
试题篮
()