下列电极反应既可以在原电池中发生,又可以在电解池中发生的是()
A.4OH--4e- 2H2O+O2↑ 2H2O+O2↑ |
B.O2+2H2O+4e- 4OH- 4OH- |
C.Cu2++2e- Cu Cu |
D.2H++2e- H2↑ H2↑ |
铅蓄电池作电源时,正极材料是PbO2,负极材料是Pb,内充稀硫酸,两极总反应为Pb+PbO2+2H2SO4 2PbSO4+2H2O,当电压由2.0 V下降到1.85 V,应停止使用,进行充电,则阴极的电极反应式为( )
2PbSO4+2H2O,当电压由2.0 V下降到1.85 V,应停止使用,进行充电,则阴极的电极反应式为( )
A.PbO2+4H++2e- Pb2++2H2O Pb2++2H2O |
B.Pb-2e- Pb2+ Pb2+ |
C.PbSO4+2e- Pb+SO Pb+SO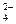 |
D.PbSO4+2H+-2e- PbO2+4H++SO PbO2+4H++SO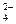 |
铅蓄电池的两极分别为Pb、PbO2,电解质溶液为H2SO4,工作时的反应为Pb+PbO2+2H2SO4====2PbSO4+2H2O,下列结论正确的是( )
| A.Pb为正极被氧化 |
| B.溶液的pH不断减小 |
C. 只向PbO2处移动 只向PbO2处移动 |
| D.电解质溶液pH不断增大 |
下列叙述正确的是( )
①原电池是把化学能转化成电能的一种装置 ②原电池的正极发生氧化反应,负极发生还原反应 ③不能自发进行的氧化还原反应,通过原电池的装置均可实现 ④碳棒不能用来作原电池的正极 ⑤反应Cu+2Ag+====2Ag+Cu2+,能以原电池的形式来实现
| A.①⑤ | B.①④⑤ | C.②③④ | D.②⑤ |
下列各烧杯中均盛有海水,铁在其中被腐蚀由快到慢的顺序为( )

图1
| A.①②③④⑤ | B.②①③④⑤ | C.④②①③⑤ | D.④⑤①②③ |
银器皿日久表面逐渐变黑色,这是由于生成硫化银,有人设计用原电池原理进行“抛光” ,其处理方法为:将一定浓度的食盐溶液放入一铝制容器中,再将变黑的银器浸入溶液中,放置一段时间后,黑色会褪去而银恢复光泽,且不会损失,试回答:
(1)食盐的作用是 。
(2)在此原电池反应中,负极发生的电极反应为 ,正极发生的电极反应为 。
(3)反应过程中产生臭鸡蛋气味的气体,溶液中发生的反应为 ,原电池总反应方程式为 。
(4)实际操作中,配制食盐水时,通常还加入一定量的小苏打,其主要作用是 ,这一反应的化学方程式是 。
(6分)铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为:
铅蓄电池示意图
Pb+PbO2+4H++2
 2PbSO4+2H2O
2PbSO4+2H2O
请完成下列问题(不考虑氢、氧的氧化还原):
(1)放电时:正极的电极反应式是
____________________________________________________;电解液中H2SO4的浓度将变_________________;当外电路通过1 mol电子时,理论上负极板的质量增加
_________________g。
(2)在完全放电耗尽PbO2和Pb时,若按右图连接,电解一段时间后,则在A电极上生成
_____________________、B电极上生成_____________________,此时铅蓄电池的正负极的极性将__________________________________。
下列叙述正确的是( )
①原电池是把化学能转变成电能的一种装置 ②原电池的正极发生氧化反应,负极发生还原反应 ③不能自发进行的氧化还原反应,通过原电池的装置可以实现 ④碳棒不能用来作原电池的负极 ⑤反应Cu +2Ag+====Cu2++2Ag可以进行
| A.①③⑤ | B.①④⑤ | C.②③④ | D.②⑤ |
随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要原因是( )
| A.利用电池外壳的金属材料 |
| B.防止电池中汞、镉和铅等重金属离子对土壤和水源的污染 |
| C.不使电池中渗泄的电解液腐蚀其他物品 |
| D.回收其中石墨电极 |
在由铜片、锌片和200 mL稀硫酸组成的原电池中,若锌片口只发生电化学腐蚀,当在铜片上共放出2.24 L气体(标准状况)时,稀H2SO4刚好用去一半,则产生这些气体消耗锌___________g,共有___________mol电子通过导线,原H2SO4溶液的浓度是________mol/L
(1)今有2H2+O2 2H2O反应,构成燃料电池,则负极通的应是____________,正极通的应是____________,电极反应式为:______________、______________。
2H2O反应,构成燃料电池,则负极通的应是____________,正极通的应是____________,电极反应式为:______________、______________。
(2)如把KOH改为稀H2SO4作导电物质,则电极反应式为____________、____________,(1)和(2)的电解液不同,反应进行后,其溶液的pH各有何变化?
(3)如把H2改为甲烷,KOH作导电物质,则电极反应式为____________。
下列叙述是小明做完铜、锌原电池的实验后得出的结论和认识,你认为正确的是( )
| A.构成原电池正极和负极的材料必须是两种金属 |
| B.由铜、锌作电极与硫酸铜溶液组成的原电池中铜是负极 |
| C.电子沿外导线由锌流向铜,通过硫酸溶液被氢离子得到而放出氢气 |
| D.铜锌原电池工作时,若有13 g锌被溶解,电路中就有0.4 mol电子通过 |
航天技术上使用的氢氧燃料电池具有高能、轻便、不污染环境等优点。氢氧燃料电池有酸式和碱式两种。它们放电时的电池总反应式均可表示为2H2+O2====2H2O。酸式氢氧燃料电池中的电解质是酸,其负极反应可表示为2H2====4H++4e-,则其正极反应可表示为_____________________,碱式氢氧燃料电池中的电解质是碱,其正极反应可表示为O2+2H2O+4e-====4OH-,则其负极反应可表示为______________________________。
熔融盐燃料电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为阳极燃气,空气与CO2的混合气为阴极燃气,制得在650 ℃下工作的燃料电池,完成有关的电池反应式:
阳极反应式:2CO+2
 4CO2+4e-
4CO2+4e-
阴极反应式为_____________________,总电池反应为_______________________、还原剂是________________。
试题篮
()