在右图所示的原电池中,下列说法正确的是( )

A.正极反应为 Cu - 2e-  Cu2+ Cu2+ |
| B.溶液中H+向锌片移动 |
| C.电子由锌片通过导线流向铜 |
| D.该装置能将电能转化为化学能 |
镁电池毒性低、污染小,电压高而平稳,它逐渐成为人们研制绿色电池的关注焦点。其中一种镁电池的反应原理为:

下列说法正确的是( )
| A.放电时,Mo3S4发生氧化反应 |
| B.放电时,负极反应式:Mo3S4+2xe-→Mo3S42x- |
| C.充电时,Mg2+向阴极迁移 |
| D.充电时,阳极反应式:xMg2++2xe-→xMg |
对于原电池的电极名称,叙述错误的是( )
| A.发生氧化反应的一极为负极 | B.正极为电子流入的一极 |
| C.比较不活泼的金属为负极 | D.电流流出的一极为正极 |
将反应IO3-+5I-+6H+ 3I2+3H2O设计成如下图所示的原电池,甲、乙烧杯中都加入淀粉溶液。开始时向甲烧杯中加入少量浓硫酸,电流计指针发生偏转,一段时间后,电流计指针回到零,再向甲烧杯中滴入几滴浓NaOH溶液,电流计指针再次发生偏转。下列判断不正确的是( )
3I2+3H2O设计成如下图所示的原电池,甲、乙烧杯中都加入淀粉溶液。开始时向甲烧杯中加入少量浓硫酸,电流计指针发生偏转,一段时间后,电流计指针回到零,再向甲烧杯中滴入几滴浓NaOH溶液,电流计指针再次发生偏转。下列判断不正确的是( )

| A.两次电流计指针偏转方向相反,电流计读数为零时,反应达到化学平衡状态 |
| B.两次实验中,盐桥中的阳离子移动方向相反 |
| C.开始加入少量浓硫酸时,只有乙烧杯中溶液变蓝。 |
| D.向甲烧杯中滴入几滴浓NaOH溶液后,乙中石墨电极上发生还原反应 |
锌铜原电池产生电流时,阳离子( )。
| A.移向Zn极,阴离子移向Cu极 | B.移向Cu极,阴离子移向Zn极 |
| C.和阴离子都移向Zn极 | D.和阴离子都移向Cu极 |
中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如下图所示。
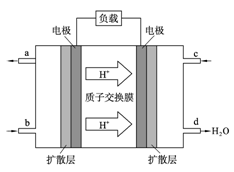
(1)该电池工作时,b口通入的物质为____________,c口通入的物质为__________。
(2)该电池负极的电极反应式为_________________。
(3)工作一段时间后,当6.4 g甲醇完全反应生成CO2时,有__________NA个电子转移。
(4)若将a口排放出的1.12L气体,通入到5L0.015mol·L-1NaOH溶液中完全反应。反应后的溶液中离子浓度由大到小的顺序为 。
如下图所示装置中,观察到电流计指针偏转,M棒变粗,N棒变细,由此判断下表中所列M、N、P物质,其中可以成立的是( )
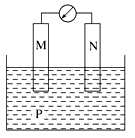
| |
M |
N |
P |
| A |
Zn |
Cu |
稀硫酸溶液 |
| B |
Cu |
Fe |
稀盐酸溶液 |
| C |
Ag |
Zn |
硝酸银溶液 |
| D |
Zn |
Fe |
硝酸铁溶液 |
某同学做完Zn-Cu-H2SO4组成的原电池的实验后,在读书卡片上作了如下记录,其中合理的是( )
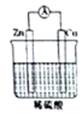

| A.①②③ | B.④⑤⑥ | C.③④⑤ | D.②③⑥ |
有关如下图所示原电池(盐桥中装有含琼胶的KCl饱和溶液)的叙述,正确的是
| A.铜棒上有气泡逸出 |
| B.取出盐桥后,电流计依然发生偏转 |
| C.反应中,盐桥中的K+会移向CuSO4溶液 |
| D.反应前后铜棒质量不改变 |
钢铁在潮湿的空气中会被腐蚀,发生的原电池反应为:2Fe+2H2O+O2=2Fe2++4OH-。以下说法正确的是
| A.负极发生的反应为:Fe-2e-==Fe2+ |
| B.正极发生的反应为:2H2O+O2+2e-==4OH- |
| C.原电池是将电能转变为化学能的装置 |
| D.钢柱在水下部分比在空气与水交界处更容易腐蚀 |
关于铅蓄电池的说法正确的是( )
| A.在放电时,正极发生的反应是Pb(s)+SO42-(aq)=PbSO4(s)+2e- |
| B.在放电时,该电池的负极材料是铅板 |
| C.在充电时,电池中硫酸的浓度不断变小 |
| D.在充电时,阳极发生的反应是 PbSO4(s)+2e-=Pb(s)+SO42-(aq) |
被称之为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰。在纸内是离子“流过”水和氧化锌组成的电解液。电池总反应为:
Zn + 2 MnO2十H2O =" ZnO" + 2MnO(OH)。下列说法正确的是
| A.该电池的正极为锌 |
| B.该电池反应中二氧化锰起催化剂作用 |
| C.当 0.lmol Zn 完全溶解时,流经电解液的电子个数为 1.204×l023 |
| D.电池正极反应式为: 2MnO2 + 2e一+ 2H2O =" 2MnO" (OH)十2OH- |
试题篮
()