如图所示,各烧杯中盛有海水,铁(含杂质C)在其中被腐蚀由快到慢的顺序为( )
A.⑤④②①③⑥ B.⑤④③①②⑥ C.②①③④⑤⑥ D.⑤③②④①⑥
从07年的“嫦娥奔月”到08年的“神七问天”,中国航天事业一次又一次取得了骄人战绩。这些人造卫星在宇宙中运行的能量来源于太阳的光能,其原理是:一定条件下光解水得到H2、O2,然后H2、O2在一定条件下形成氢氧燃料电池,两个过程循环往复。下列关于该氢氧燃料电池的说法中正确的是
| A.其总反应为: 2H2+O2 ="=" 2H2O |
| B.通入O2的一极为负极 |
| C.若电解质溶液为稀H2SO4,电池工作时,SO42-向通入H2的一极移动 |
| D.该原电池是将氢氧燃烧的热能转化为电能的一种装置 |
原电池电极的“正”与“负”不仅与电极材料的性质有关,也与电解质溶液有关.下列说法中正确的是( )
| A.由Fe、Cu和FeCl3溶液组成的原电池中,负极反应式为:Cu-2e-===Cu2+ |
| B.由Al、Cu和稀硫酸组成的原电池中,负极反应式为:Cu-2e-===Cu2+ |
| C.由Al、Mg和NaOH溶液组成的原电池中,负极反应式为:Al+4OH--3e-===AlO+2H2O |
| D.由Al、Cu和浓HNO3溶液组成的原电池中,负极反应式为:Al-3e-===Al3+ |
如图所示,把锌片和铜片用导线相连后插入稀硫酸溶液中构成原电池。下列叙述正确的是 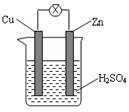
| A.该装置将化学能转变为电能 | B.电流从锌片流向铜片 |
| C.一段时间后,铜片质量减轻 | D.锌片发生还原反应 |
原电池是将化学能直接转化为电能的装置,原电池反应的本质是
| A.化合价的升降 | B.离子定向移动 |
| C.氧化还原反应 | D.电能的储存 |
在下图所示的原电池中,正极发生的反应是( )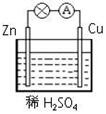
| A.H2-2e- ==2H+ | B.Cu-2e- ="=" Cu2+ |
| C.2H+ + 2e- ="=" H2↑ | D.Zn-2e- ="=" Zn2+ |
在500 mL KNO3和Cu(NO3)2的混合溶液中c(NO- 3)="6" mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4 L气体(标准状况),假定电解后溶液体积仍为500 mL,下列说法正确的是
| A.原混合溶液中 c(K+)为2 mol•L-1 | B.上述电解过程中转移电子总数为2 NA |
| C.电解得到的Cu的物质的量为0.5 mol | D.电解后溶液中c(H+)为2 mol·L-1 |
原电池产生电流的本质原因是 ( )
| A.原电池中溶液能电离出自由移动的离子 |
| B.有导线将两个活动性不同的电极连接 |
| C.正极发生了氧化反应,负极发生了还原反应 |
| D.电极上进行的氧化还原反应中有电子的转移 |
将下表中各组的两电极用导线相连后放入盛有对应该组的溶液中,能产生电流的是
| 序号 |
电极1 |
电极2 |
溶液 |
| A |
Cu |
Cu |
稀H2SO4 |
| B |
Ag |
Zn |
稀H2SO4 |
| C |
Cu |
Cu |
酒精 |
| D |
C |
C |
ZnSO4溶液 |
Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如右。该电池工作时,下列说法正确的是( )
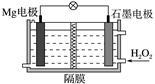
| A.Mg电极是该电池的正极 |
| B.H2O2在石墨电极上发生氧化反应 |
| C.石墨电极附近溶液的pH增大 |
| D.溶液中Cl-向正极移动 |
下图为水果电池的示意图,下列说法正确的是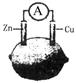
| A.锌片作负极,质量逐渐减少 | B.电子由铜片沿导线流向锌片 |
| C.铜电极逐渐溶解 | D.该装置能将电能转化为化学能 |
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )
| A.两烧杯中铜片表面均无气泡产生 |
| B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的pH均增大 |
| D.产生气泡的速度甲比乙慢 |
试题篮
()