关于下列装置的说法正确的是
| A.装置①中盐桥内的K+移向CuSO4溶液 |
| B.装置①将电能转变为化学能 |
| C.若装置②用于铁棒镀铜,则N极为铁棒 |
| D.若装置②用于电解精炼铜,溶液中的Cu2+浓度保持不变 |
化学与社会、生活密切相关。对下列现象或事实的解释正确的是
| 选项 |
现象或事实 |
解释 |
| A |
碱性锌锰电池比普通锌锰电池性能好 |
锌在碱性介质中被氧化成更高价态 |
| B |
配制FeCl2溶液时加入少量铁粉 |
抑制Fe2+的水解 |
| C |
施肥时,草木灰(有效成分为K2CO3)不能与铵盐氮肥混合使用 |
它们反应生成氨气会降低肥效 |
| D |
纯水和干木头都不导电,但木头用水浸湿后却可以导电 |
水和干木头的某些成分发生化学反应 |
某学习小组用实验验证牺牲阳极的阴极保护法装置如右图所示,下列说法正确的是: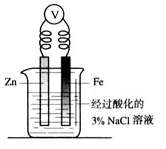
| A.实验过程会观察到电压表指针有偏转,是产生气流所致; |
| B.Zn电极作为负极,发生还原反应; |
| C.向烧杯中滴入铁氰化钾后,铁电极附近出现蓝色沉淀; |
| D.实验过程加入氯化钠是增大电解质溶液的离子浓度以加快反应速率。 |
某同学设计了如图所示的盐桥式原电池,下列说法正确的是( )

| A.X若为Fe、Y可以为Na2SO4溶液 |
| B.X若为Cu、Y可以为AgNO3溶液 |
| C.电子由X电极经盐桥流向Ag电极 |
| D.盐桥中的K+向左侧烧杯移动、Cl-向右侧烧杯移动 |
微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示(质子交换膜只允许H+通过)。下列有关微生物电池的说法错误的是
| A.正极反应中有CO2生成 |
| B.微生物促进了反应中电子的转移 |
| C.质子通过交换膜从负极区移向正极区 |
| D.电池总反应为C6H12O6+6O2=6CO2+6H2O |
铜锌原电池(如图)工作时,下列叙述正确的是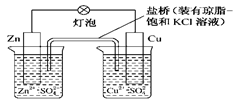
| A.正极反应为Zn-2e-===Zn2+ |
| B.电池反应为Zn+Cu2+===Zn2++Cu |
| C.在外电路中,电子从正极流向负极 |
| D.盐桥中的K+移向ZnSO4溶液 |
铅酸蓄电池是目前应用普遍的化学电池,新型液流式铅酸蓄电池以可溶性的甲基磺酸铅为电解质,电池总反应为:Pb+PbO2+4H+ 2Pb2++2H2O。下列有关新型液流式铅酸蓄电池的说法正确的是
2Pb2++2H2O。下列有关新型液流式铅酸蓄电池的说法正确的是
| A.放电时负极反应式为Pb-2e﹣+SO42﹣=PbSO4 |
| B.充放电时,溶液的导电能力变化不大 |
| C.以该电池电解NaCl溶液时,当消耗207gPb时,在阳极生成Cl222.4L |
| D.充电时的阳极反应式为Pb 2++2e-+4OH﹣=PbO2+2H2O |
若将反应:Zn+H2SO4=ZnSO4+H2↑,用锌、铜作电极设计成原电池(装置如图),则下列说法正确的是( )

| A.d溶液是稀硫酸 | B.c溶液颜色变蓝 |
| C.b极发生氧化反应 | D.a极是铜棒 |
利用如图装置探究铁在海水中的电化学腐蚀与防护。下列说法不正确的是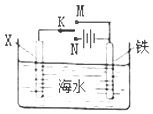
| A.若X为锌棒,开关K置于M处,可减缓铁的腐蚀,采用了牺牲阳极的阴极保护法 |
| B.若X为锌棒,开关K置于N处,X极的反应:4OH--4e-=O2↑+2H2O |
| C.若X为碳棒,开关K置于N处,可减缓铁的腐蚀,采用了外加电流的阴极保护法 |
| D.若X为碳棒,开关K置于M处,X极的反应:O2+4e-+2H2O=4OH- |
液体燃料电池相比于气体燃料电池具有体积小等优点.一种以液态肼(N2H4)为燃料 的电池装置如图所示,该电池以空气中的氧气为氧化剂,以 KOH 溶液为电解质溶液.下列关于该电池的叙述错误的是( )
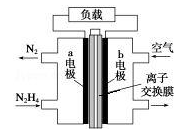
| A.b 极发生还原反应 | |
B.a 极的反应式为 N2H4﹣4e﹣═N2↑+4H+ |
C.放电时,电流从 b 极经过负载流向 a 极 |
| D.其中的离子交换膜需选用阴离子交换膜 |
X、Y、Z都是金属,把X浸入Z的硝酸盐溶液中,X的表面有Z析出,X和Y组成原电池时,Y为电池的负极.X、Y、Z三种金属的活动性顺序为
| A.X>Y>Z | B.X>Z>Y | C.Y>X>Z | D.Y>Z>X |
某原电池结构如右图所示,下列有关该原电池的说法正确的是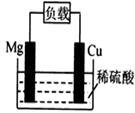
| A.电池反应为:Mg+2H+=Mg2++H2↑ |
| B.镁棒发生还原反应 |
| C.电子从铜棒经外电路流向镁棒 |
| D.铜棒为负极 |
下列说法正确的是( )

| A.图a中,随着电解的进行,溶液中c(H+)增大 |
| B.图b中,Mg电极做电池负极 |
| C.图c中,发生的反应为Co+Cd2+=Cd+Co2+ |
| D.图d中,K分别与M、N连接,Fe电极均受到保护 |
下列说法正确的是
| A.铁表面镀铜时,铁与电源的正极相连,铜与电源的负极相连 |
B.向氨水中不断通入CO2,随着CO2的增加, 不断增大 不断增大 |
| C.3C(s)+ CaO(s)=CaC2(s)+ CO(g)在常温下不能自发进行,说明该反应的△H>0 |
| D.合成氨时,其他条件不变,升高温度,反应速率v(H2)和氢气的平衡转化率均增大 |
试题篮
()